��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����йػ�ѧ�����ʾ��ȷ���ǣ�?��
A��Ư����Ч�ɷֵĻ�ѧʽ��CaClO
B��Na+�Ľṹʾ��ͼ��
C��ԭ�Ӻ�����10�����ӵ���ԭ�ӣ�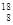 O
O
D��NaHCO3��ˮ��Һ�еĵ��뷽��ʽ��NaHCO3=Na++H++CO32��
�ο��𰸣�C
���������
���������A��Ư�۵���Ч�ɷֵĻ�ѧʽӦΪCa��ClO��2������B��Na+��ԭ�Ӻ���Ӧ��11�����ӣ�����C��818Oԭ�Ӻ�����10�����ӣ���ȷ��D��NaHCO3��ˮ��Һ�еĵ��뷽��ʽӦΪ��NaHCO3=Na++HCO3-������ѡC��
�����Ѷȣ�һ��
2��ѡ���� ij��Ӧ�з�Ӧ������������: AsH3��H2SO4��KBrO3��K2SO4��H3AsO4��H2O��һ��δ֪����X����֪0.1mol KBrO3�ڷ�Ӧ�еõ�0.5mol��������X��������˵���������
A�����������뻹ԭ����ļ���ϵ��֮��Ϊ5��2
B�������ԣ�KBrO3��H3AsO4
C��AsH3��AsԪ�ر�����������������Ӧ
D��X�Ļ�ѧʽΪBr2
�ο��𰸣�A
�����������
�����Ѷȣ�һ��
3������� ��֪��������Ͷ��ˮ���ܷ������з�Ӧ��2Na2O2+2H2O=4NaOH+O2������7.8g��������Ͷ������ˮ�У�������NaOH?�����ʵ����������ɵ�O2�ڱ�״���µ������
�ο��𰸣�2Na2O2+2H2O�T4NaOH+O2��
? 156g?4mol?22.4L
? 7.8g?n��NaOH��?V��O2��
��ã�n��NaOH��=7.8g��4mol156g=0.2mol?
V��O2��=7.8g��22.4L156g=1.12L
������NaOH?�����ʵ���Ϊ0.2mol������NaOH?�����ʵ���Ϊ1.12L��
���������
�����Ѷȣ�һ��
4��ѡ���� ��98%��Ũ����(�ܶ�Ϊ1��84 g��cm��3)����1 mol��L��1��ϡ����100 mL��������Һʱ�����õ��������Тٲ��������ڽ�ͷ�ιܣ���100 mL����ƿ����������ƽ����50 mL�ձ�����10 mL��Ͳ������ȷ��ѡ��˳����(? )
A���ޢۢݢ٢�
B���ޢݢۢ٢�
C���ܢݢۢڢ�
D���ޢݢ٢ۢ�
�ο��𰸣�D
����������ܶ�Ϊ1��84 g��cm��3��98%��Ũ����Ũ��Ϊ18��4 mol��L��1�����ø�Ũ��������100 mL 1 mol��L��1��ϡ����ʱ��ҪŨ��������Ϊ5��4 mL���������õ�10 mL��Ͳ��ϡ��ʱ���õ�50 mL�ձ��Ͳ�������ת��ʱ�õ�100 mL����ƿ������ʱ����Ҫ��ͷ�ιܡ�
�����Ѷȣ���
5��ѡ���� ���з�Ӧ�У�ˮ��Ϊ����������
A��SO2��H2O��Ӧ
B��Al��NaOH��Һ��Ӧ
C��NO2��H2O��Ӧ
D��Na2O2��H2O��Ӧ
�ο��𰸣�B
���������A�SO2��H2O��Ӧ���ڷ�������ԭ��Ӧ��B�Al��NaOH��Һ��Ӧ������Al����H2O��Ӧ��2A1+6H2O=2Al(OH)3+3H2������Al(OH)3��NaOH������Ӧ��2Al(OH)3+2NaOH=2NaAlO2+4H2O������ʽ��ӵã�2A1+2NaOH+2H2O=2NaAlO2+3H2������Al�ǻ�ԭ����H2O����������C�3NO2+H2O=2HNO3+NO��NO2�������������ǻ�ԭ����D�2Na2O2+2H2O=4NaOH+O2����2mol Na2O2����1molNa2O2ʧȥ2 mol��������1 molO2����1 mol Na2O2�õ�2 mol��������2molNaOH����Na2O2�������������ǻ�ԭ����
�����Ѷȣ���