��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��6�֣���V1 ml? 1.0 mol���� HCl��Һ��V2 mlδ֪Ũ�ȵ�NaOH��Һ��Ͼ��Ⱥ��������¼��Һ���¶ȣ�ʵ������ͼ��ʾ��ʵ����ʼ�ձ���V1+V2="=50" ml�������������в���ȷ����

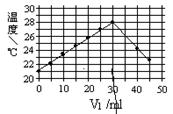
A����V1="=30" mlʱ�������NaOH��Һǡ����ȫ��Ӧ
B��NaOH��Һ��Ũ��ԼΪ1.5 mol����
C������ʵ��ʱ�����¶�Ϊ22��
D����ʵ�������ѧ�ܿ���ת��Ϊ����
�ο��𰸣�C��6�֣�
����������кͷ�Ӧ�Ƿ��ȷ�Ӧ������ǡ�÷�Ӧʱ����Һ���¶���ߣ�A��ȷ������ǡ�÷�Ӧʱ�����������������Һ�����֮����3�U2�������������Ƶ�Ũ����1.0mol/L��3/2��1.5mol/L��B��ȷ������������Ϊ0ʱ������������Һ���¶���21�棬����C����ȷ����Ӧ�Ƿ��ȷ�Ӧ������D��ȷ����ѡC��
�����Ѷȣ�һ��
2��ѡ���� �� pHΪ3��FeCl3��Һ��pH Ϊ11��Na2CO3��Һ�� pH Ϊ 3����������ˮ���������H����Ũ�ȷֱ�Ϊ��C1��C2��C3����֮��Ĺ�ϵ��
A��C1< C2< C3
B��C1= C2> C3
C��C1> C2> C3
D�����ж�
�ο��𰸣�B
���������
��ȷ�𰸣�B
�� pHΪ3��FeCl3��Һ��pH Ϊ11��Na2CO3��Һ�� pH Ϊ 3����������ˮ���������H����Ũ�ȷֱ�Ϊ���ٽ�ˮ���룬10-3mol/L���ٽ�ˮ���룬10-3mol/L������ˮ���룬10-11mol/L��B����ȷ��
�����Ѷȣ���
3��ʵ����
�� ȷ��ȡ�ռ���Ʒ4.1g������Ʒ���250mL�Ĵ���Һ����Ҫ��������������ƽ��С�ձ�����Ͳ����������?��?��(������)
�� ��?������ʽ������ʽ�����ζ�����ȡ10.00mL����Һע����ƿ�С�
������ƿ������ˮϴ�Ӻ�ˮδ������������Ʒ���ռ����������________(�ƫ�ߡ�����ƫ�͡�����Ӱ�족)��?
�����ζ������յ�ʱ�����Ӷ����ζ��ܶ�����������Ʒ���ռ����������________ (�ƫ�ߡ�����ƫ�͡�����Ӱ�족)��
�ɵζ�ʱ�ߵα�ҡ����ƿ���۾�Ӧ�۲�______��
A���ζ�����Һ��ı仯? B����ƿ����Һ��ɫ�ı仯
�ʵζ��ﵽ�յ�ʱ������?��
�� �������вⶨ���ݣ������õ��������ݣ���������ռ���Һ��Ũ�ȣ�?��
�����
| ����Һ���/mL
| ���������/mL
|
�ζ�ǰ������mL��
| ��������mL��
|
��һ��
| 10.00
| 0.50
| 20.40
|
�ڶ���
| 10.00
| 4.00
| 24.10
|
������
| 10.00
| 5.70
| 25.70
|
�� ��֪�������Ũ��Ϊ0.2010 mol��L���������������ⶨ���ݣ������õ��������ݣ������ռ�Ĵ���?��
�ο��𰸣���12�֣���6��7��8ÿ��2�֣�����1�֣�
�� 250mL����ƿ����ͷ�ι�
�� ��ʽ? ����Ӱ��? ��ƫ��? ��B?
����Һǡ���ɺ�ɫ����ɫ���Ұ�����ڲ���ɫ
�� c(NaOH)=0.4020mol/L? ��98%
������������⿼�����к͵ζ��Ļ�����������Ҳ��һ������ʵ�飬һ��ͨ����β�����ƽ��ֵ�ķ������вⶨ��
��7���������ı�Һ�����ƽ��ֵΪ��20.00ml����NaOH��ҺΪ10.00ml����c(NaOH)=0.4020mol/L���������m(NaOH)="4.020" g������Ʒ�Ĵ���Ϊ��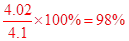
�����Ѷȣ�һ��
4��ѡ���� ���и������ʵ�ȼ������ȵ��ǣ�������
A��̼��һ����̼
B��1moL̼��2moL̼
C��3moL��Ȳ��1moL��
D�����ۺ���ά��
�ο��𰸣�A��C��D���ʲ�ͬ�����в�ͬ��������ȼ���Ȳ���ȣ�ȼ���������ʵ����ʣ������Ķ����أ���B��ȷ��
��ѡ��B��
���������
�����Ѷȣ�һ��
5��ѡ���� ����˵������ȷ����(����)
A������ʪ��pH��ֽ��ϡ����Һ��pH���ⶨֵƫС
B��CaCO3������ϡ���ᣬҲ�����ڴ���
C����Na2Sϡ��Һ�У�c(H��)��c(OH��)��2c(H2S)��c(HS��)
D���ζ�ǰ�ζ����������ݣ��յ����ʱ�����ݣ��������ƫС
�ο��𰸣�B
�����������pH��ֽ��ʪ�൱�ڰѴ�����Һϡ���ˣ��ⶨϡ����Һ��pHʱ���ƫС��A����ȷ��̼��Ƽȿ��Ժ����ᷴӦ��Ҳ���Ժʹ��ᷴӦ��ֻ�����ں����ᷴӦʱ�����ɵ�����Ƹ�����̼��Ʊ��棬��ֹ�˷�Ӧ�Ľ��У�B������ݵ���غ�c(Na��)��c(H��)��2c(S2��)��c(OH��)��c(HS��)�������غ�c(Na��)��2c(S2��)��2c(H2S)��2c(HS��)�ɵã�c(H��)��c(OH��)��2c(H2S)��c(HS��)��C����ȷ���ζ�ǰ�����ݣ��ζ��������ݣ����������Ϊ�����������������ռ����������������ƫС��D����ȷ��
�����Ѷȣ�һ��