��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ������O3������KI��Һ��Ӧ������O2�ȣ��ڷ�Ӧ�����Һ�е����̪��Ϊ��ɫ��������������Ϊ��ɫ��Ϊ�ⶨij���������еij�����������0�桢1.01��105Pa�Ŀ���33.6m3ͨ��KI��Һ��ʹ֮��ȫ��Ӧ��������Һ��0.0100mol-L-1��Na2S2O3��Һ60.0mLǡ�õζ����յ㣮��Ӧ����ʽΪ��2Na2S2O3+I2=Na2S4O6+2NaI��
��1������ͨ��KI��Һ�еĻ�ѧ����ʽ��______��
��2���ζ�������ѡ���ָʾ����______���ﵽ�ζ��յ�ʱ������Ϊ______��
��3������ÿ����г��������������
�ο��𰸣���1��O3��KI��ˮ��Ӧ����I2��KOH��O2����Ӧ����ʽΪO3+2KI+H2O=I2+2KOH+O2��
�ʴ�Ϊ��O3+2KI+H2O=I2+2KOH+O2��
��2���������۱���ɫ����ѡ�������ָʾ��������Һ����ɫ��Ϊ��ɫ���Ұ������ɫ���ٱ仯˵���ζ������յ㣮
�ʴ�Ϊ�����ۣ���Һ����ɫ��Ϊ��ɫ��
��3���ɻ�ѧ����ʽ�ã�
O3����������������I2������������2Na2S2O3
1mol? 2mol?
n��O3��? ?0.0100mol/L��0.0600L
����n��O3��=0.0100mol/L��0.0600L��1mol2mol=0.000300mol
������г������������Ϊ��0.000300mol��22.4L/mol33600L��100%=2��10-5%��
�𣺴����г������������Ϊ2��10-5%��
���������
�����Ѷȣ�һ��
2��ѡ���� �����л���1mol���ȼ�գ������������ǣ�������
A��C2H2
B��C2H6
C��C4H6
D��C4H8
�ο��𰸣�A��C2H2����x+y4=2+12=2.5����1molC2H2����2.5mol������
B��C2H6����x+y4=2+1.5=3.5����1molC2H6����3.5mol������
C��C4H6����x+y4=4+1.5=5.5����1molC4H6����5.5mol������
D��C4H8����x+y4=4+2=6����1molC4H8����6mol������
�ʺ�����������C4H8��
��ѡD��
���������
�����Ѷȣ�һ��
3������� ��ҵ�ϵ�ⱥ��ʳ��ˮ����ȡ���ֻ���ԭ�ϣ����в���ԭ�Ͽ������Ʊ��ྦྷ�裮��ͼ1�����ӽ���Ĥ��������������ͨ������������������������ͨ������ⱥ��ʳ��ˮ����������������������______��NaOH��Һ�ij���Ϊ______������ĸ�������Ʊ���ʳ��ˮ�Ľ���Ϊ______������ĸ������������Ӧʹ�õ�Һ����______��
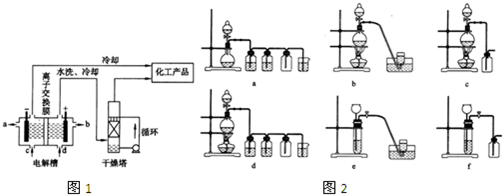
��1���ྦྷ����Ҫ����SiHC13��ԭ�����������丱����SiC14���ۺ������ܵ��㷺��ע��SiC14���������̿�ڣ�����ά��Ҫԭ����ͬ��������Ϊ������SiC14��H2��O2��Ӧ�����������֣���ѧ����ʽΪ______��SiC14��ת��ΪSiC13��ѭ��ʹ�ã�һ�������£���20L�����ܱ������з�Ӧ3SiC14��g��+2H2��g��+Si��s���T4SiHC13��g����ƽ���H2��SiHC13���ʵ���Ũ�ȷֱ�Ϊ0.140mol/L��0.020mol/L����H2ȫ����Դ�����ӽ���Ĥ���ĵ����������������NaC1������Ϊ______kg��
��2����ͼ2��ʵ�����Ʊ�H2��Cl2ͨ���������з�Ӧ��
Zn+H2SO4?ZnSO4+H2����MnO2+4HC1(Ũ)
MnC12+C12��+2H2O
�ݴˣ���������������װ����ѡ���Ʊ����ռ�H2��װ��______������ţ����Ʊ����ռ��������C12��װ��______������ţ���
��ѡ���Ʊ������װ�ã�
��3��������Ĥ���۵�ⱥ��ʳ��ˮ������ȡ�����ƣ�ͬʱ�������������Ƶ�������213.0kg������������______m3����״�����������Կ��ܴ��ڵ�������Ӧ��
�ο��𰸣���ⱥ��ʳ��ʱ����������Cl-��OH-�ŵ磬Cl-�ķŵ�����ǿ��OH-��
������2Cl--2e-�TCl2����
������2H++2e-�TH2����
�ܷ�ӦΪ��2NaCl+2H2O?���?.?Cl2��+H2��+2NaOH��
�����������ӷŵ磬������������ʹ����������Ũ�����������Ӻ����������ӵ��������������ң�����a���ڵ�����Һ��������������Һ��
�����������ӷŵ磬������������ʹ������Ũ�����ߣ�ͨ�������ӽ���Ĥ���������ң�����d���Ӧ���뾫�Ʊ���ʳ��ˮ��
Ҫ����Cl2��Ҫ�����Ը����Ũ�����P2O5�ȣ����Ը������ˮCaCl2��
�ʴ�Ϊ��������a��d��Ũ���
��1����SiCl4��H2��O2��Ӧ�����������֣����ά����Ҫ�ɷ���SiO2��H��ClԪ�ر�����һ�����У�H��ClԪ�ؽ�ϳ�HCl��Ȼ����ƽ���ɣ������Ļ�ѧ����ʽΪ��SiCl4+2H2+O2?����?.?SiO2+4HCl��
����3SiCl4��g��+2H2��g��+Si��s��?4SiHCl3��g��
��ʼ����mol��?n?0
�仯����mol��?2x?x?4x
ƽ������mol��?n-2x?4x
4x=0.020mol/L��20L=0.4mol��x=0.1mol��
n-2x=0.140mol/L��20L=2.8mol��n=3.0mol��
��2NaCl+2H2O ?���?.?Cl2��+H2��+2NaOH��
? 2mol?1mol
(2��58.5)g1mol=m(NaCl)3mol��m��NaCl��=350g=0.35kg
�ʴ�Ϊ��SiCl4+2H2+O2?����?.?SiO2+4HCl��0.35��
��2��ʵ������п��ϡ������ȡ�������÷�Ӧ�ǹ�Һ���̬�Ҳ���Ҫ���ȣ����Բ���Ҫ�ƾ��ƣ�������������ˮ���ܶ�С�ڿ����ܶȣ����Կ��Բ��������ſ���������ˮ���ռ�����ѡe��
ʵ������ȡ�����ǹ�Һ���̬����Ҫ���ȣ�������Ҫ�ƾ��ƣ�����������ˮ���ܶȴ��ڿ��������Բ��������ſ������ռ�����ѡd��
��3����NaClת��ΪNaClO3��ʧȥ������Ϊ6��H2Oת��ΪH2���õ��ĵ�����Ϊ2��
�������H2���ΪVm3��
�ɵ�ʧ�����غ�ã�6��213��103116.5mol=2��103V22.4mol��V=134.4m3���ʴ�Ϊ��134.4��
���������
�����Ѷȣ�һ��
4��ѡ���� G��Q��X��Y��Z��Ϊ�ȵĺ�����������Dz��˽����ǵĻ�ѧʽ����֪��������һ�������������µ�ת����ϵ(δ��ƽ)���� G �� Q + NaCl ?�� Q+ H2O X + H2?�� Y + NaOH �� G+ Q+H2O?�� Z + NaOH �� Q + X + H2O?�����ֻ������У��ȵĻ��ϼ��ɵ͵��ߵ�˳��Ϊ
X + H2?�� Y + NaOH �� G+ Q+H2O?�� Z + NaOH �� Q + X + H2O?�����ֻ������У��ȵĻ��ϼ��ɵ͵��ߵ�˳��Ϊ
A��GYZQX
B��GYQZX
C��QGZYX
D��ZXGYQ
�ο��𰸣�B
�����������G��QʮNaCl�У�NaCl��ClԪ��Ϊ-1�ۣ�������ͼۣ���ClԪ�صĻ��ϼ�ΪQ��G��-1����Q+ H2O X + H2�У�HԪ�صĻ��ϼ۽��ͣ���ClԪ�صĻ��ϼ����ߣ�����ClԪ�صĻ��ϼ�ΪX��Q����YʮNaOH��GʮQʮH2O�У���Ϣٿ�֪ClԪ�صĻ��ϼ�ΪQ��Y��G����ZʮNaOH��QʮXʮH2O�У���Ϣڿ�֪��ClԪ�صĻ��ϼ�ΪX��Z��Q���������ֻ��������ȵĻ��ϼ��ɵ͵��ߵ�˳��ΪGYQZX����ѡB��
X + H2�У�HԪ�صĻ��ϼ۽��ͣ���ClԪ�صĻ��ϼ����ߣ�����ClԪ�صĻ��ϼ�ΪX��Q����YʮNaOH��GʮQʮH2O�У���Ϣٿ�֪ClԪ�صĻ��ϼ�ΪQ��Y��G����ZʮNaOH��QʮXʮH2O�У���Ϣڿ�֪��ClԪ�صĻ��ϼ�ΪX��Z��Q���������ֻ��������ȵĻ��ϼ��ɵ͵��ߵ�˳��ΪGYQZX����ѡB��
�����Ѷȣ�һ��
5��ѡ���� �ڻ�ҩ��ըʱ������S+2KNO3+3C��K2S+N2��+3CO2�������б���ԭ�������ǣ�?��
A��S��KNO3
B��C ��S
C��KNO3
D��C ��KNO3
�ο��𰸣�A
�����������Ԫ�صĻ��ϼ۵ı仯��֪S��NԪ�صĻ��ϼۼ��ͣ�����ԭ�����ʵ�ΪS��KNO3��
�����Ѷȣ���