��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��4�֣���ͼ�Ǽס������ֹ������ʵ��ܽ�����ߡ�

��ش𣺼�������45��ʱ���ܽ��Ϊ?���ס��������ʵ��ܽ����ȵ��¶���?�棻Ҫʹ�ҵIJ�������Һ��Ϊ������ҺӦ?������ߡ��������͡����¶ȣ���ѹ�£�CO2��ˮ�е��ܽ�����¶ȵı仯Ӧ������?������ס������ҡ������ߡ�
�ο��𰸣�60g? t?����?��
�������������ͼ���֪����������45��ʱ���ܽ��Ϊ60g���ס��������ʵ��ܽ����ȵ��¶���t�棻�����ʵ��ܽ�����¶ȵ����߶����ͣ�����Ҫʹ�ҵIJ�������Һ��Ϊ������ҺӦ�����¶ȣ�������ܽ�����¶ȵ����߶����ͣ������������ҵġ�
�����Ѷȣ�һ��
2������� �������ȣ�ClO2����һ����ˮ�����ȷ����й㷺Ӧ�õĸ�Ч��ȫ��������������Cl2��Ȳ��������������DZ��Σ�����л��ȴ���Ʊ�ClO2���������ַ�����
����һ��2 NaClO3 + 4 HCl��2 ClO2��+ Cl2��+ 2 NaCl + 2 H2O
��������2 NaClO3 + H2O2 + H2SO4��2 ClO2��+ O2��+2 Na2SO4 + 2 H2O
��1������һ�����ӷ���ʽΪ ��
��2���������б������������� ������Ӧ����0.1mol����ת�ƣ��������ClO2�����ڱ�״���µ����Ϊ L��
��3���뷽��һ�Ƚϣ��÷������Ʊ���ClO2���ʺ���������ˮ������������Ҫԭ���� ��
�ο��𰸣���1��2ClO3-+ 4 H+ + 2Cl-��2 ClO2��+ Cl2��+ 2 H2O
��2��H2O2��2.24
��3������һ�Ƶõ�ClO2�к���Cl2
���������
���������(1)�������ӷ���ʽ����дԭ������������ĵ��������д���ӷ���ʽʱд��������ʽ��ɾȥ����ʽ���߲��μӷ�Ӧ�����ӣ���鷽��ʽ�����Ƿ�����Ԫ���غ㡢����غ㣬���Է���һ�����ӷ���ʽΪ��2ClO3-+ 4 H+ + 2Cl-��2 ClO2��+ Cl2��+ 2 H2O��
(2)����������ԭ��Ӧ���ۣ���������������Ԫ�ػ��ϼ����ߵ����ʣ��ڷ������У����ϼ����ߵ�Ԫ����H2O2�е���Ԫ�أ��� 91exam.org�Ա�������������H2O2��ÿ����1mol ClO2���壬��ת��1mol���ӣ����Ե���0.1mol����ת��ʱ��������0.1mol ClO2���壬��״���µ����Ϊ2.24L��
��3��������������ˮ����ʱ�ײ����������к����л��ȴ������һ�����������������Է��������ʺ��Ʊ�ClO2��
���㣺�������ӷ���ʽ����д��������ԭ��Ӧ���۵������Լ���ѧ�������е�Ӧ��
�����Ѷȣ�һ��
3��ѡ���� �����йػ�ѧ�����ʹ����ȷ���ǣ�?��
A��CH4���ӵı���ģ�ͣ�
B��NH3�ĵ���ʽ��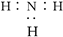
C��Cl���Ľṹʾ��ͼ��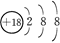
D��CO2�Ľṹʽ��O��C��O
�ο��𰸣�A
���������NH3�ĵ���ʽΪ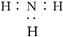 ��B����Cl���Ľṹʾ��ͼ�У�����������Ӧ����17����C����CO2���ӵĽṹʽӦ��ΪO��C��O��D����
��B����Cl���Ľṹʾ��ͼ�У�����������Ӧ����17����C����CO2���ӵĽṹʽӦ��ΪO��C��O��D����
�����Ѷȣ�һ��
4������� ��6�֣�
��1����˫���ű�����з�Ӧ�ĵ���ת�Ʒ������Ŀ������գ�
3Cu +8HNO3��3Cu(NO3)2 + 2NO��+ 4H2O
������������?��?��ԭ������??��
��2��д��������Ư��Ư��ԭ���Ļ�ѧ��Ӧ����ʽ��
??��
�ο��𰸣�
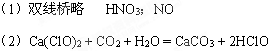
�����������
�����Ѷȣ�һ��
5������� ��100 mL NaOH��Һ��ͨ��CO2��ַ�Ӧ���ڼ�ѹ�ͽϵ��¶��£�С�ĵؽ���Һ���ɣ��õ���ɫ����M��ͨ�������̼�����V(��״����)��M������W�Ĺ�ϵ��ͼ
��ʾ����ش��������⣺
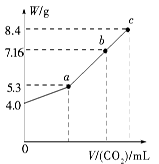
(1)b��ʱM����ɳɷ�Ϊ______________________��
(2)��Ҫʹb�����ɵ��ε�������Ϊ8.4 g����Ӧ��������Һ��ͨ�������̼________L(��״����)��
(3)�������ɵ�7.16 g�ε���Һ�м���һ������ij���ʣ���ַ�Ӧ��ѹ���������õ�������̼���ƹ���(�ᾧˮ)8.4 g��
����ֻ����0.03 molij���ʣ����������ʿ�����________��________��
����ֻ����0.06 molij���ʣ����������ʿ�����________��________��________��
(4)�����£�ͬŨ�ȵ�̼������Һ��̼��������Һ��pH
������7��������________��pH����������________________________��0.1 mol��L��1̼������Һ������Ũ�ȵĴ�С��ϵ��________����̼��������Һ����ε�������������Һ��������Ӧ�����ӷ���ʽΪ________��
�ο��𰸣�(1)Na2CO3��NaHCO3��(2)0.448
(3)��Na2O��Na2O2����Na��NaOH��NaH
(4)Na2CO3������ͬ�����£�CO32����ˮ��������HCO3����ˮ������ǿ��c(Na��)��c(CO32��)��c(OH��)��c(HCO3��)��c(H��)��Ba2����2OH����2HCO3��=BaCO3����CO32����2H2O
���������(1)��ͼ��֪����ʼʱ��������Ϊ4.0 g�����ʵ���Ϊ0.1 mol����ȫ������̼���ƣ���WΪ5.3 g����ȫ������̼�����ƣ���WΪ8.4 g��b���Ӧ�Ĺ���MΪ7.16 g������5.3 g��8.4 g֮�䡣��b���Ӧ�Ĺ���Ϊ̼���ƺ�̼�����ƵĻ���(2)��b���Ӧ�Ĺ�����̼���ơ�̼�����Ƶ����ʵ����ֱ�Ϊx��y������106 g��mol��1��x��84 g��mol��1��y��7.16 g,2x��y��0.1 mol����ã�x��0.02 mol��y��0.06 mol����Na2CO3��H2O��CO2=2NaHCO3�ã�n(CO2)��0.02 mol��(3)8.4 g Na2CO3�����ʵ���Ϊ0.08 mol�������⣬0.06 mol NaHCO3�D��0.06 mol Na2CO3�������ķ�ӦΪNaHCO3��NaOH=Na2CO3��H2O��n(NaOH)��0.06 mol������ˮ�����������Ƶ������У��ơ��������ơ������ơ��⻯��(NaH��H2O=NaOH��H2��)�����������ʡ�
�����Ѷȣ�һ��