��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ���л�����ף�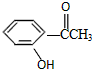 �ң�
�ң�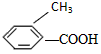 ����
����
��1����д�����к��������ŵ����ƣ�_____________��
��2�����б�������Щ�����ﻥΪͬ���칹�壺_________��
��3����ֱ�д������ס��ҡ���������ķ�����ָ����ѡ�Լ�����Ҫ���ɣ��� ����ķ�����
_________�� �����ҵķ�����_________�� ������ķ�����_________��
��4���밴������ǿ�������мס��ҡ�����˳��__________________��
�ο��𰸣���1��ȩ�����ǻ�
��2���ס��ҡ�����Ϊͬ���칹��
��3�������Ȼ�����Һ������ɫ���Ǽף���̼������Һ�������������ɵ����ң���������Һ���Ȼᷢ��������Ӧ���DZ�
��4���ң��ף���
���������
�����Ѷȣ�һ��
2������� ��12�֣�ʵ��������ˮ�ƾ���Ũ������1��3������Ȼ�ϼ�������ϩ���壬����д���пհף�
��1��д����ȡ��ϩ�Ļ�ѧ��Ӧ����ʽ_________?��
��2���¶���170�����ϻ�ʹ�Ҵ�̿���������ܷ���������ԭ��Ӧ�����ɶ�����̼���������������ˮ����д���÷�Ӧ�Ļ�ѧ����ʽ?��
��3��ʵ������Ƶõ���ϩ�����г������������壬���˻������ֱ��ͨ����ˮ���ܷ�֤����ϩ�����ӳɷ�Ӧ�����ʣ�__________����ܡ�����ԭ����______________
??��
��4��ʵ�����Ʊ���ϩ����Ũ������Ҫ������________?�������¶ȼ�ˮ�����λ����__________________��
�ο��𰸣���1�� CH3CH2OH 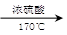 CH2��CH2����H2O
CH2��CH2����H2O
��2��C+2H2SO4(Ũ)="=" CO2��2SO2����2H2O
��3����?ԭ����SO2+Br2+2H2O=H2SO4+2HBr����SO2��ʹ��ˮ��ɫ��
��4����������ˮ��?����ӦҺ��
�������������ʵ������ȡ��ϩ�ĵ�ʵ��ԭ�����Ҵ���Ũ����Ĵ������·�����ȥ��Ӧ���õ���ϩ����ΪŨ���ỹ������ˮ�Ժ�ǿ�����ԣ������Ҵ����Ա�Ũ������������ΪŨ����Ļ�ԭ�����������Ҳ����ʹ��ˮ��ɫ�����Ի������ֱ��ͨ����ˮ�в���֤����ϩ�����˼ӳɷ�Ӧ��Ũ������������������֮�⣬������ˮ�������á���Ϊ���Ƶ�����Һ�¶ȣ������¶ȼ�ˮ����Ӧ���뵽��Һ�С�
�����Ѷȣ�һ��
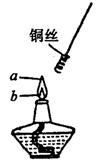
3��ʵ���� ��8�֣���ͼ��ijͬѧ���Ҵ�����ʵ��ʱ������״ͭ˿�ȷŵ�a�㴦���ȣ�Ȼ�����Ƶ�b�㣬����ͭ˿�ڻ����a��b����ʱ�������Բ�ͬ����д��a��b�����ʵ���������Ͳ����������ԭ��
?
| ʵ������
| �⡡������
|
a
| ?
| ?
|
b
| ?
| ?
�ο��𰸣�ͭ˿�ɺ��ڡ����洦�Ҵ����ȼ��
��������ͭ˿���ɺڱ�졡��о���Ҵ�δ���ȼ�ս�CuO��ԭ
����������������洦�ƾ�ȼ�ճ�֣�����a��ͭ˿�ɺ��ڣ�b������о���Ҵ�δ���ȼ�ս�CuO��ԭ�����ͭ˿���ɺڱ�졣
�����Ѷȣ�һ��
4��ʵ���� ij����С��������ͼװ�ý����Ҵ��Ĵ�����ʵ�鲢��ȡ��ȩ��ͼ������̨��װ�ü���ȥ���ֺ��߱�ʾ�齺�ܡ�����д���пհף�

��1����װ�ó��������¶�Ϊ70��80���ˮԡ�У�Ŀ����?��
��2��ʵ��ʱ���ȼ��Ȳ��������еĶ�����˿��Լ1���Ӻ�����������ʱͭ��˿���ʺ���״̬�����Ѿƾ��Ƴ��ߣ�����һ���Ĺ����ٶȣ�ͭ˿�ܳ�ʱ�䱣�ֺ���ֱ��ʵ�������
��3���Ҵ��Ĵ�������Ӧ��?��Ӧ������ȡ������ȡ������÷�Ӧ�Ļ�ѧ����ʽΪ?��
��4����ʵ������п��ƹ������ٶȺ���Ҫ:
�ٿ��ƹ����ٶȵķ�����?��
���������ٶȹ��췴Ӧ��ֹͣ,ԭ��?��
���������ٶȹ�����ӦҲ��ֹͣ,ԭ��?��
��5�����Թܶ�����ˮ���ղ����Ҫ�ڵ����ҡ���֮�������װ�ã������ӷ����ǣ�����װ���е��ܴ��ţ����ҽ�?��?�ӱ���
�ο��𰸣���1���ʵ��ӿ������Ҵ����������ʣ����ƽ�ȵ��Ҵ���������3�����ȣ�2CH3CH2OH��O2 2CH3CHO��2H2O����4���ٿ��Ƽ��е�λʱ�������������ڴ��߹������������Ա�֤��Ӧ�����¶ȣ��۷�Ӧ����̫�٣����ܴﵽ��Ӧ��Ҫ�¶ȣ�5��b��a 2CH3CHO��2H2O����4���ٿ��Ƽ��е�λʱ�������������ڴ��߹������������Ա�֤��Ӧ�����¶ȣ��۷�Ӧ����̫�٣����ܴﵽ��Ӧ��Ҫ�¶ȣ�5��b��a
�����������1����װ�ó��������¶�Ϊ70��80���ˮԡ�У�ˮԡ��ʹ�������Ⱦ��ȣ���ʹ�����Ҵ�ƽ���������Ҵ��������ʴ�Ϊ���ʵ��ӿ������Ҵ����������ʣ����ƽ�ȵ��Ҵ���������3��ʵ��ʱ���ȼ��Ȳ��������еĶ�����˿��Լ1���Ӻ�����������ʱͭ˿���ʺ���״̬�����Ѿƾ��Ƴ��ߣ�����һ���Ĺ����ٶȣ�ͭ˿�ܳ�ʱ�䱣�ֺ���ֱ��ʵ�������˵����Ӧ����������ȼ��ɽ��е��ף�˵���÷�Ӧ�Ƿ��ȵķ�Ӧ���Ҵ�����������������ȩ��ˮ���ʴ�Ϊ�����ȣ�2CH3CH2OH+O2 2CH3CHO+H2O����3���ٹ������ٶ�Խ�죬���е�λʱ����ð���������Խ�࣬��֮��Խ�٣��ʴ�Ϊ�����Ƽ��е�λʱ�������������ڹ����ٶȹ�����������������߹������������Ա�֤��Ӧ�����¶ȣ����·�Ӧֹͣ���ʴ�Ϊ�������ٶȹ�����������������߹������������Ա�֤��Ӧ�����¶ȣ��۹����ٶȹ�����Ӧ����̫�٣����ܴﵽ��Ӧ��Ҫ�¶ȣ����·�Ӧֹͣ���ʴ�Ϊ����Ӧ����̫�٣����ܴﵽ��Ӧ��Ҫ�¶ȣ���4��Ϊ��ֹ��ֹ����ˮ��������ȫƿ�еĵ������ǡ��̽������������Գ������л������ã��ʴ�Ϊ��b��a�� 2CH3CHO+H2O����3���ٹ������ٶ�Խ�죬���е�λʱ����ð���������Խ�࣬��֮��Խ�٣��ʴ�Ϊ�����Ƽ��е�λʱ�������������ڹ����ٶȹ�����������������߹������������Ա�֤��Ӧ�����¶ȣ����·�Ӧֹͣ���ʴ�Ϊ�������ٶȹ�����������������߹������������Ա�֤��Ӧ�����¶ȣ��۹����ٶȹ�����Ӧ����̫�٣����ܴﵽ��Ӧ��Ҫ�¶ȣ����·�Ӧֹͣ���ʴ�Ϊ����Ӧ����̫�٣����ܴﵽ��Ӧ��Ҫ�¶ȣ���4��Ϊ��ֹ��ֹ����ˮ��������ȫƿ�еĵ������ǡ��̽������������Գ������л������ã��ʴ�Ϊ��b��a��
�����Ѷȣ�һ��
5������� (1)1 mol�������ΪC3H8O��Һ̬�л���A���������Ľ��������ã�������11.2 L(��״��)��������A�����б���һ��?�������˻���̼����һ�ˣ���A����֧������A�Ľṹ��ʽΪ?��
(2)A��Ũ���Ṳ�ȣ���������ȥ1����ˮ������B��B�Ľṹ��ʽΪ?��Bͨ����ˮ���ܷ���?��Ӧ������C��C�Ľṹ��ʽΪ?��
(3)A��ͭ������ʱ���������ڼ��������·���������ԭ��Ӧ����D��D�Ľṹ��ʽΪ?��
д������ָ����Ӧ�Ļ�ѧ����ʽ��
��A��B?��
��B��C?��
��A��D?��
�ο��𰸣�(1)�ǣ�CH3CH2CH2OH
(2)CH3��CH��CH2���ӳɣ�CH3CHBr��CH2Br
(3)CH3CH2CHO
��CH3CH2CH2OH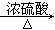 CH3CH��CH2����H2O CH3CH��CH2����H2O
��CH3CH��CH2��Br2�D��CH3CHBr��CH2Br
��2CH3CH2CH2OH��O2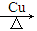 2CH3CH2CHO��2H2O 2CH3CH2CHO��2H2O
���������A�ķ���ʽ����ͨʽCnH2n��2O����������������ò���H2�����A�DZ���һԪ��������һ���ǻ������ǻ���̼����һ�ˣ�A����֧��������A�Ľṹ��ʽΪCH3CH2CH2OH��A������ȥ��Ӧ����B��CH3CH��CH2��B������ˮ�����ӳɷ�Ӧ��A��ͭ������ʱ�ܱ���������ΪCH3CH2CHO��
�����Ѷȣ�һ��
|