|
高考化学必考知识点《能量的相互转化》试题强化练习(2017年最新版)(六)
2017-07-10 18:45:52
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8分)下列是用化学方程式表示的化学变化,请在每小题后的横线上注明能量的转化形式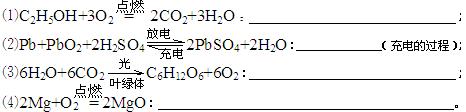
参考答案:8分)、⑴?化学能转化为热能?;?⑵?电能转化为化学能?;
⑶?太阳能转化为化学能(或生物质能)?;⑷?化学能转化为光能和热能
本题解析:略
本题难度:一般
2、选择题 美国普度大学的研究人员开发出一种利用铝镓合金制备氢气的新工艺(如图所示).?下列有关该工艺的说法错误的是( )
A.能量的转化形式只有两种
B.铝镓合金可以循环使用
C.铝镓合金与水反应的化学方程式为:2Al+3H2O Al2O3+3H2↑
D.总反应式为:2H2OH2↑+O2↑
| 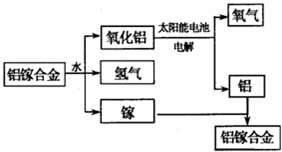
参考答案:A、该工艺中能量的转化形式有:太阳能转化为电能、电能转化为化学能、电能转化为热能,所以有三种形式的能量转化,故错误.
B、开始的反应物是铝镓合金,最终的生成物是铝镓合金,所以铝镓合金能循环使用,故正确.
C、铝镓合金与水的反应中生成物是氧化铝、氢气和镓,相当于镓未参加反应,所以实际上发生的反应是2Al+3H2O?一定条件?.?Al2O3+3H2↑,故正确.
D、该工艺中发生的反应有:2Al+3H2O?一定条件?.?Al2O3+3H2↑①,2Al2O3?电解?.?4Al+3O2②,将方程式①×12+②得方程式2H2O?一定条件?.?H2↑+O2↑,故D正确.
故选A.
本题解析:
本题难度:简单
3、选择题 已知反应?P+Q=M+N是放热反应,下列关于反应能量的变化的说法中不正确的是( )
A.断裂P和Q中化学键吸收的总能量小于形成M和N中化学键释放的总能量
B.P和Q的总能量大于M和N的总能量
C.P和Q的总能量小于M和N的总能量
D.任何化学反应都伴随着能量变化
参考答案:A.生成物化学键生成释放的能量高于反应物化学键断裂放出的能量,故A正确;
B.在放热反应中,反应物的能量高于生成物的能量,故B正确;
C.在放热反应中,反应物的能量高于生成物的能量,故C错误;
D.化学反应在生成新物质的同时,还伴随着能量的变化,故D正确.
故选C.
本题解析:
本题难度:一般
4、填空题 (12分) 2SO2(g)+O2(g)? ? 2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。 ? 2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。
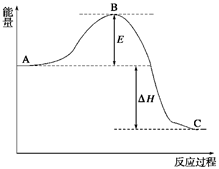
请回答下列问题:
(1) E的大小对该反应的反应热有无影响??。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低??;(2)图中ΔH=?kJ/mol;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式?;
?;
(4)如果反应速率v(SO2)为0.05 mol/(L・min),则
 v(O2)=?mol/(L・min)、v(SO3)=?mol/(L・min); v(O2)=?mol/(L・min)、v(SO3)=?mol/(L・min);
(5)已知S (s)+O2(g)? ?SO2(g) ΔH=-296 kJ/mol,计算由S(s)生成3 mol SO3(g)的ΔH?。 ?SO2(g) ΔH=-296 kJ/mol,计算由S(s)生成3 mol SO3(g)的ΔH?。
参考答案:(1)没有影响 降低
(2)-198? (3)SO2+V2O5===SO3+2VO2,4VO2+O2===2V2O5?(4)0.025 0.05?
(5)-1 185 kJ/mol
本题解析:(1)由图像可知E代表活化能,和反应热无关。催化剂能降低反应的活化能,从而加快反应速率。
(2)1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol,而方程式中二氧化硫是2mol,所以ΔH=-198 kJ/mol.
(3)根据所给元素化合价的变化可写出反应的方程式,SO2+V2O5===SO3+2VO2,4VO2+O2===2V2O5?。
(4)因为化学反应速率之比是相应的化学计量数之比,所以v(O2)=0.025mol/(L・min)、v(SO3)=0.05mol/(L・min).
(5)考查盖斯定律的应用。由反应① 2SO2(g)+O2(g) 2SO3(g)? ΔH=-198 kJ/mol和②S (s)+O2(g) 2SO3(g)? ΔH=-198 kJ/mol和②S (s)+O2(g) SO2(g)? ΔH=-296 kJ/mol联立即①+②×2得2S(s)+3O2(g) SO2(g)? ΔH=-296 kJ/mol联立即①+②×2得2S(s)+3O2(g) 2SO3(g)? ΔH=-790 kJ/mol,所以由S(s)生成3 mol SO3(g)的ΔH= 2SO3(g)? ΔH=-790 kJ/mol,所以由S(s)生成3 mol SO3(g)的ΔH= 。 。
本题难度:简单
5、选择题 根据热化学方程式:S(l)+O2(g)===SO2(g) ΔH=-293.23 kJ・mol-1,分析下列说法正确的是()
A.S(s)+O2(g)===SO2(g),反应放出的热量大于293.23 kJ・mol-1
B.S(g)+O2(g)===SO2(g),反应放出的热量小于293.23 kJ・mol-1
C.1 mol SO2的化学键断裂吸收的能量总和大于1 mol 硫和1 mol氧气的化学键断裂吸收的能量之和
D.1 mol SO2的化学键断裂吸收的能量总和小于1 mol硫和1 mol氧气的化学键断裂吸收的能量之和
参考答案:C
本题解析:反应热是断键吸收的总能量和形成化学键所放出的总能量的差值,所以根据热化学方程式可知,该反应是放热反应,这说明1 mol SO2的化学键断裂吸收的能量总和大于1 mol 硫和1 mol氧气的化学键断裂吸收的能量之和,C正确,D不正确。由于固态S的能量最小,液态其次,气态最高,所以气态S燃烧放出的热量最多,固态S燃烧放出的热量最少,AB都是错误的,答案选C。
点评:该题是高考中的常见题型,属于基础性试题的考查。试题基础性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和抽象思维能力。该题的关键是明确反应热的含义和影响反应热的因素,然后再结合题意灵活运用即可。
本题难度:简单
| 