微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列关于电解池的叙述中不正确的是( )
A.与电源正极相连的是电解池的阴极
B.与电源负极相连的是电解池的阴极
C.电解池的阳极发生氧化反应
D.电解池的阴极发生还原反应
参考答案:A
本题解析:电解池中与电源正极相连的是电解池的阳极,失去电子,发生氧化反应,所以选项A不正确,其余选项都是正确的,答案选A。
本题难度:一般
2、填空题 (1)将等物质的量的KI和CuCl2溶于水,用惰性电极电解,该电解反应可分为________个阶段(表格不一定填满,若不够还可以自行添加)。
阶段
| 相当于电解什么溶液
| 离子方程式
|
①
| ?
| ?
|
②
| ?
| ?
|
③
| ?
| ?
|
④
| ?
| ?
|
⑤
| ?
| ?
|
?
(2)画出过程中溶液pH随时间变化的曲线(假定生成的Cl2全部逸出)。

参考答案:
4 ①CuI2 Cu2++2I-=Cu+I2
②CuCl2 Cu2++2Cl-=Cu+Cl2↑
③KCl 2Cl-+2H2O=Cl2↑+H2↑+2OH-
④KOH 2H2O=2H2↑+O2↑

本题解析:
开始电解时阳极是I-失电子,阴极是Cu2+得电子;当I-完全反应时,Cu2+有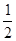 被还原,此时阳极变成Cl-失电子,相当于电解CuCl2溶液;当Cu2+完全反应时,Cl-有
被还原,此时阳极变成Cl-失电子,相当于电解CuCl2溶液;当Cu2+完全反应时,Cl-有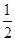 被氧化;以后阴极是H2O电离的H+得电子,此段相当于电解KCl溶液;当Cl-完全反应后,最后相当于电解KOH溶液,实质是电解水。
被氧化;以后阴极是H2O电离的H+得电子,此段相当于电解KCl溶液;当Cl-完全反应后,最后相当于电解KOH溶液,实质是电解水。
本题难度:一般
3、简答题 (14分)
对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(1)含氰废水中的CN-有剧毒。
①CN-中C元素显+2价, N元素显-3价,用原子结构解释N元素显负价的原因是?,共用电子对偏向N原子,N元素显负价。
②在微生物的作用下,CN-能够被氧气氧化成HCO3-,同时生成NH3,该反应的离子方程式为?。
(2)含乙酸钠和对氯酚(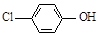 )的废水可以利用微生物电池除去,其原理如下图所示。
)的废水可以利用微生物电池除去,其原理如下图所示。
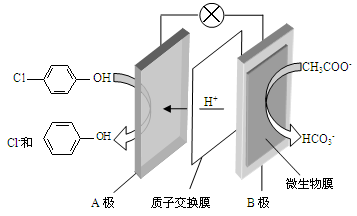
①B是电池的?极(填“正”或“负”);②A极的电极反应式为?。
(3)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如下图所示(图中“HA”表示乳酸分子,A- 表示乳酸根离子)。
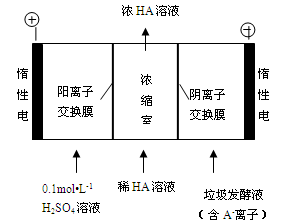
①阳极的电极反应式为?。
②简述浓缩室中得到浓乳酸的原理:?。
③ 电解过程中,采取一定的措施可控制阳极室的pH约为6-8,此时进入浓缩室的OH-可忽略不计。400mL 10 g?L-1乳酸溶液通电一段时间后,浓度上升为145 g?L-1(溶液体积变化忽略不计),阴极上产生的H2在标准状况下的体积约为?L。(乳酸的摩尔质量为90 g? mol-1)
参考答案:(14分)
(1)①C和N的原子电子层数相同(同周期),核电荷数C小于N,原子半径C大于N(吸引电子能力C弱于N)
注:以递变规律的方式表述也给分。如“C和N同周期,C在N的左边。同周期元素从左至右核电荷数逐渐增多,原子半径逐渐减小,核对最外层电子的引力逐渐减弱”)
② 2CN-+ 4H2O + O2  ?2HCO3- + 2NH3
?2HCO3- + 2NH3
(2)①负;②Cl- -OH + 2e- + H+ ="=="
-OH + 2e- + H+ ="=="  -OH + Cl-
-OH + Cl-
(3)①4OH--4e-="==" 2H2O+O2↑
② 阳极OH-放电,c(H+)增大,H+从阳极通过阳离子交换膜进入浓缩室(1分);A-通过阴离子交换膜从阴极进入浓缩室(1分),H+ +A- ="==" HA,乳酸浓度增大。
③ 6.72
本题解析:(1)①C和N的原子电子层数相同,核电荷数C小于N,原子半径C大于N,所以N吸引电子的能力强于C,表现为负价;
②,CN-能够被氧气氧化成HCO3-,同时生成NH3,根据所给反应物和生成物判断反应物中应有水参与,该反应的离子方程式为2CN-+ 4H2O + O2  ?2HCO3- + 2NH3
?2HCO3- + 2NH3
(2)①HCO3-中C为+4价,CH3COO-中C平均为0价,化合价升高,发生氧化反应,所以B极为负极;
②A极发生还原反应,对氯苯酚结合氢离子生成苯酚和氯离子,电极反应式为Cl- -OH + 2e- + H+ ="=="
-OH + 2e- + H+ ="=="  -OH + Cl-
-OH + Cl-
(3)①阳极的电极反应式为
本题难度:一般
4、填空题 (6分)下图表示一个精炼粗铜的电解池,电解液a选用CuSO4溶液,X、Y是两块电极板,通过导线与直流电源相连
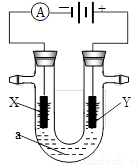
请回答以下问题
(1)Y电极的材料是 ,
(2)电极反应式是 ,
(3)X电极的现象是 。
参考答案:34.(1)粗铜 (2)Cu-2e-=Cu2+ (3)X电极上有红色的铜析出
本题解析:精炼粗铜时,粗铜做阳极,发生的主要反应为Cu-2e-=Cu2+,精铜做阴极,发生的电极反应为:Cu2++2e-=Cu,所以答案为:(1)粗铜 (2)Cu-2e-=Cu2+(3)X电极上有红色的铜析出。
考点:考查铜的电解精炼。
本题难度:一般
5、填空题 (14分)汽车尾气中CO、NOx 以及燃煤废弃中的SO2都是大气污染物,对它们的治理具有重要意义。
Ⅰ.CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H1=" ―574" kJ・mol- 1.
CH4(g) + 4NO(g) = 2N2(g)+ CO2(g)+2H2O(g) △H2= 一1160 kJ・mol- 1
(1)甲烷直接将NO2还原为N2的热化学方程式为 ;
Ⅱ.吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):
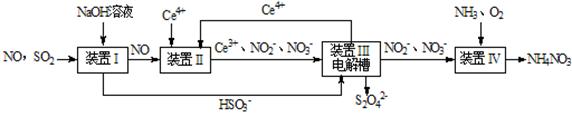
(2)装置Ⅱ中,酸性条件下,NO被Ce 4+ 氧化的产物主要是NO3- 、NO2- ,写出只生成NO3- 的离子方程式 ;
(3)装置Ⅲ的作用之一是再生Ce4+,其原理如下图所示。
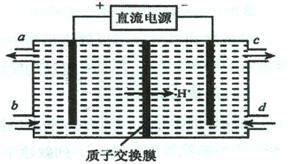
①生成的Ce4+ 从电解槽的 (填字母序号)口流出;
②生成S2O42 - 的电极反应式为 ;
(4)已知进入装置Ⅳ的溶液中,NO2- 的浓度为a g・L- 1 ,要使1m3该溶液中的NO2- 完全转化为NH4NO3,至少需向装置Ⅳ中通入标准状况下的O2 L。(用含a代数式表示,计算结果保留整数)
参考答案:(1)CH4(g)+2NO2(g)=2H2O(g)+ CO2(g)+N2(g) △H=-867kJ/mol
(2)NO+2H2O+3Ce4+=3Ce3++NO3-+4H+
(3)①a
②2H++2HSO3-+2e-=S2O42-+2H2O
(4)243a(或5600a/23)
本题解析:(1)根据盖斯定律,将两个已知热化学方程式相加得2CH4(g)+4NO2(g)=4H2O(g)+2 CO2(g)+2N2(g) △H=(―574 kJ・mol- 1)+(一1160 kJ・mol- 1)=-1734kJ/mol,所以甲烷直接将NO2还原为N2的热化学方程式为CH4(g)+2NO2(g)=2H2O(g)+ CO2(g)+N2(g) △H=-867kJ/mol
(2)由图可知,NO被Ce 4+ 氧化为NO3- ,则Ce4+被还原为Ce3+,所以只生成NO3- 的离子方程式为NO+2H2O+3Ce4+=3Ce3++NO3-+4H+
(3)①装置Ⅲ的作用之一是再生Ce4+,在电解池中,阳极上是Ce3+失电子成为Ce4+的过程,所以生成Ce4+从电解槽的阳极上a极流出,
②电解池的阴极发生得电子的还原反应,亚硫酸氢根离子得电子生成S2O42-,电极反应式为2H++2HSO3-+2e-=S2O42-+2H2O
(4)NO2-的浓度为a g?L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,则失去电子的物质的量是(1000×ag)/46g/mol×(5-3),设需要标准状况下的O2VL,则氧气得电子的物质的量是VL/22.4L/mol×2×(2-0),根据氧化还原反应中得失电子守恒定律,有(1000×ag)/46g/mol×(5-3)= VL/22.4L/mol×2×(2-0),解得V=243aL。
考点:考查盖斯定律的应用,离子方程式的书写,电化学反应原理的应用,氧化还原反应的计算
本题难度:一般