微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 现欲用浓度为5mol/L?的NaOH溶液配制?1mol/L?的NaOH溶液,应取?5mol/L的NaOH溶液与蒸馏水的体积比约为( )
A.1:4
B.1:5
C.2:1
D.2:3
参考答案:忽略稀释时体积的变化,混合后溶液体积为5mol/L的NaOH溶液与蒸馏水的体积之和.
令5mol/L的NaOH溶液与蒸馏水的体积分别为xL、yL,溶液稀释前后氢氧化钠的物质的量不变,则:
5mol/L×xL=1mol/L×(xL+yL).
解得x:y=1:4.
故选A.
本题解析:
本题难度:简单
2、选择题 下列说法正确的是
[? ]
A.?在标准状况下,22.4?L水的质量?为18g
B?.?22.4?L氧气含阿伏加得罗常数个氧分子
C.?22g二氧化碳与标准状况下11.2?L?HCl含有相同的分子数
D.?在同温同压下,相同体积的任何气体含有相同的原子数
参考答案:C
本题解析:
本题难度:简单
3、选择题 (1)相同质量的SO2、SO3的物质的量之比为____________;氧原子的个数之比为_ _______。
(2)19 g某二价金属氯化物(ACl2)中含有0.4 mol Cl-,则ACl2的摩尔质量是________;A的相对原子质量是____________;ACl2的化学式是__________。
参考答案:(1)5∶4 5∶6 (2)95 g・mol-1 24 MgCl2
本题解析:(1)根据 n=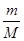 可知,相同质量的SO2、SO3的物质的量之比=
可知,相同质量的SO2、SO3的物质的量之比=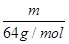 :
: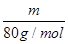 =5∶4;氧原子的个数之比=5×2∶4×3=5∶6。
=5∶4;氧原子的个数之比=5×2∶4×3=5∶6。
(2)19 g某二价金属氯化物(ACl2)中含有0.4 mol Cl-,则ACl2的物质的量=0.4mol÷2=0.2mol,因此根据n=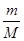 可知,该化合物的摩尔质量M=19.2g÷0.2mol=95 g/mol;氯元素的相对原子质量35.5,所以A的相对原子质量=95-35.5×2=24,因此A是Mg,则该化合物的化学式是MgCl2。
可知,该化合物的摩尔质量M=19.2g÷0.2mol=95 g/mol;氯元素的相对原子质量35.5,所以A的相对原子质量=95-35.5×2=24,因此A是Mg,则该化合物的化学式是MgCl2。
考点:考查物质的量的有关计算、化学式确定
本题难度:一般
4、选择题 在标准状况下,1molSO2的体积是( )2.24L
A.小于
B.等于
C.大于
D.无法判断