| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点归纳《物质的量》考点强化练习(2017年押题版)(四)
参考答案:C 本题解析:摩尔质量的单位是g/mol,而质量的单位是g,所以选项A和B都是错误的;根据 本题难度:一般 2、填空题 (10分)现有m g某气体X2,它的摩尔质量为M g・mol-1。若阿伏加德罗常数用NA表示,则: 参考答案: m/M ;2mNA/M ;22.4m/M; m/(m+1000) ;m/MV 本题解析:考查物质的量的有关计算。 本题难度:一般 3、选择题 配制100mL.1.0mol?L-1的NaOH溶液,下列情况会导致溶液浓度偏高的是( ) 参考答案:A.配制最后需加水定容,故容量瓶使用前有少量蒸馏水,对所配溶液浓度无影响,故A错误; 本题解析: 本题难度:简单 4、选择题 关于2mol二氧化碳的叙述中,正确的是 |
参考答案:B
本题解析:不正确,因为不一定是在标准状况下;CO2的摩尔质量是44g/mol,所以2molCO2的质量是88g,B正确;C不正确,分子数应该是2×6.02×1023;根据CO2的化学式可知,含有2mol×3=6mol原子,其中氧原子是4mol,碳原子是2mol,D不正确,答案选B。
考点:考查物质的量的有关计算
点评:该题是高考中的常见题型,属于基础性试题的考查。试题基础性强,侧重对学生基础知识的训练和检验。该类试题需要注意的是在进行物质的量的有关计算时,关键是熟练应用几个关系式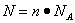 、n=m/M、
、n=m/M、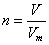 、
、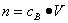 ,特别还要注意气体摩尔体积的使用条件,即只能适用于气体,且只有在标准状况下,气体的摩尔体积才是22.4L/mol。
,特别还要注意气体摩尔体积的使用条件,即只能适用于气体,且只有在标准状况下,气体的摩尔体积才是22.4L/mol。
本题难度:简单
5、实验题 实验室里需要纯净的氯化钠溶液,但手边只有混有硫酸钠、碳酸氢铵和氯化钠。某学生设计了如下图方案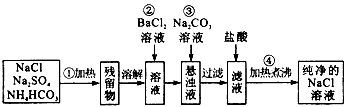
如果此方案正确,那么:
(1)操作①可选择_______或_______(填仪器名称)。
(2)操作②是否可改为加硝酸钡溶液?为什么?___________________________________
(3)进行操作②后,如何判断SO42-已除尽,方法是____________________________
(4)操作③的目的是___________,不必先过滤后加碳酸钠溶液,理由是_____________________。
(5)操作④的目的是______________________________。
参考答案:(1)蒸发皿;坩埚
(2)不可以,改用Ba(NO3)2会使溶液中引入新的杂质离子NO3-,以后操作中无法除去
(3)取少量上层清液加入BaCl2溶液,若无沉淀说明SO42-已除尽
(4)除去过量的Ba2+减少一次过滤操作
(5)除去溶解在溶液中的CO2和HCl
本题解析:
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《影响盐类水解的因.. | |