��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �����Ǹ������Դ���⣬���ú�ˮ����ȡ�������Ʒ��
��1���ȼҵ���Ե��ʳ��ˮΪ������ѧ��ҵ��д�����ʳ��ˮ�Ļ�ѧ����ʽ___________________________________________________________________.
��2���Ӻ�ˮ����ȡ�峣�ô���������������(Cl2)����ˮ���廯�ƣ�NaBr���е����û����������ÿ���������(Br2)������ʾ��ͼ���£�
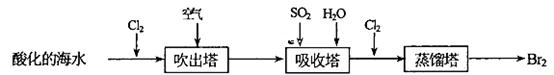
��д��������NaBr���û����嵥�ʵĻ�ѧ����ʽ��____________________;�÷�Ӧ��pH=3�����������½��У�����________�ⶨ��ӦҺ�����ȡ�
�ڴ�������ʹ�����������ڡ����������������������ͼ������ͨ��SO2��ˮ��Ŀ���ǡ�_____________________________________________________.���û�ѧ����ʽ��ʾ��
�ο��𰸣���1�� 2NaCl+2H2O Cl2����H2 ��+2NaOH
Cl2����H2 ��+2NaOH
��2����Cl2+2NaBr=2NaCl+Br2?PH��ֽ
��Br2+S02+2H20�TH2S04+2HBr
���������
��1�� 2NaCl+2H2O Cl2����H2 ��+2NaOH
Cl2����H2 ��+2NaOH
��2�����������������֪�������廯�ƿ����û����嵥�ʣ���Ӧ�����������廯�ƣ����������Ȼ��ƺ��壬���ݹ۲취��ƽ���ɣ��仯ѧ����ʽΪ��Cl2+2NaBr=2NaCl+Br2�������IJⶨ��Һ���ȵķ�����ʹ��pH��ֽ�ⶨ��Һ�����ȡ�
�������������з����ķ�Ӧ��Br2+S02+2H20�TH2S04+2HBr���Լ�����������Ŀ����ʹ�����������룻
�����Ѷȣ�һ��
2��ѡ���� ��15�֣��������[aFe2(SO4) 3��b(NH4) 2SO4��cH2O]�㷺���ڳ�����������ˮ����ҵѭ��ˮ�ľ��������ȡ�ij����������������������������ƣ��������Ϊԭ�ϣ���������¹���������ȡ������李�

��ش��������⣺
��1������������Һ��H2SO4�ữ����ҪĿ����____________________________������A����Ҫ�ɷ���__________________��
��2���������������ʺϵ�������B��?����Ӧ�����ӷ���ʽ?��
a��NaClO? b��H2O2? c��KMnO4? d��K2Cr2O7
��3�������ס��ҵ����Ʒֱ��ǣ���______________����___________________��
��4�����������У����������ʺϵ�������B����֮��ͼ�������֮ǰ����ȡ��������Fe2+�Ƿ���ȫ���������������Լ�Ϊ?��д���ƣ����ܷ������Ե�KMnO4��Һ��??������ܣ����ʺ��ԣ��������ǣ�?�����������ֻ�ʽ˵����
��5���������������NH4+�ķ�����?��
��6����ȡ14.00 g������Ʒ����������ˮ���Ƴ�100 mL��Һ���ֳ����ȷݣ�������һ���м�������NaOH��Һ������ϴ�ӵõ�2.14 g����������һ����Һ�м���0.05 mol Ba (NO3)2��Һ��ǡ����ȫ��Ӧ�����������淋Ļ�ѧʽΪ______________________��
�ο��𰸣�
��1��������Һ��SO42-Ũ�ȣ���Ca2+ת��Ϊ������ͬʱ����Fe2+�� Fe3+ˮ�⣻CaSO4.
��2��b;H2O2��2Fe2+��2H+��2Fe2+��2H2O
��3����ȴ�ᾧ����������
��4�����軯����Һ�����ܣ���Ϊ��������Ͷ��������Ӿ���ʹ���Ը��������Һ��ɫ
��5�����Թ��м���������Ʒ���������ƹ�����ȣ����Թܿ���ʪ��ĺ�ɫʯ����ֽ���飬������ֽ�����ɫ����6��Fe2(SO4)3��2(NH4)2SO4��2H2O
�����������1��������Һ��SO42-Ũ�ȣ���Ca2+ת��Ϊ������ͬʱ����Fe2+�� Fe3+ˮ�⣻CaSO4.
��2��b����ɫ��������������Լ����������µ����ʣ�H2O2��2Fe2+��2H+��2Fe2+��2H2O
��3����ȴ�ᾧ����������
��4���������������Ӧ��ʹ�û�ɫ�����軯��K3��Fe(CN)6����Һ����������������������ӷ�Ӧ���ɴ���������ɫ�����軯����������3Fe2+��2��Fe(CN)6��3-��Fe3��Fe(CN)6��2�������ܣ���Ϊ��������Ͷ��������Ӿ���ʹ���Ը��������Һ��ɫ
��5�����Թ��м���������Ʒ���������ƹ�����ȣ����Թܿ���ʪ��ĺ�ɫʯ����ֽ���飬������ֽ�����ɫ����֤��ԭ��Һ�к��а������ӡ�
��6��14.00 g������Ʒ�У������������Ƶõ�2.14 g����Ϊ��������������
n(Fe)��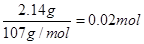
 ����һ����Һ�м���0.05 mol Ba (NO3)2��Һ��ǡ����ȫ��Ӧ�������ᱵ�����������Һ�е����������Ϊ0.05 mol ��Ҳ�������к��е�Fe2(SO4)3Ϊ0.01 mol��(NH4)2SO4Ϊ0.02 mol ����ʱ����Ϊ��0.01 mol ��400g/mol��0.02 mol ��132g/mol��6.64g��ʣ�µľ���H2O����������ôÿһ����Һ��ˮ������Ϊ��7.00g��6.64g��0.36g,n(H2O)��0.02 mol����˸�������淋Ļ�ѧʽΪ��Fe2(SO4)3��2(NH4)2SO4��2H2O
����һ����Һ�м���0.05 mol Ba (NO3)2��Һ��ǡ����ȫ��Ӧ�������ᱵ�����������Һ�е����������Ϊ0.05 mol ��Ҳ�������к��е�Fe2(SO4)3Ϊ0.01 mol��(NH4)2SO4Ϊ0.02 mol ����ʱ����Ϊ��0.01 mol ��400g/mol��0.02 mol ��132g/mol��6.64g��ʣ�µľ���H2O����������ôÿһ����Һ��ˮ������Ϊ��7.00g��6.64g��0.36g,n(H2O)��0.02 mol����˸�������淋Ļ�ѧʽΪ��Fe2(SO4)3��2(NH4)2SO4��2H2O
�����Ѷȣ�һ��
3��ѡ���� ���и���Һ��������÷�Һ©���������?
A���屽����
B���������ˮ
C������������
D���Ҵ���ˮ
�ο��𰸣�B
������������鳣���Ļ���ʵ���������Һ�����ڻ�������Һ��ķ��롣ѡ��A��C��D�����ʾ���ܽ⣬���ܽ��з�Һ�������鲻����ˮ����Һ����ʵ�ַ��룬��ѡB��
�����Ѷȣ���
4��ʵ���� ��8�֣��ⶨ����ͭ���壨CuSO4��5H2O����ᾧˮ�ĺ�����ʵ�鲽��Ϊ������ĥ?�ڳ�����������װ������������������?�ۼ���?����ȴ?�ݳ������ظ������ݵIJ�����ֱ���������γ��������������0.1 gΪֹ?�߸���ʵ�����ݼ�������ͭ������ᾧˮ�ĺ�����
��ش��������⣺
��1����������������ǯ�����żܡ������ǡ�����������������ҩ�ס�����ͭ������Ʒ��ʵ����Ʒ�����и�ʵ��ʱ��ȱ�ٵ�ʵ����Ʒ��
____________________________________________��
��2����ʵ������һ������Ҫʹ�ø�������ʹ�ø�������Ŀ����ʲô����
____________________________________________��
��3��ʵ�鲽���Ŀ����________________________________________________________��
��4����������ȷ��ʵ���õ�����ͭ�����нᾧˮ�ĺ���ƫ�ͣ���ԭ������У�����ѡ��ı�ţ���_______________________��
A��������Ʒ�к��м��Ȳ��ӷ�������
B��������Ʒ�к��м����ӷ�������
C��ʵ��ǰ������Ʒ���в���ʧˮ
D������ǰ���õ�����δ��ȫ����
�ο��𰸣���1���в���������ƽ���ƾ��ƣ����벻��������Ҳ���۷֣�?��2���ܣ���ȴ����ֹ��ˮ?��3��������Ʒ�� �Ľᾧˮ�Ƿ��Ѿ�ȫ����ȥ?��4��AC
���������������Դ�ڸ��л�ѧ�̲��е�һ��ѧ��ʵ�顣ͨ����ʵ�鿼����ѧ���Ļ���ʵ�����ʣ�ͬʱҲ������ѧ�����ۺϷ��������������Լ����ֱ���������
�������������ϸ߿���Ҫ����Դ�ڽ̲ĵ��������ڽ̲ġ������Ҫ����ƽʱ�Կα��еĸ���ʵ����һ������ʶ�����ա�
�����Ѷȣ���
5������� ��ѡ������ʵ�鷽���������ʣ������뷽����������ں����ϣ�
A�����ȷֽⷨ��B�����˷���C���ᾧ��D����Һ����E������
��1�����뱥��ʳ��ˮ��ɳ�ӵĻ����______��
��2������ˮ�����͵Ļ����______��
��3���������Ȼ�̼���е�Ϊ76.75�棩�ͼױ����е�Ϊ110.6�棩�Ļ����______��
�����������ʣ�A�������Ȼ���B��������C��̼���D���ƾ�E��������̼F��ͭG������������ҺH������
��4�����������У��ܵ������______������ǿ����ʵ���______�����ڷǵ���ʵ���______������ţ���
��5��д������B��G��ˮ�з�Ӧ�����ӷ���ʽ��______��
�ο��𰸣�I�����벻���Թ������Һ���ù��˵ķ��������뻥�����ܵ�Һ����÷�Һ�ķ��������뻥�ܵ�Һ���������ķ�����
��1�����뱥��ʳ��ˮ��ɳ�ӵĻ������ù��˷�������ѡB��
��2��ˮ�����Ͳ����ܣ��Ҷ���Һ�壬���Է���ˮ�����͵Ļ������÷�Һ��������ѡD��
��3�����Ȼ�̼�ͼױ������Ҷ���Һ�壬���Է������Ȼ�̼���е�Ϊ76.75�棩�ͼױ����е�Ϊ110.6�棩�Ļ���������������ѡE��
II��4�����������ƶ������ӻ���ӵ������ܵ��磬�����Ȼ��ơ�����������Һ�к��������ƶ����ӣ������ܵ��磬ͭ�к��������ƶ��ĵ��ӣ������ܵ��磬��ѡAFG��
��ȫ����ʵĵ������ǿ����ʣ������Ȼ��ơ�̼�������ǿ����ʣ���ѡAC��
��ˮ��Һ�������״̬�¶�������Ļ������Ƿǵ���ʣ��ƾ���������̼�����Ƕ��Ƿǵ���ʣ���ѡDEH��
�ʴ�Ϊ��AFG��AC��DEH��
��5��������������Ʒ����кͷ�Ӧ���ɴ����ƺ�ˮ�����ӷ���ʽΪ��CH3COOH+OH-=CH3COO-+H2O���ʴ�Ϊ��CH3COOH+OH-=CH3COO-+H2O��
���������
�����Ѷȣ�һ��