微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 同温同压下,甲容器中所盛气体为CH4,乙容器中所盛气体为C2H2.
(1)若甲、乙两容器中所含氢原子数相等,则两容器所盛气体的体积之比为______.
(2)若甲、乙两容器中所含气体质量相等,则两容器所盛气体的分子数之比为______.
(3)若甲、乙两容器中所含体积相等,则两容器所盛气体的质量之比为______.
参考答案:(1)由n=NNA=VVm可知,同温同压下,气体的体积之比等于分子数之比等于物质的量之比,若甲、乙两容器中所含氢原子数相等,两容器所盛气体的分子数之比为1:2,则两容器所盛气体的体积之比为1:2,故答案为:1:2;
(2)设甲、乙两容器中所含气体质量为m,由n=NNA=mM可知:N=m?NAM,则两容器所盛气体的分子数之比与相对分子质量呈反比,所以:N(CH4):N(C2H2)=26:16=13:8,故答案为:13:8;
(3)由n=mM=VVm可知:m=V?MVm,即若甲、乙两容器中所含体积相等,则两容器所盛气体的质量之比与气体的相对分子质量呈之比,则m(CH4):m(C2H2)=16:26=8:13,故答案为:8:13.
本题解析:
本题难度:一般
2、选择题 已知阿伏加德罗常数、物质的摩尔质量及摩尔体积,下列物理量中尚不能计算出其近似值的是?
[? ]
A.固体物质分子的大小和质量
B.液态物质分子的大小和质量
C.气体物质分子的质量
D.气体物质分子的大小
参考答案:D
本题解析:
本题难度:简单
3、选择题 下列说法正确的是
A.1mol H2的质量是1 g
B.1mol HCl的质量是36.5 g・mol-1
C.Cl2的摩尔质量等于它的相对分子质量
D.硫酸根离子的摩尔质量是96 g・mol-1
参考答案:D
本题解析:A 错误,1mol H2的质量是2g
B 错误,1mol HCl的质量是36.5 g
C 错误,Cl2的摩尔质量在数值上等于它的相对分子质量
D 正确
本题难度:简单
4、选择题 以NA代表阿伏加德罗常数,有关反应
C2H2(g)+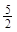 O2(g)→2CO2(g)+H2O(l);ΔH= -1300kJ/mol
O2(g)→2CO2(g)+H2O(l);ΔH= -1300kJ/mol
下列关于热化学方程式的说法正确的是(? )
A.有5NA个电子转移时,该反应放出1300kJ的能量
B.有NA个水分子生成且为液体时,吸收1300kJ的能量
C.有4NA个碳氧共用电子对生成时,放出1300kJ的能量
D.有8NA个碳氧共用电子对生成时,放出1300kJ的能量
参考答案:D
本题解析:根据方程式可知,每放出1300kJ的热量,反应中就转移10mol电子,生成2molCO2。由于CO2分子中含有4对共用电子对,所以正确的答案选D。
本题难度:简单
5、选择题 在一密闭气缸中,用一不漏气可滑动的活塞隔开,左边充有N2,右边充有H2和O2的混合气体,在20℃时,将右边混合气体点燃,反应后冷却到原来温度,若活塞原来离气缸左端的距离为总长的
,反应后静止于气缸的正中(忽略水蒸气),则原来H2和O2的体积比可能为( )
A.4:5
B.1:4
C.8:1
D.2:7
参考答案:左室中氮气的物质的量不变,令开始氮气的物质的量为1mol,左右两室压强相同,体积之比等于物质的量之比,故开始右室中氢气与氧气的物质的量为1mol×3414=3mol,反应后左右体积相等,则右室剩余气体的物质的量为1mol,则:
? 2H2+O2=2H2O? 气体物质的量减少△n
? 2? 1?3
?43mol? 23mol?3mol-1mol=2mol
若剩余气体为氢气,则原混合气体中氧气为23mol,则氢气为3mol-23mol=73mol,H2和O2的体积比为73mol:23mol=7:2,
若剩余气体是氧气,则原混合气体中氢气为43mol,则氢气为3mol-43mol=53mol,H2和O2的体积比为43mol:53mol=4:5,
故选A.
本题解析:
本题难度:一般