微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列电池属于二次电池的是

| 
| 
| 
|
A.锌银钮扣电池
| B.氢氧燃料电池
| C.铅蓄电池
| D.锌锰干电池
|
参考答案:C
本题解析:二次电池又称为充电电池,答案选C。
考点:化学电源
本题难度:简单
2、选择题 氢氧燃料电池已用于航天飞机,以30%KOH溶液为电解质溶液。电极反应如下:
2H2 +4OH--4e- = 4H2O,O2+2H2O+4e- = 4OH- 。据此作出判断,下列说法中不正确的是
[? ]
A.O2在正极发生还原反应
B.电池总反应为2H2 + O2 = 2H2O
C.反应时负极附近pH增大
D.氢氧燃料电池属于环境友好电池
参考答案:C
本题解析:
本题难度:一般
3、填空题 能源问题是当前世界各国所面临的严重问题,同时全球气候变暖,生态环境问题日益突出,开发氢能、研制燃料电池、发展低碳经济是化学工作者的研究方向。
I.氢气通常用生产水煤气的方法制得。其中CO(g)+H2O(g)? ?CO2(g)+H2(g)
?CO2(g)+H2(g)
△H<0。在850℃时,平衡常数K=1。
(1)若降低温度到750℃时,达到平衡时K?1(填“大于”、“小于”或“等于”)
(2)850℃时,若向一容积可变的密闭容器中同时充入1.0molCO、3molH2O、1.0molCO2
和x molH2,则:
①当x=5.0时,上述反应向?(填“正反应”或“逆反应”)方向进行。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是?。
③在850℃时,若设x=5.0和x=6.0,其它物质的投料不变,当上述反应达到平衡后,
测得H2的体积分数分别为a%、b%,则a?b(填“大于”、“小于”或“等于”)
II.已知4.6g液态乙醇完全燃烧生成二氧化碳和液态水放出热量136kJ・mol液态水转
化为气体水吸收44kJ的热量。
(3)请写出乙醇燃烧生成气态水的热化学方程式
?。
(4)将0.1mol乙醇在足量氧气中燃烧,得到的气体全部通入到100mL3mol/LNaOH溶液中,忽略HCO-3的电离,则所得溶液中c(CO2-3)?c(HCO-3)(填“大于”、“小于”或“等于”,)原因是?(用文字叙述)。
参考答案:(1)大于(2分)
(2)①逆反应(2分)? ②x<3(2分)? ③小于(2分)
(3)C2H5OH(l)+3C2(g)=2CO2(g)+3H2O(g)? △H=-1228kJ/mol(2分)
(4)小于(2分)? CO32-?水解程度大于HCO3-水解程度(2分)
本题解析:略
本题难度:一般
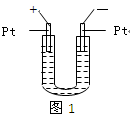
4、选择题 如图1所示,U形管中装入含有紫色石蕊的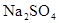 试液,通直流电,一段时间后U形管内会形成三色“彩虹”的现象,它从左到右颜色的次序是:(?)
试液,通直流电,一段时间后U形管内会形成三色“彩虹”的现象,它从左到右颜色的次序是:(?)
A.蓝、紫、红
B.红、蓝、紫
C.红、紫、蓝
D.蓝、红、紫
参考答案:C
本题解析:惰性电极电解硫酸钠溶液,相当于电解水。阴极是氢离子放电,所以阴极周围溶液选碱性。阳极是OH-放电产生氧气,所以阳极周围溶液显酸性。根据装置图可知,左侧是阳极,右侧电极是阴极,所以正确的答案是C。
本题难度:一般
5、填空题 (8分)水煤气不仅是合成氨的原料气也是合成烃及其化工产品的原料。
(1)在水煤气燃料电池中,通CO、H2的极为电池的 极(选填“正”、“负”)。
(2)水煤气变换反应:CO(g) + H2O(g)  CO2(g) + H2(g) △H<0,下列措施能提高反应速率的有 (不定项选择)。
CO2(g) + H2(g) △H<0,下列措施能提高反应速率的有 (不定项选择)。
a.升高温度 b.加入催化剂 c.增大压强 d.降低浓度
(3)H2和N2在催化剂、高温高压条件下合成氨的化学方程式为 。
(4)将标准状况下582.4L合成气[已知:n(CO)∶n(H2)= 4∶9]通入合成塔,一定条件下可发生2CO(g)+ 4H2(g) → CH2=CH2(g)+2H2O(g);CO(g)+3H2→CH4(g)+H2O(g),充分反应后,经测定产品中只有甲烷、乙烯和水蒸气(假定CO和H2均无剩余),逸出的气体中乙烯的物质的量为 。
参考答案:(1)负 (1分) (2)abc(1分) (3)N2 + 3H2 2NH3(1分)
2NH3(1分)
(4)3mol(共4分)
本题解析:(1)水煤气燃料电池中,CO、H2发生氧化反应,所以通CO、H2的极为电池的负极。
(2)a、升高温度,反应速率加快,正确;b、加入催化剂,反应速率加快,正确;c、增大压强,反应速率加快,正确,d、降低温度,反应速率减小,错误。
(3)H2和N2在催化剂、高温高压条件下合成氨的化学方程式为:N2 + 3H2 2NH3
2NH3
(4)标准状况下582.4L合成气物质的量为:582.4L÷22.4L/mol=26mol,则n(CO) +n(H2)= =26mol,因为n(CO)∶n(H2)= 4∶9,则n(CO)=26mol×4/(4+9)=8mol,n(H2)=26mol-8mol=18mol,由化学方程式:2CO(g)+ H2(g)→C2H4(g)+2H2O(g)和CO(g)+ 3H2(g) → CH4(g)+ H2O(g),可得:n(CH4)+2n(C2H4)="8mol" ,3n(CH4)+4n(C2H4)=18mol,解得n(C2H4)=3mol。
考点:本题考查原电池原理、影响化学反应速率的因素、化学方程式的书写与计算。
本题难度:一般