微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 胃酸过多是常见的胃病。下面是甲、乙两种常见胃药的说明摘要。
甲:
(1)白色结晶状粉末,可缓缓分解;
(2)能溶于水,水溶液呈弱碱性;
(3)遇酸及酸性药物则产生二氧化碳;
(4)胃酸过多患者服用多见胃胀气,甚至有引起胃溃疡穿孔的危险?。
乙:
(1)与胃酸作用是中和反应,作用缓慢而持久,可维持3~4小时。
(2)凝胶本身覆盖于溃疡面上,具有保护作用。
(3)可溶于稀酸或氢氧化钠溶液中。
(1)请你推测,甲中含有的主要化学成分是________(填化学式);乙中含有的主要化学成分是________(填化学式)。
(2)试写出甲中含有的主要化学成分引起胃胀气反应的离子方程式:__________________________。
(3)试写出乙中含有的主要化学成分溶于NaOH溶液的离子方程式:____________________________。
参考答案:(1)NaHCO3;Al(OH)3
(2)HCO3-+H+===H2O+CO2↑
(3)Al(OH)3+OH-===AlO2-+2H2O
本题解析:
本题难度:一般
2、填空题 (1)若向NaHSO4溶液中逐滴加入Ba(OH)2溶液,使原溶液中的SO42-恰好完全沉淀,试写出该反应的化学方程式_________________________
(2)明矾是一种无色晶体,可溶于水并形成Al(OH)3胶体来净水。已知明矾水溶液的主要成分是
KAl(SO4)2,现向明矾溶液中逐滴加入Ba(OH)2溶液,当Al3+恰好全部沉淀时,试写出该反应的化学方程式
_________________________。
参考答案:(1)NaHSO4+Ba(OH)2==BaSO4↓+H2O+NaOH
(2)2KAl(SO4)2+3Ba(OH)2==3BaSO4↓ + Al(OH)3↓+K2SO4
本题解析:
本题难度:一般
3、选择题 以下有关正三价铝的叙述正确的是
[? ]
A.当向溶液中加入强酸溶液时,氢氧化铝主要发生酸式电离
B.当向溶液中加入强碱溶液时,氢氧化铝主要发生碱式电离
C.在强酸性环境中正三价的铝以Al3+形式存在于溶液中
D.在pH较大的溶液中正三价的铝以Al3+形式存在于溶液中
参考答案:C
本题解析:
本题难度:简单
4、填空题 化学科学在药物的开发、合成和使用中起着至关重要的作用。如小苏打(NaHCO3)、氢氧化铝、三硅酸镁等可治疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答 91eXaM.org下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:__________________________。
(2)写出胃舒平药片(复方氢氧化铝)与胃酸(主要成分为稀盐酸)作用的离子方程式:
_______________________。
(3)若选氯水作氧化剂,将补铁剂中的Fe2+氧化成Fe3+,写出相关的离子反应__________________。
参考答案:(1)HCO3-+H+=H2O+CO2↑
(2)Al(OH)3+3H+=Al3++3H2O
(3)2Fe2++Cl2=2Fe3++2Cl-
本题解析:
本题难度:一般
5、填空题 盐R的化学式为XmYbZp(X、Y、Z为三种不同离子),其组成元素均为短周期元素,取两份等质量等浓度R的水溶液各5 mL进行如下实验:
I.取一份R的水溶液与过量的Ba(OH)2溶液反应,反应过程中生成白色沉淀,沉淀量先增加后减少,最终剩余沉淀甲2.33 g,且甲不溶于稀盐酸。
Ⅱ.取另一份R的水溶液与过量的NaOH溶液混合加热,生成具有刺激性气味的气体乙0.112 L(标准状况),乙能使湿润的红色石蕊试纸变蓝。
据此回答:
(1)写出R和甲的化学式:R___,甲____。
(2)另取1 LR的水溶液,向其中逐滴加入NaOH溶液,所得沉淀与加入NaOH的物质的量关系如图所示。则:
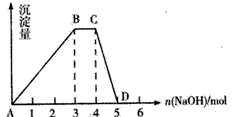
①R溶液的物质的量浓度为____。
②BC段表示的含义是____。
③CD段反应的离子方程式为____。
参考答案:(1)NH4Al(SO4)2 ; BaSO4
(2)①1 mol・L-1
②NH4+与OH -结合生成NH3・H2O
③Al(OH)3+OH-==AlO2-+2H2O
本题解析:
本题难度:一般