微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列措施对增大反应速率明显有效的是( )
A.Al在氧气中燃烧生成A12O3,将Al粉改为Al片
B.Fe与稀盐酸反应制取H2时,改用氢离子浓度相同的稀硫酸
C.Zn与稀硫酸反应时,适当提高溶液的温度
D.Na与水反应时增大水的用量
参考答案:A、将Al片改成Al粉,增大了反应物的接触面积,所以能使反应速率加快,故A正确;
B、Fe与稀盐酸反应制取H2时,改用氢离子浓度相同的稀硫酸,氢离子浓度相同,反应速率相同,故B错误;
C、Zn与稀硫酸反应时,适当提高溶液的温度,升高温度能加快化学反应的速率,故C正确;
D、钠和水反应的速率与水的多少无关,故D错误.
故选AC.
本题解析:
本题难度:简单
2、选择题 现有下列各组溶液:
①10℃时10 mL 0.1 mol・L-1的Na2S2O3溶液和50 mL0.05 mol・L-1的H2SO4溶液;
②10℃时10 mL 0.05 mol・L-1的Na2S2O3溶液和10 mL 0.1 mol・L-1的H2SO4溶液;
③30℃时10 mL 0.05 mol・L-1的Na2S2O3溶液和10 mL 0.1 mol・L-1的H2SO4溶液。
若同时将它们混合发生反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O,则出现浑浊的先后顺序是(?)
A.①②③
B.②①③
C.③②①
D.①③②
参考答案:C
本题解析:温度越高,反应速率越快,③的反应速率最大;相同温度下,②混合液中Na2S2O3和H2SO4的浓度大于①,故反应速率②>①。
本题难度:一般
3、实验题 (7分)为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验:
编号
| 操作
| 实验现象
|
①
| 分别在试管A、B中加入5 mL 5% H2O2溶液,各滴入2滴1 mol・L-1 FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡
| 试管A中无明显气泡产生;
试管B中产生的气泡量增加
|
②
| 另取两支试管分别加入5 mL 5% H2O2溶液和5 mL 10% H2O2溶液
| 试管A、B中均未明显见到有气泡产生
|
请回答下列问题:
(1)过氧化氢分解的化学方程式为? ?。
(2)实验①的目的是___________________________________________________;实验中滴加FeCl3溶液的目的是________________________________________。
(3)实验②未观察到预期的实验现象。为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是_________________________(用实验中所提供的试剂或条件)。
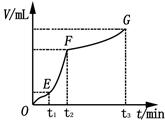
(4)某同学在50 mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如下图所示,分析判断OE、EF、FG三段中,___________段化学反应速率最快。
参考答案:(1)2H2O2  2H2O+O2↑(1分)?(2)研究温度对H2O2分解速率的影响(1分)
2H2O+O2↑(1分)?(2)研究温度对H2O2分解速率的影响(1分)
作为催化剂,加快H2O2分解速率?(1分)
(3)将两支试管同时放入盛有相同温度热水的烧杯中(或向两支试管中同时滴入2滴1mol・L-1 FeCl3溶液),观察产生气泡的速率(2分)?(4)EF(2分)
本题解析:(1)过氧化氢分解,二氧化锰在此反应中作催化剂,起催化作用,能加快过氧化氢分解产生氧气的速率,故答案为:2H2O2  2H2O+O2↑;?
2H2O+O2↑;?
(2)分别在试管A、B中加入?5mL?5%?H2O2溶液,各滴入1~2?滴1mol/L?FeCl3溶液.待试管中均有适量气泡出现,说明过氧化氢分解能发生,试管A、B中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中,两支试管不同点是试管A的温度比试管B的温度低,说明研究的是温度对反应速率的影响,而开始加滴加FeCl3溶液,目的加快H2O2分解,故答案为:研究温度对H2O2分解速率的影响;加快H2O2分解速率,使实验现象易于观察;
(3)影响化学反应速率的外界因素有浓度、温度、气体的压强、催化剂、固体的表面积,另取两支试管分别加入?5mL?5%H2O2溶液和?5mL10%H2O2溶液,试管A、B中均未见气泡产生,为加快反应速率,可从温度、或催化剂的影响角度考虑,故答案为:将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/L?FeCl3溶液,观察产生气泡的速率;
(4)该图象横坐标表示时间,纵坐标表示生成气体的体积,时间越短生成的气体越多,反应速率越快,曲线的斜率越大,所以速率最快的是EF段。
本题难度:一般
4、选择题 已知N2 (g) + 3H2(g) 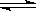 2NH3(g) (正反应放热),工业合成氨采用在500℃的条件下进行的原因是
2NH3(g) (正反应放热),工业合成氨采用在500℃的条件下进行的原因是
①只有在此温度下反应才能发生?②升高温度有利于NH3的合成
③提高反应速率,以提高单位时间内NH3的产量?④使催化剂达到最佳催化活性
A.③④
B.①②
C.①③
D.②④
参考答案:A
本题解析:应该从产率、反应速率及生产实际来综合考虑
采用高温主要是提高反应速率,以提高单位时间内NH3的产量、使催化剂达到最佳催化活性,答案为A
本题难度:一般
5、选择题 设C+CO2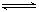 2CO △H > 0 反应速率为u1,N2+3H2
2CO △H > 0 反应速率为u1,N2+3H2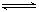 2NH3 △H<0 反应速率为u2,对于上述反应,当温度升高时,u1和u2的变化情况为
2NH3 △H<0 反应速率为u2,对于上述反应,当温度升高时,u1和u2的变化情况为
A.同时增大
B.同时减小
C.增大,减小
D.减小,增大