微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子方程式中正确的是( )
A.向NaOH溶液中通入少量CO2:OH-+CO2=HCO3-
B.小苏打治疗胃酸过多CO32-+2H+=CO2↑+H2O
C.向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-═Al(OH)3↓
D.二氧化碳通入碳酸钠溶液中:CO2+CO32-+H2O=2HCO3-
参考答案:A.向NaOH溶液中通入少量CO2的离子反应为2OH-+CO2=CO32-+H2O,故A错误;
B.小苏打治疗胃酸过多的离子反应为HCO3-+H+=CO2↑+H2O,故B错误;
C.向AlCl3溶液中加入过量的NaOH溶液的离子反应为Al3++4OH-═AlO2-+2H2O,故C错误;
D.二氧化碳通入碳酸钠溶液中的离子反应为CO2+CO32-+H2O=2HCO3-,故D正确;
故选D.
本题解析:
本题难度:简单
2、选择题 含有a mol FeBr2的溶液中,通入x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是
A.x=0.4a,2Fe2++Cl2=2Fe3++2Cl-
B.x=0.6a,2Br-+Cl2=Br2+2Cl-
C.x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl-
D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2++2Fe3++6Cl-
参考答案:B
本题解析:根据氧化还原反应的先后顺序知,Cl2先氧化Fe2+,然后再氧化Br-。x=0.4a时,Cl2不能完全氧化Fe2+,只能发生反应2Fe2++Cl2=2Fe3++2Cl-,A项正确;当x=0.6a时,Cl2能将Fe2+完全氧化后,又能氧化的Br-,故B错误;x=a时,Cl2氧化Fe2+后又能氧化a mol的Br-,C正确;x=1.5a时,Cl2能将Fe2+、Br-完全氧化,D正确。答案选择B。
本题难度:一般
3、填空题 某微粒的结构示意图为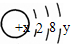 试回答:
试回答:
(1)当x-y=10时,该粒子为______(选填“原子”或“阳离子”、“阴离子”);
(2)当y=8时,该粒子可能是(用化学式表示,任填3种)______、______、______;
(3)请写出工业上制取y=7元素对应单质时的离子方程式:______.
参考答案:(1)x-y=10时,说明x=10+y,符合核电荷数=质子数=核外电子数,是原子,故答案为:原子;
(2)原子核电荷数=质子数=核外电子数,原子得失电子可能形成8电子稳定结构,稀有气体是8电子稳定结构;符合结构的原子为Ar,阳离子为K+、Ca2+,阴离子为S2-Cl-等,故答案为:S2-;Cl-;Ar;
(3)y=7元素对应单质为Cl2,依据制备氯气是用二氧化锰和浓盐酸加热反应生成;反应的离子方程式为:MnO2+4H++2Cl-△.Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-△.Mn2++Cl2↑+2H2O.
本题解析:
本题难度:一般
4、选择题 下列反应中,能用H++OH-═H2O表示的是( )
A.NaOH溶液和CO2的反应
B.Ba(OH)2溶液和稀H2SO4的反应
C.NaOH溶液和盐酸的反应
D.氨水和稀H2SO4的反应
参考答案:A、氢氧化钠和二氧化碳反应生成碳酸钠和水,不能用H++OH-=H2O表示,故A错误;
B、Ba(OH)2溶液和稀H2SO4的反应生成的硫酸钡是难溶解的物质,故B错误;
C、氢氧化钠是强碱,盐酸是强酸,生成的氯化钠是易溶于水的盐,能用H++OH-=H2O表示,故C正确;
D、氨水是弱碱,和盐酸的反应不能用H++OH-=H2O表示,故D错误.
故选C.
本题解析:
本题难度:简单
5、选择题 下列离子方程式正确的是( )
A.用铂电极电解氯化镁溶液:2Cl-+2H2O
H2↑+Cl2↑+2OH-
B.向NaHS溶液中通入少量氯气:HS-+Cl2=S↓+H++2Cl-
C.向Fe(OH)3悬浊液中加入氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
D.用醋酸除去水垢:CaCO3+2H+=Ca2++H2O+CO2↑
参考答案:A、用铂电极电解氯化镁溶液:Mg2++2Cl-+2H2O?通电?.?H2↑+Cl2↑+Mg(OH)2↓,氢氧化镁是难溶物,不能拆成离子形式,故A错误;
B、氯气具有氧化性,能将强还原性的离子HS-氧化,故B正确;
C、生成的三价铁接着和氢碘酸中的碘离子发生氧化还原反应,故C错误;
D、醋酸是弱酸,是弱电解质,弱电解质在离子反应中不能拆成离子的形式,故D错误.
故选B.
本题解析:
本题难度:一般