微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在实验室里,下列除去杂质的方法正确的是
[? ]
A.溴苯中混有溴,用汽油萃取出溴
B.乙烷中混有乙烯,通氢气在一定条件下反应,使乙烯转化为乙烷
C.硝基苯中混有浓硝酸和浓硫酸,将其倒入烧碱溶液中,静置,然后分液
D.乙烯中混有CO2 ,将其通人浓氢氧化钠溶液洗气后干燥
参考答案:CD
本题解析:
本题难度:一般
2、选择题 油脂皂化后,使肥皂和甘油充分分离,可采用的方法是(? )
A.萃取
B.蒸馏
C.结晶
D.盐析
参考答案:D
本题解析:萃取适合于溶质在不同溶剂中的溶解性不同而分离的一种方法,结晶法适用于不同溶质的溶解度受温度影响不同而分离的一种方法,蒸馏是依据混合物中个组分沸点不同而分离的一种法,适用于除去易挥发、难挥发或不挥发杂质。油脂皂化后,使肥皂和甘油充分分离,可采用的方法是渗析,答案选D。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生能力的培养和解题方法的指导与训练。该类试题需要注意的是分离提纯方法的选择思路是根据分离提纯物的性质和状态来定的。具体如下: ①分离提纯物是固体(从简单到复杂方法) :加热(灼烧、升华、热分解),溶解,过滤(洗涤沉淀),蒸发,结晶(重结晶);②分离提纯物是液体(从简单到复杂方法) :分液,萃取,蒸馏;③分离提纯物是胶体:盐析或渗析;④分离提纯物是气体:洗气。
本题难度:简单
3、选择题 下列实验操作中正确的是( )
A.分液漏斗中的液体分层后应从下口逐一流出,并用不同的容器接收
B.蒸馏时,温度计水银球应伸入液体中,冷却水应从冷凝管的下口通入,上口流出
C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D.配制稀硫酸时,先向烧杯中注入蒸馏水,再缓慢注入浓硫酸,并用玻璃棒不断搅拌
参考答案:D
本题解析:
本题难度:一般
4、实验题 (13分)某研究性学习小组欲探究Na2CO3溶液与MgCl2溶液反应产生白色沉淀的成分,小组成员做如下实验
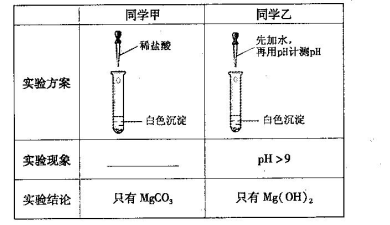
(1)若按所得的结论分析,甲观察到的实验现象是___________________________。
(2)在探究沉淀物成分前,甲、乙都将沉淀物从溶液中分离出来,洗涤并干燥。同学丙认为他们并未将沉淀洗涤干净,请用简单的实验证明丙的观点。
(3)同学丁认为甲结论不合理,理由是Ksp(MgCO3)___Ksp [Mg(OH)2](选填“<”或“>”),所以沉淀物未必是MgCO3。经查阅资料得知:该白色沉淀的组成应为Mgx(OH)y(CO3)z・nH2O。为确定沉
淀物的具体组成,他设计下图装置进行实验(所有夹持装置已省略)。
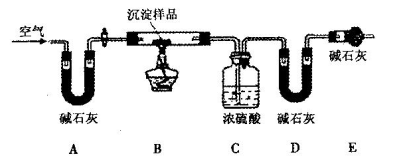
(4)请将丁设计的实验步骤补充完整:
①检查装置气密性;
②先装入药品,并称量相关装置的质量,后连接各装置;
③________________________________________________________;
④停止加热,持续通入空气直至实验结束,再次称量步骤②中相关装置的质量。
(5)装置E中碱石灰的作用是_________________________________________________。
三次实验所得数据如下:(部分数据已换算为相应的物质的量)
 ?
?
(6)分析实验数据可知,第_________组出现误差较大的数据,应舍去。由实验数据计算
得该白色沉淀物的组成为___________(选填序号)。
a.Mg2(OH)2CO3・3H2O? b.Mg(OH)2(CO3)2・3H2O
c.Mg4(OH)2(CO3)3・3H2O? d.Mg5(OH)4(CO3)3・2H2O
参考答案:(1)沉淀溶解,有气泡产生(2分)
(2)取最后一次洗涤液于另一试管中,加入硝酸酸化的硝酸银溶液,出现白色沉淀。(2分,或取最后一次洗涤液,用焰色反应检验存在的钠离子。答案合理即可得分)?(3)>(2分)
(4)先通入一会儿空气,再加热(2分)?(5)防止空气中的水蒸气和CO2进入装置D(2分)
(6)3(1分) c(2分)
本题解析:(1)碳酸镁与稀盐酸反应生成氯化镁、水和CO2,因此实验现象是沉淀溶解,有气泡产生。
(2)由于沉淀表面有吸附的氯离子,所以可以通过检验氯离子来判断沉淀是否洗涤干净,即取最后一次洗涤液于另一试管中,加入硝酸酸化的硝酸银溶液,出现白色沉淀即证明没有洗涤干净。
(3)由于氢氧化镁的溶度积常数小于碳酸镁的溶度积常数,所以Ksp(MgCO3)>Ksp [Mg(OH)2]。
(4)由于装置中有残留的空气,而空气中通过碱石灰时水蒸气和CO2被吸收,所以因此先通入一会儿空气,再加热。
(5)由于空气中还含有水蒸气和CO2会进入装置D干扰实验,所以E装置中碱石灰的作用是防止空气中的水蒸气和CO2进入装置D。
(6)由于水蒸气和CO2的物质的量与样品的质量成比例,因此根据实验1、2中的数据可知,实验3中水蒸气的物质的量偏大(应该是0.12mol),应该舍去。根据表中数据可知CO2与水蒸气的物质的量之比是3:4,则a.Mg2(OH)2CO3・3H2O中CO2与水蒸气的物质的量之比是1:4,a不正确; b.Mg(OH)2(CO3)2・3H2O中CO2与水蒸气的物质的量之比是1:2,b不正确;c.Mg4(OH)2(CO3)3・3H2O中CO2与水蒸气的物质的量之比是3:4,c正确;d.Mg5(OH)4(CO3)3・2H2O中CO2与水蒸气的物质的量之比是3:4,但3.64g该物质得不到0.03molCO2,d不正确,答案选c。
本题难度:困难
5、选择题 C和CuO在一定温度下反应,产物有Cu、Cu2O、CO、CO2。将2.00 g C跟16.0 g CuO混合,隔绝空气加热,将生成的气体全部通过足量的澄清石灰水,反应一段时间后共收集到1.12 L气体(标准状况),生成沉淀的质量为5.00 g。下列说法错误的是
A.反应后的固体混合物中还含有碳
B.反应后的固体混合物总质量为14.4 g
C.反应后的固体混合物中单质Cu的质量为12.8 g
D.反应后的固体混合物中氧化物的物质的量为0.05 mol
参考答案:C
本题解析:试题分析:A、通入石灰水就说明有0.05mol CO2,收集到气体也是0.05 mol,由此可算出C有剩余,正确;B、由题可算得反应生成的CO2,CO质量分别为2.2g,1.4g,故18-3.6=14.4g,正确;C、由上述反应式易知反应后的固体混合物中单质Cu的质量为6.4 g,错误;D、由于反应后生成CO2和CO的物质的量比为1:1,可由此得到一个综合反应式:? 2C + 4CuO =" 2Cu" + Cu2O + CO +CO2?所以混合物中氧化物的物质的量为0.05 mol,正确。
考点:本题考查了化学反应计算。
本题难度:一般