��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��֪��EΪ�����������ʣ�C��D��F��I��Ϊ�������壬����C��DΪ���ʣ�F��IΪ����������Ԫ����ͬ��D��F�ж���IΪֱ���ͷǼ��Է��ӣ����������¿�ͼ��ϵ��

��1����Ӧ�������ĵ缫��Ӧʽ?��
��2����Ӧ�۵Ļ�ѧ����ʽ?��
��3����Ӧ�ܵ����ӷ���ʽΪ?��
��4��K��һ��������ˮ�Ĺ��壬K���ȷֽ������H��ʵ����G��Һ��K��ת��ʱ���Լ�����Լ��ǣ���дѡ����ĸ��?
A��NaOH��Һ?B����ˮ ?C��Na2CO3��Һ?D��NaHCO3��Һ
��5����G�ı�����Һ���뵽��ˮ�У��������ȿɵú��ɫҺ�壬д����Ӧ�����ӷ���ʽ��??
��Һ���ֱͨ�����___? __��������ɫ������ֹ��̽���____? _��
��6����E�к��кϽ�Ԫ�أ��ᵼ��G�������ⶨG����������ͨ�����õ������ⶨ����ȡmg��ˮG��Ʒ������ϡ���ᣬ��ת�Ƶ�100mL����ƿ��������ˮ���ݣ�ȡ��10.00mL�������Թ�����KI��Һ����ַ�Ӧ���õ�����ָʾ������cmol��L-1Na2S2O3��Һ�ζ���I2+2S2O32-=2I�� +S4O62����������ȥVmL�������ʲ����뷴Ӧ�� ����Ʒ��G����������Ϊ��?����??��
����Ʒ��G����������Ϊ��?����??��
�ο��𰸣�
�����������
�����Ѷȣ�һ��
2���ƶ��� X��Y��Z��W��R��T�������ʵ��ת����ϵ����ͼ��ʾ����Ӧ���������ֲ���δ�г���

(1)���X��Y��Z���Ƕ����ڵķǽ������ʣ���X��Y����Ԫ��ͬ���壬X��Z����Ԫ��ͬ���ڡ�
����֪Y���� �ڵ��ӹ�ҵ������Ҫ���ã���Y��ԭ�ӽṹʾ��ͼΪ_____������T�ĽṹʽΪ_______��
�ڷ�Ӧ�ٵĻ�ѧ����ʽΪ______________________��
(2)��X��YΪ�������ڳ����Ľ������ʣ�ZΪһ�ֳ������ᣬX��Y�ֱ���Z��Ũ��Һ�ڼ��������²��ܷ� �����ԵĻ�ѧ��Ӧ��д����Ӧ�ܵĻ�ѧ����ʽ______________________��������X����ҺR��ַ�Ӧ��������W�н��������ӵļ��鷽��Ϊ_____________________��
�ο��𰸣�(1)��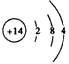 ��O=C=O����2C+SiO2
��O=C=O����2C+SiO2 2CO��+Si
2CO��+Si
(2)Cu+2H2SO4(Ũ) CuSO4+SO2��+2H2O��ȡ����W��Һ���Թ��У��μ�KSCN��Һ�����������ٵμ���ˮ����Һ��Ѫ��ɫ
CuSO4+SO2��+2H2O��ȡ����W��Һ���Թ��У��μ�KSCN��Һ�����������ٵμ���ˮ����Һ��Ѫ��ɫ
���������
�����Ѷȣ�һ��
3������� ��10�֣�A��B��C��D��E��Ϊ��ѧ��ѧ�����Ĵ����BΪ��Ȼ���к�������Һ�壬����֮�������µķ�Ӧ��ϵ��
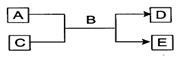
��1�������£���AΪ��̬���ʣ�CΪ�ǽ��������A��C����ʹƷ����Һ��ɫ����Է�������E>D��
��÷�Ӧ�Ļ�ѧ����ʽΪ��?��
����D�������������Լ�Ϊ��?��
��2����AΪ�����ڵĽ������ʣ�DΪ��̬���ʣ�C��Һ�����Ի�ǿ����ʱ���÷�Ӧ���ܽ��С�д��C
��Һ��ǿ����ʱ��Ӧ�����ӷ���ʽ��?��
(3)��A��C��Ϊ�����EΪ��ɫ������CΪ��������ЧӦ����Ҫ���壬д��E���ܵ����ʵĻ�ѧʽ(д����)��?��?��
�ο��𰸣���10�֣�(1)? Cl2 + SO2 + 2H2O = H2SO4 + 2 HCl(2��)
AgNO3��Һ��?ϡHNO3��ֻ��AgNO3��Һ�����֣���2�֣�
(2)? 2Al + 2 OH- + 2H2O ="2Al" O2- + 3H2����2�֣�? (3) H2SiO3? Al(OH)3?��ÿ��2�֣�
���������BΪ��Ȼ���к�������Һ�壬��B��ˮ����1�����AΪ��̬���ʣ�CΪ�ǽ��������A��C����ʹƷ����Һ��ɫ����AӦ����������C��SO2����Ӧ�ķ���ʽ��Cl2 + SO2 + 2H2O = H2SO4 + 2 HCl����Է�������E>D������E�����ᣬD���Ȼ��⡣ʵ���Ҽ��������ӵ��Լ��������ữ����������
��2��AΪ�����ڵĽ������ʣ�DΪ��̬���ʣ�C��Һ�����Ի�ǿ����ʱ���÷�Ӧ���ܽ��У�����A�ǵ���������ǿ�Ӧ�����ӷ���ʽ��2Al + 2 OH- + 2H2O ="2Al" O2- + 3H2����
��3��CΪ��������ЧӦ����Ҫ���壬��C��CO2������ΪA��C��Ϊ�����EΪ��ɫ���������Ը÷�Ӧ��̼����ȡ��̼�ỹ������ĸ��ֽⷴӦ������E�����ǹ��������������
��������ѧ�ƶ�����һ���ۺ��Խ�ǿ�����⣬��Ԫ�ؼ����������ʺ�������������������ѧ�����֪ʶ����������ѧ�Ƽ��ۺϡ��������ɿ���ѧ���Ի�ѧ֪ʶ������̶ȣ�����Ҫ��������ѧ�����ۺϷ���������˼ά���������ͼ��ķ�������ؼ�����Ѱ�ҡ�ͻ�ƿڡ�����ͻ�ƿڡ�����ץ���ء��֣�����������ɫ������״̬��������ζ�����ⷴӦ���������������Ʒ���������;�ȡ�
�����Ѷȣ�һ��
4������� ��14�֣�A��J����ѧ��ѧ�г��������ʣ�����֮���ת����ϵ���¿�ͼ��ʾ�����ֲ�������ȥ������֪A��һ�ָ��۵����ʣ�J��һ�ֺ��ɫ������

��ش��������⣺
(1)A�Ļ�ѧʽΪ?��
(2)H��I��Һ��Ϻ�����Ӧ�����ӷ���ʽ��?��
G��J�Ļ�ѧ����ʽΪ?��
(3)D����ǡ������һ������ϡ������ú��ʵĻ�ѧ�����ʾ������Һ������ԭ��?��
(4) ʵ��֤�������ᷢ��������ԭ��Ӧʱ������Խϡ��Ӧ��ԭ�����е�Ԫ�صĻ��ϼ�Խ�͡�ijͬѧȡһ������C��E�Ͻ���һ�����ĺ�ϡ�������ַ�Ӧ����Ӧ������������ų����ڷ�Ӧ���������Һ�У���μ���һ��Ũ�ȵ�����������Һ�������������Ƶ����ʵ���������ij��������ʵ�����mol���Ĺ�ϵ����ͼ��ʾ���Իش��������⣺
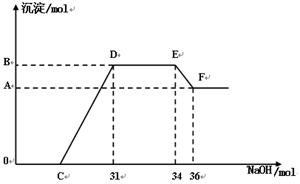
��ͼ��OC��û�г������ɣ��˽η��������ӷ���ʽΪ��_______________________________��
����DE��û�г��������ʵ���û�б仯����˽η�����Ӧ�����ӷ���ʽΪ��_________________________________��
��B���Ӧ�ij�����Ϊ________________ mol,C���Ӧ�ĺ�����Ϊ___________mol��
�ο��𰸣���1��Al2O3��2�֣�
��2��3AlO2����Al3����6H2O=4Al(OH)3��?��2�֣�4Fe(OH)2+2H2O+O2�T4Fe(OH)3?��2�֣�
��3��Fe3++3H2O  ?Fe(OH)3+3H+����д��ѧ����ʽ��2�֣�
?Fe(OH)3+3H+����д��ѧ����ʽ��2�֣�
��4����H++OH��====H2O?��2�֣�
��NH4++OH��==NH3��H2O��2�֣�?��8 ��1�֣�? 7��1�֣�
�������������������ͼ�⣬�ؼ�����ͻ�Ƶ㡣A��һ�ָ��۵����ʣ�J��һ�ֺ��ɫ����������A����������J��������������D����������C������B��������E������F���Ȼ�������G��������������H��ƫ�����ƣ�I���Ȼ�����
��1���������Ȼ�ѧʽ��Al2O3��
��2��ƫ�����ƺ��Ȼ���ˮ����ٽ�������������������Ӧ�ķ���ʽ��3AlO2����Al3����6H2O=4Al(OH)3�����������������ȶ������ױ�����������������������ʽ��4Fe(OH)2+2H2O+O2�T4Fe(OH)3 ��
��3���������������������Ȼ������Ȼ���ˮ�⣬��Һ�����ɣ�����ʽ��Fe3++3H2O  ?Fe(OH)3+3H+��
?Fe(OH)3+3H+��
��4����ͼ��OC��û�г������ɣ�˵�������ǹ����ģ����Է�Ӧ�ķ���ʽH++OH��====H2O��
����DE��û�г��������ʵ���û�б仯��˵����Һ�л�����NH4+�����Է�Ӧ�ķ���ʽ��NH4++OH��==NH3��H2O��
�۸���ͼ���֪��NH4+���ĵ�����������3mol����˷�Ӧ��ת�Ƶ��ӵ����ʵ�����24mol���ܽ������������ĵ�����������2mol�������������������ĵ�����������6mol�����Խ����������ʵ�����2mol��ʧȥ6mol���ӣ���˸��ݵ��ӵĵ�ʧ�غ��֪���������ʵ����ǣ�24mol��6mol����3��6mol������BB���Ӧ�ij�����8mol������6mol����������������������18mol������C����31mol��18mol��6mol��7mol��
�����Ѷȣ�һ��
5��ѡ���� ��ͼ��M��NΪ��XԪ�صij����������XԪ��Ϊ

A��C��Al
B��Cu��
C��N��S
D��Fe��C
�ο��𰸣�D
�����������
�����Ѷȣ�һ��