��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ������м����һ�������ᷴӦ���ڶ�����NaOH��Һ��Ӧ�������������������Ϊ1��2��������м�вμӷ�Ӧ������������Ϊ��������
A��1��1
B��1��2
C��1��3
D��2��1
�ο��𰸣����������ᡢNaOH��Һ��Ӧ���ɵ����������ʵ����ֱ�Ϊ1mol��2mol����
��2Al+6HCl=2AlCl3+3H2��
2 3
23mol 1mol
2Al+2NaOH+2H2O=2NaAlO2+3H2��
23
43mol 2mol
���һ����ڶ�����м��������Ϊ����23mol��27g/mol������43mol��27g/mol��=1��2��
��ѡB��
���������
�����Ѷȣ���
2��ѡ���� ��Һ�п��Դ��������һ�������ǣ�?��
A��Al3+�� Na+��OH-��Cl-
B��H+��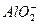 ��Na+��
��Na+��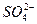
C��Mg2+��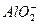 ��Al3+��
��Al3+��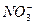
D��OH-��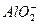 ��K+��Na+
��K+��Na+
�ο��𰸣�D
���������Al3+��OH-���ܹ��棬H+��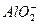 ���ܹ��棬Al3+��
���ܹ��棬Al3+��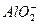 ���ܹ��档
���ܹ��档
�����Ѷȣ���
3��ѡ���� ���������Ҫ�ɷ���Al2O3��Fe2O3��SiO2�ȣ���������ұ��Al2O3���������£�

����˵����ȷ����
A������Aһ��ΪHCl
B����Һ�������ʽ���NaAlO2
C����������Ҫ�ɷ�Ϊ�����
D����Ӧ1����Ӧ2������������ԭ��Ӧ
�ο��𰸣�CD
���������A������Aһ��ΪHCl��ֻҪ����ǿ��ƫ��������ԣ�����Ƕ�����̼���壬���������µ����ʣ�����B����Һ�������ʽ���NaAlO2����ʣ����������ƣ�����C�������ƺ����ӷ�Ӧ���ɳ�������Ҫ�ɷ�Ϊ����ƣ���ȷ��D����Ӧ1����Ӧ2������������ԭ��Ӧ����ȷ��
�����Ѷȣ�һ��
4��ѡ���� �ס������ձ��и�ʢ��1L0.6mol?L-1�������NaOH��Һ�������ձ��зֱ��������������ۣ���Ӧ�����������ɵ����������ΪV���ף���V���ң�=3��4����������۵�����Ϊ��������
A��2.7g
B��3.6g
C��5.4g
D��7.2g
�ο��𰸣����������������Һ�����ʵ����ʵ�����Ϊ1L��0.6mol/L=0.6mol��
�����ձ��зֱ�������������ۣ���Ӧ�����������ɵ����������Ϊ�ף���=3��4��
�������ᷴӦʱ����ȫ��Ӧ�����ɵ����������ʵ���Ϊx��
�� 2Al+6HCl�T2AlCl3+3H2��
63
0.6mol x
��ã�x=0.3mol��
һ�������£���������ʵ���֮�ȵ������֮��Ϊ3��4��
������������Ӧ���ɵ����������ʵ���Ϊ0.4mol��
�����������Ӧʱ����ȫ��Ӧ������Ӧ���������ʵ���Ϊy��
�� 2Al+2NaOH+2H2O�T2NaAlO2+3H2��
2 3
y 0.4mol
��ã�y=0.83mol��
����������Ϊ0.83mol��27g/mol=7.2g��
��ѡD��
���������
�����Ѷȣ�һ��
5������� ����һ��Ӧ�ù㷺�Ľ�������ҵ����Al2O3�ͱ���ʯ��Na3AlF6��������ڵ���Ƶá����������Ҫ�ɷ���Al2O3��SiO2������������NaOH��Һ�����ʡ���������������Al2O3���������£�

�ش��������⣺
��1��д����Ӧ1�Ļ�ѧ����ʽ?��
��2����Һ���м���CaO���ɵij�����?����Ӧ2�����ӷ���ʽΪ?��
��3����������Ļ�ѧ����ʽ��?����ʯīΪ�缫�����������Ļ������ijɷ���?��
�ο��𰸣���1��2NaOH��SiO2=Na2SiO3��H2O��2�֣� 2NaOH��Al2O3=2NaAlO2��H2O��2�֣�
��2��CaSiO3��1�֣�?
?2AlO2��+CO2+3H2O=2Al(OH)3��+CO32��?��AlO2��+CO2+2H2O=Al(OH)3��+HCO3����2�֣�
��3��2Al2O3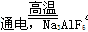 4Al��3O2����2�֣� ?O2��CO2��CO����2�֣�
4Al��3O2����2�֣� ?O2��CO2��CO����2�֣�
�����������1��������������������ﶼ������ǿ����Һ�������κ�ˮ����2���������Ǽ����������ˮ��Ӧ�����������ƣ����������������ӽ�ϳɹ���Ƴ�����ƫ��������Һͨ�����������CO2��������ȡ����������������3�������������������ȡ����������ӦʽΪ2O2����2e��=O2����������C��O2��Ӧ����CO2��CO��
�����Ѷȣ�һ��