微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 硫酸亚铁铵[(NH4)2SO4・FeSO4・6H2O]又称莫尔盐,是常用的分析试剂。实验室用FeSO4和(NH4)2SO4两种溶液混合很容易得到莫尔盐晶体。为了确定产品中Fe2+的含量,研究小组用KMnO4(酸化)溶液来滴定莫尔盐溶液中的Fe2+。滴定时必须选用的仪器有? ( )。
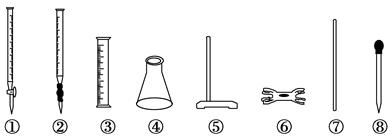
A.①④⑤⑥
B.②③⑦⑧
C.②④⑤⑥
D.④⑤⑥⑧
参考答案:A
本题解析:一般滴定实验均需要的仪器是滴定管、锥形瓶(④)、铁架台(⑤)、滴定管夹(⑥)。本实验中的KMnO4(酸化)溶液具有强氧化性,必须用酸式滴定管(①)。
本题难度:一般
2、选择题 下列实验操作与预期实验目的或所得实验结论一致的是(?)
选项
| 实验操作和现象
| 预期实验目的或结论
|
A
| 用洁净的铂丝蘸取某食盐试样,在酒精灯火焰上灼烧,火焰显黄色
| 说明该食盐不是加碘盐
|
B
| 银氨溶液中滴入少量组成为C2H4O2的液态有机物,水浴微热,有银镜出现
| 可确定该有机物一定是甲酸甲酯
|
C
| 向两支盛有KI3的溶液的试管中,分别滴加淀粉溶液和AgNO3溶液,前者溶液变蓝,后者有黄色沉淀
| KI3溶液中存在平衡:I?I2
+I-
|
D
| 室温下向CuCl2和少量FeCl3的混合溶液中,加入铜屑,充分搅拌,过滤,得蓝绿色溶液
| 除去杂质FeCl3得纯净CuCl2
溶液
|
?
参考答案:C
本题解析:A项,钾的焰色反应应透过蓝色钴玻璃片观察,显紫色,错误;B项,也可以是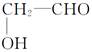 ,错误;C项I2使淀粉变蓝,I-和Ag+反应生成黄色沉淀;D项,加入铜屑发生2Fe3++Cu=2Fe2++Cu2+,不能除去生成的FeCl2。
,错误;C项I2使淀粉变蓝,I-和Ag+反应生成黄色沉淀;D项,加入铜屑发生2Fe3++Cu=2Fe2++Cu2+,不能除去生成的FeCl2。
本题难度:一般
3、选择题 有五瓶失去标签的溶液,它们分别为:①Ba(NO3)2②KCl ③NaOH ④CuSO4 ⑤Na2SO4如果不用其他任何试剂(包括试纸),用最简便的方法将它们――鉴别开来,则在下列的鉴别顺序中,最合理的是
A.④③①⑤②
B.④①③⑤②
C.①⑤③④②
D.③④①⑤②
参考答案:A
本题解析:略
本题难度:简单
4、选择题 下列实验装置和操作一般不用于分离物质的是
[? ]
A.
B.
C.
D.
参考答案:B
本题解析:
本题难度:简单
5、实验题 已知粗盐中含有CaCl2、MgCl2及一些可溶性硫酸盐,请根据你所学的知识,将除杂试剂、所除杂质以及除杂时的化学方程式按照除杂顺序填入下表:
试剂加入顺序
| 加入的试剂
| 所除杂质
| 化学方程式
|
①
| ?
| ?
| ?
|
②
| ?
| ?
| ?
|
③
| ?
| ?
| ?
|
④
| ?
| ?
| ?
参考答案:
加入的试剂
所除杂质
化学方程式
BaCl2
硫酸盐
BaCl2+Na2SO4====BaSO4↓+2NaCl
NaOH
MgCl2
MgCl2+2NaOH====Mg(OH)2↓+2NaCl
Na2CO3
CaCl2、BaCl2
BaCl2+Na2CO3====BaCO3↓+2NaCl? CaCl2+Na2CO3====CaCO3↓+2NaCl
盐酸
NaOH溶液、Na2CO3溶液
NaOH+HCl====NaCl+H2O
Na2CO3+2HCl====2NaCl+CO2↑+H2O
本题解析:为了使杂质能除得比较干净,所加试剂一般要过量,而试剂过量又出现引入新杂质的问题,为此,加入试剂的顺序要尽可能使前一过量试剂在后续除杂操作中除去。本题中,加入顺序是BaCl2、NaOH、Na2CO3、盐酸。加过量Na2CO3时可除去过量的BaCl2,最后加盐酸除去过量的NaOH、Na2CO3,当溶液达到中性微酸性时,得到几乎不含杂质的氯化钠溶液。
本题难度:简单
|