��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ijλͬѧ���ü��зϾɲ���������һ����ʹ�������������������װ�ã���ͼ�������йظõ�ع���ʱ��˵���������(����)
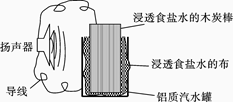
A����������ʴ
B����������Ϊ������ˮ�ޡ����ߡ������������ߡ�̿��
C��ʳ��ˮ�е�Na����̿���ƶ�
D��̿���Ϸ����ķ�ӦΪ��2H����2e��=H2��
�ο��𰸣�D
�������������������������������Ӧ��̼������������������ԭ��Ӧ�����ӴӸ��������ߡ������������ߵ����������������ƶ����������������ƶ������ѡD��
�����Ѷȣ�һ��
2������� ��10�֣�Ϊ��ʡҩƷ��ʱ�䣮�ס��ҡ�����λͬѧ��ͭƬ��пƬ��ϡ���ᡢֱ����Դ�����ߡ��ձ����Թܵ���ѧ��ѧ������ҩƷ������(��Ʒ)��������Ĺ�˼�����������ķ�ʽ������˱Ƚ�ͭ��п����������ǿ����ϵ��ʵ�顣����д���пհף�
(1)��ͬѧ��ͭƬ��пƬ����ʢ��ϡ������ձ���(ͭ��п���Ӵ�)���۲쵽����������������
(2)��ͬѧ���ż�ͬѧ��ʵ�飬�õ��߽�ͭƬ��пƬ�����������ԭ��أ���ʱ�������Ϲ۲쵽���������������������������ĵ缫��ӦʽΪ����������������
(3)��ͬѧ������ͬѧ��ʵ�飬ȥ������ͭƬ��пƬ�ĵ��ߣ���ͭƬ��пƬ�ֱ���ͬһֱ����Դ�������������ӣ������ձ��м���һ������CuSO4��Һ���е�⡣��ʱ�����ĵ缫��ӦʽΪ����������������������������Һ��pH������������(���������С�����䡱)��
(4)�ס��ҡ���3λͬѧ�ܴﵽ�Ƚ�ͭ��п�Ľ���������ǿ����Ŀ�ĵ�������������������
A��ֻ�м�ͬѧ
B������ͬѧ
C���Һͱ�ͬѧ
D���ס��Һͱ�ͬѧ
�ο��𰸣�(1)пƬ���������ݲ�����ͭƬ���ޱ仯? (2)ͭƬ�������ݲ�������Zn��2e����Zn2+
(3)Cu2++2e����Cu?����? (4)B
�����������1����ͭƬ��пƬ����ʢ��ϡ������ձ���(ͭ��п���Ӵ�)�����ܹ���ԭ��أ�пֱ�Ӻ����ᷴӦ������пƬ���������ݲ�����ͭƬ���ޱ仯��
��2����ԭ����нϻ��õĽ�����������ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ������ϣ�������Һ�е��������������ƶ������������ƶ��������õ����ӣ�������ԭ��Ӧ��п��ͭ���á�ͭ����������Һ�е������ӷŵ磬����������п�Ǹ�����ʧȥ���ӣ�����ʽΪZn��2e����Zn2+��
��3����ʱ���ɵ��أ�ͭ��������ʧȥ���ӣ�����������Ӧ��п����������Һ�е�ͭ���ӷŵ磬����ͭ������ʽΪCu2++2e����Cu ����������ͭ�ܽ⣬���Ը��ݵ��ӵ�ʧ�غ��֪����Һ��pH���䡣
��4���������Ϸ��������ѵó�ѡ��B��ȷ���������ó�������ǿ������ѡB��
�����Ѷȣ�һ��
3��ѡ���� �ݱ�����п��ؿ���ȡ��Ŀǰ�㷺ʹ�õ�Ǧ���أ���Ϊп�������������û��Ǧ��Ⱦ�����ط�ӦΪ��2Zn��O2��2ZnO��ԭ��Ϊп����̼�������Һ�Ϳ�����������������ȷ����
A��пΪ�������������븺����Ӧ
B��������ӦΪ: Zn��2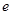 ����Zn2��
����Zn2��
C������ʱ������̼���缫�����·����п��
D����������������Ӧ
�ο��𰸣�C
�����������ԭ����нϻ��õĽ�����������ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ������ϣ�������Һ�е��������������ƶ������������ƶ��������õ����ӣ�������ԭ��Ӧ�����ݷ�Ӧʽ��֪��пʧȥ���ӣ��������������õ����ӣ�������ͨ�룬����ֻ��ѡ��C����ȷ�ģ�����Ǵ���ģ���ѡC��
�����Ѷȣ���
4��ѡ���� ���й���ͭ�缫��������ȷ����
A��ͭпԭ�����ͭ������
B���õ�ⷨ������ͭʱ�ô�ͭ������
C���ڶƼ��ϵ��ͭʱ�Ƽ���������
D�����ϡ������H2��O2ʱͭ���Դ��������
�ο��𰸣�A
���������
��ȷ�𰸣�A
B������ȷ���õ�ⷨ������ͭʱ�ô�ͭ����������ͭ��������
C������ȷ���ڶƼ��ϵ��ͭʱ�Ƽ�������?��ͭ��������?
D������ȷ�����ϡ������H2��O2ʱͭ�������Դ����������������:Cu�D2e�D=Cu2��,�ò���������
�����Ѷȣ���
5��ѡ���� �����ʺϵ�����������ӦFe3����Ag Fe2����Ag����Ƴ���ͼ��ʾ��ԭ���(����װ����֬���������Һ�����������Ƶ�0�̶Ⱦ��У����Ҿ��п̶�)����֪��ͨ��۲쵽������ָ������ƫת�������ж���ȷ����(����)
Fe2����Ag����Ƴ���ͼ��ʾ��ԭ���(����װ����֬���������Һ�����������Ƶ�0�̶Ⱦ��У����Ҿ��п̶�)����֪��ͨ��۲쵽������ָ������ƫת�������ж���ȷ����(����)

A�������·�У����Ӵ�ʯī�缫�������缫
B�������е�K���������ձ�
C��һ��ʱ�������ָ�뷴��ƫת��Խ��0�̶ȣ������ƫת
D��������ָ����к������ձ��м���һ���������ۣ�������ָ�뽫����ƫת
�ο��𰸣�D
��������������ԭ��ط�Ӧԭ����֪��ʯī�缫Ϊ������Fe3���õ��ӣ�������ԭ��Ӧ�����缫Ϊ������Agʧ���ӣ�����������Ӧ����������·�У�����Ӧ�����缫����ʯī�缫��A���������е�������Ӧ������������FeCl3��Һ���Ա�֤���������Һ�����ֵ����ԣ�B����һ��ʱ���ԭ��ط�Ӧ������������ָ�뽫ָ��0�̶ȣ�C����
�㲦�����⿼��绯ѧ���ۣ����ڿ��鿼����ʵ������ֽ⣬ͨ���������֪ʶ�����÷������ۺϵķ����������ѧ�����������
�����Ѷȣ�һ��