��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���з�Ӧ�����ӷ���ʽ��д��ȷ���ǣ�������
A�������ǻ�����������Һ�еμӹ�����̼��������Һ��[Al��OH��4]-+4H+=Al3++2H2O
B��������SO2����ͨ��������NaClO��Һ�У�SO2+2ClO-+H2O=SO32-+2HClO
C��NaHSO4��Һ��Ba��OH��2��Һ��Ӧ�����ԣ�2H++SO42-+Ba2++2OH-=BaSO4��+2H2O
D�����ˮ�еμӱ����Ȼ�����Һ��Fe3++3H2O=Fe��OH��3��+3H+
�ο��𰸣�A�������ǻ�����������Һ�еμӹ�����̼��������Һ�����ӷ�ӦΪ[Al��OH��4]-+HCO3-=Al��OH��3��+CO32-+H2O����A����
B��������SO2����ͨ��������NaClO��Һ�е����ӷ�ӦΪSO2+ClO-+H2O=SO42-+2H++Cl-����B����
C��NaHSO4��Һ��Ba��OH��2��Һ��Ӧ�����Ե����ӷ�ӦΪ2H++SO42-+Ba2++2OH-=BaSO4��+2H2O����C��ȷ��
D�����ˮ�еμӱ����Ȼ�����Һ�����ӷ�ӦΪFe3++3H2O?Fe��OH��3�����壩+3H+����D����
��ѡC��
���������
�����Ѷȣ���
2������� ��8�֣�д�����з�Ӧ�����ӷ���ʽ��
��1����ϡ������ϴ���⣨Fe2O3��?
��2��̼������Һ��������?
��3������ͭ��Һ������������Һ���?
��4������������ʯ��ˮ��ͨ�������̼?
�ο��𰸣�ÿ������ʽ2�֣���8��
��1��Fe2O3��6H�� 2Fe3����3H2O
2Fe3����3H2O
��2��CO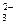 ��2H��
��2H�� H2OʮCO2��
H2OʮCO2��
��3��C u2����SO
u2����SO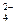 ��Ba2����2OH��
��Ba2����2OH�� BaSO4����Cu��OH��2��
BaSO4����Cu��OH��2��
��4��Ca2����2OH����CO2 CaCO3����H2O
CaCO3����H2O
�����������
�����Ѷȣ�һ��
3��ѡ���� ���л�ѧ����ʽ�����ӷ���ʽ�У���ȷ����
A����Ũ������4-��-1-�������ȷ�����ȥ��Ӧ��
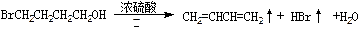
B��ˮ���ᣨ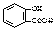 ���м���NaHCO3��Һ��
���м���NaHCO3��Һ��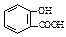 +2HCO3����
+2HCO3����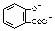 +2CO2��+2H2O
+2CO2��+2H2O
C����CuSO4��Һ�еμӹ����İ�ˮ��Cu2++2NH3��H2O��Cu(OH)2��+2NH4+
D���ú����Ƽ�Ƶ�NaHCO3 : Na++NH3+CO2+H2O =NaHCO3��+NH4+
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
4��ѡ���� ��500ml����BaCl2��KCl�Ļ����Һ�ֳ�5�ȷݣ�ȡһ�ݼ���amol��������Һ��ǡ��ʹ��������ȫ��������һ�ݼ��뺬��bmol��������Һ��ǡ��ʹ��������ȫ��������û����Һ�м�����Ũ��Ϊ��������
A��0.1��b-2a��
B��10��b-2a��
C��10��b-a��
D��10��2a-b��
�ο��𰸣�ȡһ�ݼ��뺬amol�����Ƶ���Һ��ǡ��ʹ��������ȫ��������
Ba2++SO42-�TBaSO4��
1 1
amolamol
��ȡһ�ݼ��뺬bmol����������Һ��ǡ��ʹ��������ȫ��������
Ag++Cl-�TAgCl��
11
bmolbmol
�ɻ����Һ�ֳ�5�ȷݣ���ԭ��Һ�б����ӵ�Ũ��Ϊamol��50.5L=10amol/L��
�����ӵ�Ũ��Ϊbmol��50.5L=10bmol/L��
������Һ���Ե��ԣ���ԭ�����Һ�м��������ʵ���Ũ��Ϊx��
��10amol/L��2+x��1=10bmol/L��1��
���x=10��b-2a��mol/L��
��ѡB��
���������
�����Ѷȣ���
5��ѡ���� ���з�Ӧ�����ӷ���ʽ��ȷ���ǣ�������
A����100mL0.1mol/LFeBr2��Һ��ͨ��0.025mol��Cl2����ַ�Ӧ2Fe2++4Br-+3Cl2�T2Fe3++2Br2+6Cl-
B����Fe��NO3��3��Һ�м��������HI��Һ2NO3-+8H++6I-�T3I2+2NO��+4H2O
C����̼��������Ũ���Ṳ�ȷ�Ӧ����������ͨ���������������Һ��CO2+SO2+4OH-�TSO32-+CO32-+2H2O
D��������������ʵ���Ũ�ȵ�NaHCO3��Һ��Ba��OH��2��Һ���HCO-3+Ba2++OH-�TBaCO3��+H2O
�ο��𰸣�A��FeBr2�����ʵ���Ϊ0.01mol��Cl2Ϊ0.025mol�����ݷ����ķ�Ӧ��2Fe2+Cl2�T2Fe3++2Cl-��2Br-+Cl2�T2Cl-+2Br2����֪�����������ʷ�Ӧ�����ӷ���ʽΪ��2Fe2++4Br-+3Cl2�T2Fe3++2Br2+6Cl-����A��ȷ��
B��Fe3+���Ӿ���ǿ�����ԣ��������HI��Һ��Fe3+��HI����������ԭ��Ӧ����ԭΪ����Fe2+�����ⲻ���Ϸ�Ӧʵ�ʣ���B����
C����̼��Ũ���Ṳ�ȷ�Ӧ����ʽΪ��C+2H2SO4?��?.?CO2��+2SO2��+2H2O������CO2��SO2��������ʵ���֮��Ϊ1��2����ȷ�����ӷ���ʽӦΪCO2+2SO2+6OH-=2SO2-3+CO32-+3H2O����C����
D������������ʵ���Ũ�ȵ�NaHCO3��Һ��Ba��OH��2��Һ�У�NaHCO3��Ba��OH��2���ʵ�����ȣ��漰��Ӧ�У�
HCO-3+OH-=CO32-��+H2O��CO32-+Ba2+=BaCO3�����ܷ�ӦΪ��HCO-3+Ba2++OH-=BaCO3��+H2O����D��ȷ��
��ѡAD��
���������
�����Ѷȣ���