| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《化学基本概念》高频考点预测(2017年最新版)(二)
参考答案:B 本题解析: 氧化还原反应中有元素化合价的变化,ACD中没有化合价的变化,故不属于氧化还原反应,B中锌和氢元素化合价有变化,所以B属于氧化还原反应。 本题难度:简单 4、选择题 下列各组物质相互反应时,水作氧化剂的是 |
参考答案:A
本题解析:H2O为氧化剂,则H2O中的H元素在反应后化合价应降低,应有H2生成。①Na和H2O反应生成NaOH和H2,反应中H元素化合价降低,水为氧化剂,正确;②Na2O+H2O=2NaOH,不是氧化还原反应,错误;③3Fe+4H2O(g) Fe3O4+4H2反应中H元素化合价降低,水为氧化剂,正确;④Na2O2和H2O反应生成NaOH和O2,反应中H和O的元素化合价没有发生变化,水既不是氧化剂也不是还原剂,错误。
Fe3O4+4H2反应中H元素化合价降低,水为氧化剂,正确;④Na2O2和H2O反应生成NaOH和O2,反应中H和O的元素化合价没有发生变化,水既不是氧化剂也不是还原剂,错误。
考点:考查氧化还原反应。
本题难度:一般
5、填空题 (8分)(1)(3分)下列各组物质中: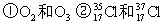 ③H2O和 D2O ④ CH3CH3和CH3CH2CH2CH3 ⑤ CH3-CH2-OH和CH3-O-CH3
③H2O和 D2O ④ CH3CH3和CH3CH2CH2CH3 ⑤ CH3-CH2-OH和CH3-O-CH3
互为同位素的是;____ __; 互为同素异形体是:____ __;
互为同分异构体是:___ ___。
(2)(5分)利用氧化还原反应原理配平以下化学方程式,并填空:
FeSO4 + KNO3 + H2SO4 === K2SO4 + Fe2(SO4)3 + NO↑+ H2O
①氧化产物为
②当电子转移了0.3mol时,有 g氧化剂参加反应
参考答案:(1)②;①;⑤(各1分)
(2)6 FeSO4 + 2KNO3 + 4H2SO4 === 1K2SO4 + 3Fe2(SO4)3 + 2NO↑+ 4H2O(2分)
①Fe2(SO4)3(1分) ②10.1(2分)
本题解析:(1)同位素的定义:质子数相同而中子数不同的同一元素的不同核素,即同位素的研究对象是原子;
同素异形体的定义:同种元素形成的性质不同的单质,即同素异形体的研究对象是单质;
同分异构体的定义:分子式相同而结构不同的化合物,即同分异构体的研究对象是化合物;
(2)利用化合价升降相等:Fe由+2价升高到+3价,N由+5价降低到+2价,
则(3-2)×6=(5-2)×2,即FeSO4系数为6,Fe2(SO4)3系数为3,KNO3、NO系数均为2;再利用K原子守恒,得K2SO4系数为1;再利用S原子守恒,得H2SO4系数为4;再利用H原子守恒,得H2O系数为4;最后,可利用O原子守恒检查配平是否正确;
①Fe元素由+2价升高到+3价,被氧化,得氧化产物Fe2(SO4)3;
②N元素由+5价降低到+2价,被还原,做KNO3氧化剂,在方程式中转移了6个电子,
即:2 KNO3 ― 6e-
2 6
n(KNO3) 0.3mol,得:n(KNO3)="0.1" mol,则m(KNO3)=" 0.1" mol×101g.mol-1=10.1g
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《磷及其化合.. | |