微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 能在溶液中大量共存的一组离子是
A.Cu2+、SO42-、OH-、K
B.Na、CO32-、H+、Cl-
C.H+、Cl-、NO3-、Ba2+
D.Ca2+、H+、CO32-、NO3-
参考答案:C
本题解析:分析:根据离子之间不能结合生成水、气体、沉淀等,则离子能大量共存,以此来解答.
解答:A.因Cu2+、OH-结合生成沉淀,则不能共存,故A错误;
B.因H+、CO32-、结合生成水和气体,则不能共存,故B错误;
C.因该组离子之间不反应,能共存,故C正确;
D.因H+、CO32-结合生成水和气体,Ca2+、CO32-结合生成沉淀,则不能共存,故D错误;
故选C.
点评:本题考查离子的共存,较简单,熟悉复分解反应发生的条件及常见物质的溶解性即可解答.
本题难度:一般
2、选择题 在100mL某混合溶液中,c(HNO3)=0.4mol?L-1,c(H2SO4)=0.1mol?L-1,现向混合液中加入1.92g铜粉,微热,充分反应后溶液中Cu2+的物质的量浓度约为(假设反应前后溶液的体积保持不变)
A.0.15?mol/L
B.0.225?mol/L
C.0.3?mol/L
D.0.6?mol/L
参考答案:B
本题解析:分析:根据n=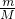 计算1.92g铜物质的量,根据n=cV计算n(H+)、n(NO3-),铜屑投入HNO3和H2SO4的混合溶液中发生的反应:3Cu+8H++2NO3-=3Cu2++2NO+4H2O,结合铜、硝酸根、氢离子的物质的量根据离子方程式进行过量计算,再根据不足的物质计算铜离子的物质的量,结合c=
计算1.92g铜物质的量,根据n=cV计算n(H+)、n(NO3-),铜屑投入HNO3和H2SO4的混合溶液中发生的反应:3Cu+8H++2NO3-=3Cu2++2NO+4H2O,结合铜、硝酸根、氢离子的物质的量根据离子方程式进行过量计算,再根据不足的物质计算铜离子的物质的量,结合c=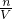 计算铜离子浓度.
计算铜离子浓度.
解答:n(HNO3)=0.1L×0.4mol/L=0.04mol,n(H2SO4)=0.1L×0.1moL/L=0.01moL,
n(NO3-)=n(HNO3)=0.04mol,
溶液中的氢离子既包括硝酸电离的又包括硫酸电离的:所以n(H+)=0.04moL+2×0.01moL=0.06mol,
n(Cu)= =0.03mol,
=0.03mol,
? 3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O
? 3mol?2mol?8mol
0.03mol 0.02mol 0.08mol
由反应关系可以看出,NO3-过量,H+不足,根据H+计算生成的铜离子,则生成的n(Cu2+)=0.06mol×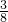 =0.0225mol,
=0.0225mol,
c(Cu2+)=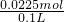 =0.225mol/L,
=0.225mol/L,
故选B.
点评:本题考查物质的量浓度的计算,题目难度不大,解答该题的关键是把握反应的离子方程式,根据离子方程式判断反应的过量问题.
本题难度:困难
3、选择题 由CO和H2组成的混合气体2.8g?在足量的O2?中充分燃烧后,立即通入足量的Na2O2?固体中,固体的质量增加
A.2.8g
B.3.6g
C.4.4g
D.5.6g
参考答案:A
本题解析:分析:利用差量法,根据化学方程式分析:CO与H2在氧气中完全燃烧,生成CO2和H2O,生成的CO2和H2O再与Na2O2反应.
2CO+O2? 2CO2,一氧化碳与二氧化碳物质的量相等,Na2O2与CO2反应:2CO2+2Na2O2=2Na2CO3+O2,质量增重△m=2Na2CO3-2Na2O2=2CO,可知反应后固体质量增加量为CO的质量;
2CO2,一氧化碳与二氧化碳物质的量相等,Na2O2与CO2反应:2CO2+2Na2O2=2Na2CO3+O2,质量增重△m=2Na2CO3-2Na2O2=2CO,可知反应后固体质量增加量为CO的质量;
2H2+O2 2H2O,生成的水与氢气物质的量相等,Na2O2与H2O反应2:H2O+2Na2O2=4NaOH+O2,质量增重△m=2H2O-O2=2H2,可知反应后固体增加的质量为氢气质量.
2H2O,生成的水与氢气物质的量相等,Na2O2与H2O反应2:H2O+2Na2O2=4NaOH+O2,质量增重△m=2H2O-O2=2H2,可知反应后固体增加的质量为氢气质量.
解答:CO与H2在氧气中完全燃烧,生成CO2和H2O,生成的CO2和H2O再与Na2O2反应.
2CO+O2? 2CO2,一氧化碳与二氧化碳物质的量相等,Na2O2与CO2反应:2CO2+2Na2O2=2Na2CO3+O2,质量增重△m=2Na2CO3-2Na2O2=2CO,可知反应后固体质量增加量为CO的质量;
2CO2,一氧化碳与二氧化碳物质的量相等,Na2O2与CO2反应:2CO2+2Na2O2=2Na2CO3+O2,质量增重△m=2Na2CO3-2Na2O2=2CO,可知反应后固体质量增加量为CO的质量;
2H2+O2 2H2O,生成的水与氢气物质的量相等,Na2O2与H2O反应2:H2O+2Na2O2=4NaOH+O2,质量增重△m=2H2O-O2=2H2,可知反应后固体增加的质量为氢气质量,
2H2O,生成的水与氢气物质的量相等,Na2O2与H2O反应2:H2O+2Na2O2=4NaOH+O2,质量增重△m=2H2O-O2=2H2,可知反应后固体增加的质量为氢气质量,
故过氧化钠固体增重等于CO和H2的质量之和为2.8g,
故选A.
点评:本题考查混合物的计算,难度中等,注意从CO2、H2O与Na2O2生成固体质量的变化分析规律,是解答该题的关键.
本题难度:一般
4、选择题 下列叙述不正确的是
A.CH4与C4H10互为同系物
B.C5H12有三种同分异构体
C.甲烷与氯气在三溴化铁催化下发生取代反应
D.苯分子中的碳碳键是介于单键和双键之间的独特的键
参考答案:C
本题解析:甲烷和氯气的取代反应,需要光照,选项C不正确,其余都是正确的,答案选C。
本题难度:简单
5、选择题 除去SO2中混有的SO3气体,不能选用的试剂是
A.98.3% H2SO4
B.BaCl2溶液
C.饱和NaHSO3溶液
D.饱和NaHCO3溶液
参考答案:D
本题解析:分析:根据除杂原则,选择除杂剂最少要满足两个条件:①加入的试剂只能与杂质反应,或吸收杂质,不能吸收被提纯物质,不能与被提纯物质反应;②反应时不能引入新的杂质.注意生成被提纯的物质最好,结合选项中各物质的性质判断.
解答:A、98.3% H2SO4可以吸收SO3气体,不影响SO2气体,故A正确;
B、BaCl2溶液与SO2气体不反应,与SO3气体反应生成硫酸钡沉淀,除去SO3气体,故B正确;
C、饱和NaHSO3溶液与SO3、水反应,除去SO3气体,同时生成SO2气体,故C正确;
D、亚硫酸是中强酸,比碳酸酸性强,饱和NaHCO3溶液与SO2、水反应,SO2气体被吸收,故D错误.
故选:D.
点评:本题考查了二氧化硫和三氧化硫的性质应用,主要考查气体除杂的原则不增不减,简单易分离复原,最好.
本题难度:简单