微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 多少克KCl溶解于1.8L水中,才能使100个水分子中含有1个K+
A.7.45g
B.37.5g
C.39g
D.74.5g
参考答案:D
本题解析:1.8L水的质量是1800g,物质的量是1800g÷18g/mol=100g。由于100个水分子中含有1个K+,所以钾离子的物质的量是1mol,则氯化钾的物质的量也是1mol,因此氯化钾的质量是74.5g,答案选D。
本题难度:困难
2、填空题 (4分)黑火药爆炸时发生如下的反应:2KNO3 + 3C + S = K2S + N2↑+ 3CO2↑ 该反应的氧 化剂是______ 、还原剂 。
化剂是______ 、还原剂 。
参考答案: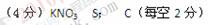
本题解析:略
本题难度:一般
3、选择题 分析下表中的四个热化学方程式,判断氢气和丙烷的燃烧热分别是
A.571.6 kJ・mol-1,2221.5kJ・mol-1
B.241.3 kJ・mol-1,2013.8 kJ・mol-1
C.285.8 kJ・mol-1,2013.8 kJ・mol-1
D.285.8 kJ・mol-1,2221.5 kJ・mol-1
参考答案:D
本题解析:燃烧热是指在常温常压下,1mol纯物质完全燃烧生成稳定的氧化物时所放出的能量叫做该物质的燃烧热,所以,氢气和丙烷的燃烧热分别为285.8 kJ・mol-1,2221.5 kJ・mol-1;正确选项为D;
本题难度:困难
4、填空题 已知铜能被稀硝酸溶解,其反应的化学方程式如下
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
(1)用双线桥法分析上述反应的电子转移情况(只需标出电子得失的方向和数目)__________________________________________________________________。
(2)上述反应中氧化剂是 ,氧化产物是 。
(3)上述反应中氧化剂与还原剂的物质的量之比为 。
(4)若反应中转移了0.6 mol电子,产生的气体在标准状况下的体积是 。
参考答案:(1)
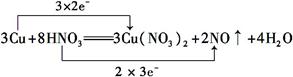
(2)HNO3 Cu(NO3)2
(3)2∶3
(4)4.48 L
本题解析:(1)在反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O中,Cu元素的化合价由0升高到+2价,N元素的化合价由+5降低为+2价,转移的电子为6e-,
则双线桥法标出电子得失的方向和数目为 ,
,
故答案为: ;
;
(2)N元素的化合价降低,Cu元素的化合价升高,则硝酸为氧化剂,硝酸铜为氧化产物;(3)生成硝酸盐体现硝酸的酸性,生成NO体现硝酸的氧化性,由反应及氮原子守恒可知,8mol硝酸反应时6mol硝酸体现酸性,2mol硝酸体现氧化性,3mol铜体现了还原性,故氧化剂与还原剂的物质的量之比为2:3;(4)由反应可知生成2molNO转移的电子为6mol,则反应中转移了0.6mol电子,产生的气体的物质的量为0.2mol,其在标准状况下的体积为0.2mol×22.4L/mol=4.48L。
考点:氧化还原反应;硝酸的化学性质。
本题难度:一般
5、选择题 丙烷在光照的条件下与氯气混和,生成的二氯代物有几种
A.2种
B.3种
C.4种
D.5种
参考答案:C
本题解析:
本题难度:困难