| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《物质结构和元素周期律》高频试题预测(2017年最新版)(四)
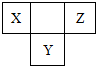 参考答案:短周期元素M、X、Y、Z,由元素X、Y、Z在周期表中所处的位置关系可知,X、Z处于第二周期,Y处于第三周期,X、Y、Z三种元素原子的质子数之和为32,令X的原子序数为x,则Y的原子序数为x+9,Z的原子序数为x+2,则:x+x+9+x+2=32,解得x=7,故X为氮元素、Y为硫元素、Z为氟元素;M元素原子的最外层电子数为次外层电子数的2倍,则M元素原子有2个电子层,最外层电子数为4,故M为碳元素, 本题解析: 本题难度:简单 2、选择题 砹(At)是卤族元素中位于碘后面的元素,推测砹和砹的化合物最不可能具备的性质( ) 参考答案:A.砹单质属于非极性分子,易溶于非极性的有机溶剂,故A正确; 本题解析: 本题难度:一般 3、推断题 有A、B、C、D四种元素,它们的原子序数依次增大,但均小于18,A和B在同一周期,A的电子式为 参考答案:(1)碳;氧;镁;铝 本题解析: 本题难度:一般 4、选择题 下列四种离子中结合质子(H+)的倾向最强的是: 参考答案:B 本题解析: 本题难度:困难 5、选择题 在元素周期表的金属和非金属的分界线的附近可以找到 参考答案:A 本题解析: 本题难度:简单 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《铁的氧化物》高频.. | |