| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《化学反应进行的方向》在线测试(2017年最新版)(二)
参考答案:B 本题解析:A、根据?H―T?S,若反应为熵减小的反应,温度较高时,可能不能自发进行,故A错误;B、应用盖斯定律,根据容易测量焓变的反应,可计算某些难以直接测量的反应焓变,故B正确;C、根据?H―T?S,若反应△H>0,温度较低时,可能不能自发进行,故C错误;D、根据?H―T?S,△H>0,△S<0的化学反应一定不能自发进行,故D错误。 本题难度:一般 2、选择题 下列有关说法正确的是 |
参考答案:BD
本题解析:A.钢铁的腐蚀过程中,若是强酸性环境,则发生析氢腐蚀,若是弱酸性环境,就既发生吸氧腐蚀,也发生吸氧腐蚀,可以同时发生,错误;B.反应NH4Cl(s)=NH3(g)+HCl(g)的正反应是体系混乱增大的反应,在室温下不能自发进行,ΔG=ΔH-TΔS>0,则该反应的ΔH>0,正确;C.由于Ksp(BaSO4)<Ksp(BaCO3),向含有BaSO4沉淀的溶液中加入Na2CO3,若c(Ba2+)?c(CO32-)>Ksp(BaCO3),则BaSO4沉淀就能转化为BaCO3 沉淀,错误;D.在CH3COOH溶液中存在电离平衡:CH3COOH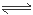 CH3COO-+H+;同时也存在水的电离平衡。当向25℃时,0.1 mol・L-1CH3COOH溶液加水稀释时,溶液中的c(H+)、c(CH3COO-)、c(CH3COOH)的浓度都减小,由于稀释对电离产生的离子浓度影响大,所以醋酸的电离平衡正向移动,c(H+)减小的倍数小于c(CH3COOH),在温度不变时,水的离子乘积是个常数,c(H+)减小,则c(OH-)增大,所以c(OH-)/c(CH3COOH)增大,正确。
CH3COO-+H+;同时也存在水的电离平衡。当向25℃时,0.1 mol・L-1CH3COOH溶液加水稀释时,溶液中的c(H+)、c(CH3COO-)、c(CH3COOH)的浓度都减小,由于稀释对电离产生的离子浓度影响大,所以醋酸的电离平衡正向移动,c(H+)减小的倍数小于c(CH3COOH),在温度不变时,水的离子乘积是个常数,c(H+)减小,则c(OH-)增大,所以c(OH-)/c(CH3COOH)增大,正确。
考点:考查计算腐蚀的存在、反应自发性的判断、溶度积常数的应用、稀释对弱电解质电离平衡移动的影响的知识。
本题难度:一般
3、选择题 下列说法正确的是( )
A.△H>0、△S>0的反应在任何温度下都不能自发进行
B.在滴有酚酞的Na2CO3溶液中,加入BaC12溶液后红色褪去
C.测氯水的pH,可用干燥洁净的玻璃棒蘸取氯水点在pH试纸上,待其变色后和标准比色卡比较
D.使用催化剂可以改变化学反应的反应热
参考答案:B
本题解析:
本题难度:一般
4、选择题 有如下反应:
①2H2O2(aq)====2H2O(l)+O2(g)
②NH3(g)+HCl(g)====NH4Cl(s)
③N2(g)+3H2(g)====2NH3(g)
④N2O4(g)====2NO2(g)
⑤CH3COOH(l)====CH3COOH(s)
其中属熵增加过程的是
[? ]
A.①⑤
B.②③⑤
C.③④
D.①④
参考答案:D
本题解析:
本题难度:简单
5、选择题 下列关于化学反应的熵变的叙述中,正确的是
A.化学反应的熵变与反应的方向无关
B.化学反应的熵变直接决定了反应的方向
C.熵变为正的反应都是混乱度增大的反应
D.能自发进行的反应熵变一定都为正
参考答案:C
本题解析:A、△G=△H-T・△S,由此可知,化学反应的熵变与反应的方向有关,错误; B、反应的方向是由焓变和熵变两个量来确定的,错误;C、正确;D、能自发进行的反应自由能一定小于零,但熵不一定都为正,像零下十度时,水结成冰是一个自发反应,但是一个熵减小的反应,错误。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《电解池的应.. | |