微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (10分)某研究性学习小组为了研究影响化学反应速率的因素,设计如下方案:
实验编号
| 0.01mol・L-1
酸性KMnO4溶液
| 0.1mol・L-1
H2C2O4溶液
| 水
| 1mol・L-1
MnSO4溶液
| 反应温度
/℃
| 反应时间
|
I
| 2mL
| 2mL
| 0
| 0
| 20
| 125
|
II
| ____mL
| ____mL
| 1mL
| 0
| 20
| 320
|
III
| ____mL
| ___mL
| ___mL
| 0
| 50
| 30
|
IV
| 2mL
| 2mL
| 0
| 2滴
| 20
| 10
|
已知:反应的方程式(未配平):KMnO4 + H2C2O4 + H2SO4 ―― K2SO4 + MnSO4 + CO2↑+ H2O
(1)实验记时方法是从溶液混合开始记时,至___ ___ __时记时结束。
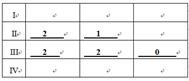
(2)实验I和II研究浓度对反应速率的影响,实验I和III研究温度对反应速率的影响。请在上表空格中填入合理的实验数据。
(3)从实验数据分析,实验I和IV研究________对反应的影响。
(4)请配平上面的化学方程式:
KMnO4 + H2C2O4 + H2SO4= K2SO4 + MnSO4 + CO2↑+ H2O
参考答案:(1)溶液紫红色刚好褪色
(2)
(3)催化剂 (4)2 5 3 1 2 10 8
本题解析:(1)高锰酸钾溶液呈紫色,反应使高锰酸钾褪色;(2)实验I和II研究浓度对反应速率的影响,,溶液的总体积相同,所以实验II 加2mL0.01mol・L-1酸性KMnO4溶液、1mL0.1mol・L-1H2C2O4溶液;实验I和III研究温度对反应速率的影响,投料应该相同,所以实验III 加2mL0.01mol・L-1酸性KMnO4溶液、2mL0.1mol・L-1H2C2O4溶液,0 mL水;(3)实验IV比实验I多加了两滴MnSO4,研究催化剂对反应的影响;(4)根据化合价升降相同,所以化学方程式为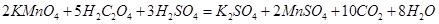 。
。
考点:本题考查影响化学反应速率的因素。
本题难度:一般
2、选择题 将Mg条投入盛有稀HCl的容器里,产生H2的速率与下列因素:①盐酸浓度②温度③镁条的表面积④容器的密闭情况⑤溶液中c(Cl-)大小,有关系的是(?)。
A.①②
B.③④
C.①②③④
D.①②③④⑤
参考答案:C
本题解析:影响镁和盐酸反应的反应速率大小因素有温度、氢离子的浓度、镁条的表面积。反应中有氢气生成,则和容器中的压强也有关系,但与氯离子的浓度没有关系,答案选C。
点评:该题是常识性知识的考查,试题紧扣教材,旨在培养学生灵活运用基础知识解决实际问题的能力。该题的关键是明确外界条件是如何影响反应速率的,并能结合题意和反应式灵活运用即可,有利于调动学生的学习兴趣和学习积极性。
本题难度:一般
3、选择题 反应CO(g) +H2O(g)  H2(g) +CO2(g) ΔH<0,改变其中一种条件,能加快反应速率且反应放出的热量不变的是
H2(g) +CO2(g) ΔH<0,改变其中一种条件,能加快反应速率且反应放出的热量不变的是
A.升高温度
B.减小压强
C.加入CO
D.加入催化剂
参考答案:D
本题解析:A、正方应是放热反应,升高温度反应速率增大,平衡向逆反应方向移动,放出的热量减少,A不正确;B、正方应是体积不变的,减小压强平衡不移动,但反应速率降低,B不正确;C、加入CO反应速率增大,平衡向正反应方向移动,放出的热量增加,C不正确;D、加入催化剂平衡不移动,反应速率增大,D正确,答案选D。
本题难度:一般
4、选择题 决定化学反应速率的主要因素是
[? ]
A.参加反应的物质本身的性质
B.催化剂
C.温度、压强以及反应物的接触面
D.反应物的浓度
参考答案:A
本题解析:
本题难度:一般
5、实验题 某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
(一)制取氧化铜
①称取2 gCuSO4・5H2O研细后倒入烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是_______________(填实验序号),步骤②中加热所用仪器的名称是___________________;
(2)步骤③中洗涤沉淀的操作是___________________________________。
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较
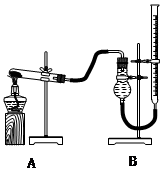
用下图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
实验序号
| KClO3质量
| 其它物质质量
| 待测数据
|
④
| 1.2 g
| 无其他物质
| ?
|
⑤
| 1.2 g
| CuO? 0.5 g
| ?
|
⑥
| 1.2 g
| MnO2? 0.5 g
| ?
|
回答下列问题:
(3)上述实验中的“待测数”据指_____________;
(4)本实验装置图中量气装置B由干燥管、乳胶管和50 mL滴定管改造后组装而成,此处所用滴定管是___________(填“酸式”或“碱式”)滴定管;
(5)若要读取实验⑤中干燥管内收集的气体体积,应注意 ____________________
__________________________________ __________________;
⑹为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a._______________________________,
b.CuO的化学性质有没有改变
参考答案:(1)①②③?蒸发皿?(2)沿玻璃棒向过滤器中的沉淀上加蒸馏水?至淹没沉淀,静置使其全部滤出,重复2~3次?(3)时间?(4)碱式?(5)待装置内的气体冷却至室温后,上下移动滴定管,使两边的液面相平,视线要与凹液面相切。?⑹CuO的质量有没有改变
本题解析:(1)在①溶解物质用玻璃棒搅拌 。②给物质加热用玻璃棒搅拌是水分快速蒸发。③过滤用玻璃棒引流。步骤②中用蒸发皿加热。(2)洗涤沉淀的操作沿玻璃棒向过滤器中的沉淀上加蒸馏水至淹没沉淀,静置使其全部滤出,重复2~3次 (3)上述实验中的“待测数”据指生成25 mL气体所需要的时间。(4)酸式滴定管下边有活塞,容易漏液体,所以要用碱式滴定管。(5)为减小实验误差,提高实验的准确度,读取气体体积时应注意待装置内的气体冷却至室温后,上下移动滴定管,使两边的液面相平,视线要与凹液面相切。 催化剂是能改变其它物质的化学反应速率,而本身的质量和化学性质不发生改变的物质。所以还需测CuO的质量有没有改变。
本题难度:困难