|
�߿���ѧ�ؿ�֪ʶ�㡶���ʵ�������Ƶ������ѵ��2017����ϰ�棩(��)
2017-07-18 01:05:54
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��NA���������ӵ�����������˵����ȷ����( )
A��9 g������������Ϊ0.5��6.02��1023
B����⾫��ͭʱ��ÿת��l mol���ӣ��������ܽ�Ľ�����Ϊ32g
C��������V2O5���ܱ������м���2molSO2��lmolO2����ַ�Ӧ�������������2NA
D��V L a mol��L
|
�ο��𰸣�
���������
�����Ѷȣ�һ��
2��ѡ���� �����£���20�����������ͨ��a mol H2S��b mol SO2��a��b��Ϊ����������a��5,b��5��,��Ӧ��ɺ�������������ܴﵽ������ܶ���
?[? ]
A��24.5g/L
B��14.4g/L
C��8g/L
D��5.1g/L
�ο��𰸣�B
���������
�����Ѷȣ�һ��
3��ѡ���� ������Һ���й����ʵ���Ũ�ȹ�ϵ��ȷ���ǣ�������
A��pH��ȵ�CH3COONa��NaOH��Na2CO3������Һ��[NaOH]��[CH3COONa]��[Na2CO3]
B��Na2CO3��Һ��[Na+]��[CO32-]֮��Ϊ2��1
C��[NH4+]��ȵ�NH4Cl��NH4HCO3��NH4HSO4������Һ��[NH4HSO4]��[NH4Cl]��[NH4HCO3]
D����֭������ѪҺ��������Һ��θҺ��[H+]���ν���
�ο��𰸣�A��ǿ�������Σ���Ӧ�������Խ����ˮ��̶�Խ����Һ�����ʵ����ʵ���ԽС�����Դ�С��ϵΪ�����̼�ᣬ����̼����ˮ��̶ȴ�pH��ͬʱ�������Ƶ�Ũ�ȴ���̼���Ƶ�Ũ�ȣ���������Ϊǿ�Ũ����С������pH��ͬ������Ũ�ȹ�ϵΪ��[NaOH]��[Na2CO3]��[CH3COONa]����A����
B��̼������Һ�У�����̼������ӷ�����ˮ�⣬���ʵ�����С������[Na+]��[CO32-]֮�ȴ���2��1����B����
C���Ȼ���������������Ρ�̼������������������Σ�����˫ˮ�⣬ˮ��̶�����̼�������Һ��ʾ���ԣ���Һ�е������������������ˮ�⣬������Һ�������Ũ����ȣ�������ҺŨ�����㣺��[NH4HSO4]��[NH4Cl]��[NH4HCO3]����C��ȷ��
D��ѪҺ��7.35��7.45��θҺ��0.9��1.5����֭��ʾ�����ԣ�pH��3.5���ҡ����dz����ԣ�����������Ũ��Ϊ��θҺ����֭�����ǣ�ѪҺ����D����
��ѡC��
���������
�����Ѷȣ���
4��ѡ���� ���ܱ���������H2��O2��Cl2�Ļ�����塣���ȼ�������е���������ǡ����ȫ��Ӧ����ȴ�����º�õ�Һ��������������������33.6%����������ԭH2��O2��Cl2���������()
A��2��1��1
B��9��4��1
C��4��2��2
D��9��4��3
�ο��𰸣�B
���������������Ҫ����Cl2�ͷǽ����ķ�Ӧ�����ʵ����������ļ��㷽����
�ⷨһ�����淽����
��ԭ��������зֱ�O2�����x��Cl2�����y�������⣬��������HCl�����������ɵ�ˮ�еõ����ᡣ�ɰ����ӵ����ɣ�V1��V2=n1��n2��
2H2��O2 2H2O 2H2O
(2x)?x? (2x)
H2+Cl2 2HCl 2HCl
(y)?y? (2y)
33.6%=2y�� ��100%�� ��100%��
���x��y=4��1����V��H2����2x+y��
��V��H2����V��O2����V��Cl2)=9��4��1��
ѡB��
�ⷨ������DZ����
ͨ����Ӧ����ʽ2H2��O2 2H2O��H2��Cl2 2H2O��H2��Cl2 2HCl����ϸ�۲������������ʵ�������ھ��DZ�ڹ�ϵ��H2�������ʵ�������O2�����ʵ�������������Cl2�����ʵ������� 2HCl����ϸ�۲������������ʵ�������ھ��DZ�ڹ�ϵ��H2�������ʵ�������O2�����ʵ�������������Cl2�����ʵ�������
V��H2����2V��O2����V��Cl2)������ѡ�ֻ��B����ǡ����ȫ��Ӧ��9��2��4+1��
�����Ѷȣ���
5��ѡ���� ����ʱ�����������Ļ����Һ20mL������������μ���0.05mol/L Ba(OH)2��Һʱ�����ɵ�BaSO4��pH�ı仯��ͼ��ʾ����������Һ���ʱ����ı仯��������˵����ȷ����

A��ͼ��A����Һ��pH=1
B�����ɳ������������Ϊ2.33g
C��ԭ�����Һ���������ʵ���Ũ��Ϊ0.1mol/L
D����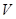 [Ba(OH)2(aq)]=10mLʱ��������Ӧ�����ӷ���ʽΪ��Ba2++SO [Ba(OH)2(aq)]=10mLʱ��������Ӧ�����ӷ���ʽΪ��Ba2++SO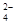 �TBaSO4�� �TBaSO4��
�ο��𰸣�A
�����������ͼ��֪��0��20mLBa(OH)2��Һ����H2SO4+Ba(OH)2�TBaSO4��+2H2O�����������ӷ���ʽ��2H����SO42��+Ba2����2OH���TBaSO4��+2H2O��D����20mL��60mLBa(OH)2��Һ��������H��+OH���TH2O����ͼ��֪������20mLBa(OH)2��Һʱ�����ᱵ���������ֵ������������ʵ���Ϊx����
H2SO4?+? Ba(OH)2?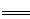 ?BaSO4��? +? H2O ?BaSO4��? +? H2O
1?1? 233g
x?0.02L��0.05mol��L��1? y
��x=0.02L��0.05mol��L��1=0.001mol��y��0.233g��
��������ʵ���Ũ��Ϊ ?=0.05mol��L��1���������ᱵ�������������Ϊ0.233g��B���� ?=0.05mol��L��1���������ᱵ�������������Ϊ0.233g��B����
��ͼ��֪��PH=7ʱ������60mLBa(OH)2��Һ����H��+OH���TH2O��֪ԭ��Һ�к��е�n��H����=n��OH����=0.06L��0.05mol��L��1=0.003mol����n��HCl��=0.003mol��2��0.001mol��2=0.004mol��
��ԭ��Һ��HCl�����ʵ���Ũ��= ?=0.2mol��L��1��C���� ?=0.2mol��L��1��C����
��ͼ��֪��A��������ȫ��Ӧ�������ӵ�Ũ��Ϊ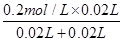 =0.1mol��L��1����pH=-lg0.1=1��A�ԣ� =0.1mol��L��1����pH=-lg0.1=1��A�ԣ�
��������������ѡA��
�����Ѷȣ���
|