微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 环保部门测定某气体样品中一氧化碳的含量,其方法和实验步骤如下:
(1)将2.000 L的气体样品通过盛有I2O5固体的加热管,发生的反应为:5CO+I2O5 5CO2+I2。
5CO2+I2。
(2)将所产生的碘升华,并加入30.00 mL 0.005 0 mol・L-1的硫代硫酸钠溶液,发生的反应为:I2+2 ====2I-+
====2I-+ 。
。
(3)将(2)中溶液取出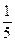 ,加入1.00 mL 0.010 0 mol・L-1的碘水,正好将所取溶液中过量的Na2S2O3全部氧化。
,加入1.00 mL 0.010 0 mol・L-1的碘水,正好将所取溶液中过量的Na2S2O3全部氧化。
试计算1 L该气体样品中有多少毫克(mg)的CO。
参考答案:1.75 mg
本题解析:根据题意,反应中各物质间的关系为:5CO―I2―2
得 与CO和I2O5反应生成的I2的物质的量为:
与CO和I2O5反应生成的I2的物质的量为:
n( )="0.005" 0 mol・L-1×30.00 mL×10-3L・mL-1-5×0.010 0 mol・L-1×1.00 mL×10-3 L・mL-1×2=5.00×10-5 mol
)="0.005" 0 mol・L-1×30.00 mL×10-3L・mL-1-5×0.010 0 mol・L-1×1.00 mL×10-3 L・mL-1×2=5.00×10-5 mol
n(CO)= n(
n( )=
)= ×5.00×10-5 mol=1.25×10-4 mol
×5.00×10-5 mol=1.25×10-4 mol
m (CO)=1.25×10-4 mol×28 g・mol-1=3.50×10-3 g
c (CO)= =1.75×10-3 g・L-1="1.75" mg・L-1。
=1.75×10-3 g・L-1="1.75" mg・L-1。
本题难度:简单
2、填空题 水是一种重要的自然资源,是人类赖以生存不可缺少的物质。水质优劣直接影响人体健康。
(1)含有较多?的水称为硬水,硬水加热后产生沉淀的离子方程式为____________(写出生成一种沉淀物的即可)。
(2)下图为某饮用水厂从天然水制备纯净水(去离子水)的工艺流程示意图:
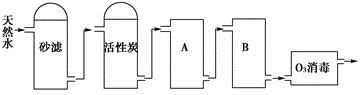
①活性炭的作用是____________;O3消毒的优点是___________。
②A、B中放置的物质名称分别是A_________;B__________。A、B中放置的物质是否可以互换?请说明原因__________。
(3)通过施加一定压力使水分子通过半透膜而将大分子或离子截留, 从而获得纯净水的方法称为?。电渗析法净化水时, 使离子通过半透膜的推动力是?。
(4)检验蒸馏水的纯度时, 最简单易行的方法是测定水的?。
(5)某城市用水中,c(Ca2+)为1.0×10-3mol/L, c(Mg2+)为5.0×10-4mol/L,c(HCO3-)为8.0×10-4mol/L。如用药剂软化该水1000L,应加入Ca(OH) 2?g, Na2CO3__________ g
参考答案:(1)Ca2+、Mg2+? Ca2++ 2HCO3- CaCO3↓+CO2↑+H2O(或Mg2++ 2HCO3-
CaCO3↓+CO2↑+H2O(或Mg2++ 2HCO3- MgCO3↓+CO2↑+H2O? MgCO3+2H2O=Mg(OH)2+CO2↑+H2O)
MgCO3↓+CO2↑+H2O? MgCO3+2H2O=Mg(OH)2+CO2↑+H2O)
(2) ①吸附水中的有机物(或去除水中的异味);反应产物无毒无害
②阳子交换树脂;阴离子交换树脂;水中的Ca2+ 、Mg2+会与阴离子树脂中的OH-生成Mg(OH)2、Ca(OH)2沉淀造成堵塞,损坏离子交换树脂。
(3)反渗透法;电势差或电场力
(4)电导率或电阻率?
(5)66.6? 116.6
本题解析:(1)含钙、镁离子较多的水为硬水,硬水加热后与碳酸氢根离子反应生成碳酸钙沉淀、碳酸镁沉淀或氢氧化镁沉淀。离子方程式为:
Ca2++2HCO3- CaCO3↓+CO2↑+H2O(或Mg2++2HCO3-
CaCO3↓+CO2↑+H2O(或Mg2++2HCO3- MgCO3↓+CO2↑+H2O? MgCO3+2H2O=Mg(OH)2+CO2↑+H2O
MgCO3↓+CO2↑+H2O? MgCO3+2H2O=Mg(OH)2+CO2↑+H2O
(2)①活性炭具有吸附性,其作用为吸附水中的有机物(或去除水中的异味),臭氧具有强氧化性,可用O3消毒,其优点是还原产物无毒。
②A、B的作用除去钙、镁离子,应先透过金属阳离子,则A为阳离子交换膜,B为阴离子交换膜,A、B不能放反,否则水中的Ca2+、Mg2+会与阴离子树脂中的OH-生成Mg(OH)2、Ca(OH)2沉淀造成堵塞,损坏离子交换树脂。
(3)压力使水分子通过半透膜而将大分子或离子截留,为反渗透法;电渗析法净化水时,电势差(或电场力)使离子通过半透膜。
(4)蒸馏水为纯水,其电导率很低,则检验蒸馏水的纯度时,最简单易行的方法是测定水的电导率或电阻率。
(5)c(Ca2+)=1.0×10-3mol/L,c(Mg2+)=5.0×10-4mol/L,c(HCO3-)=8.0×10-4mol/L.如用药剂软化该1000L,n(Ca2+)=1000L×1.0×10-3mol/L=1mol
,n(Mg2+)=1000L×5.0×10-4mol/L=0.5mol,
n(HCO3-)=1000L×8.0×10-4mol/L=0.8mol,加入氢氧化钙发生的反应为:
Mg2++2OH-=Mg(OH)2↓?
0.5mol 1mol
HCO3-+OH-=CO32-+H2O
0.8mol 0.8mol
共需要n(OH-)=1.8mol则需要Ca(OH)2的质量为1.8mol×1/2×74g/mol=66.6g
水溶液中Ca2+物质的量为1mol+0.9mol=1.9mol,其中需要加入的碳酸根离子为1.9mol-0.8mol=1.1mol,其质量为1.1mol×106g/mol=116.6g。
本题难度:简单
3、选择题 垃圾分类从你我他开始。废电池属于

参考答案:C
本题解析:A用于回收B、C、D之外的其它垃圾,A错;B用于回收各种废弃金属及制品、塑料等垃圾,不符合题意;C用于回收会造成环境污染或危害人体健康的物质,C正确;D回收厨房垃圾,也不符合。
本题难度:简单
4、选择题 酸雨是指
A.酸性的雨
B.pH<5.6的雨
C.pH=5.6的雨
D.pH<7的雨
参考答案:B
本题解析:pH<5.6的雨才叫酸雨。酸雨主要是由于溶解了SO2而形成的。
本题难度:简单
5、选择题 水体污染加剧水资源短缺,严重危害人体健康。下列关于水污染的描述中不正确的是( )
A.水俣病是由汞等重金属污染水体而造成的
B.“赤潮”和“水华”是由水体富营养化而形成的
C.海湾战争期间波斯湾严重的石油泄漏事件是人类历史上一次灾难性的水体污染事件
D.化肥和农药的广泛使用可以促进农产品增产,不会造成水体污染
参考答案:D
本题解析:本题取材于教材中“爱护水资源”中的典型水污染实例,A属于重金属污染,B属于植物营养物质污染,C属于石油泄漏污染。D选项化肥和农药的广泛使用也是当前水体污染的重要因素。答案:D
本题难度:简单