��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ͬ���������в����Ƴ���ͬ���ȵ����ӣ��ܵ������������������?
[? ]
A��������
B��������
C����������
D��̼����
�ο��𰸣�B
���������
�����Ѷȣ���
2��ʵ���� �������ԭ���ܹ�ҵ������Դ��ҵ�е���Ҫ���ʡ���ҵ�ϳ��æ¡���﮿�(��Ҫ�ɷ���LiAlSi2O6�����������ơ�þ����)�Ʊ�����ﮣ��������������£�

��֪Li2CO3����ˮ����ش��������⣺
��1��д��LiAlSi2O6�����ᷴӦ�Ļ�ѧ����ʽ_______________________��
��2������B����Ҫ�ɷ���_____________(д��ѧʽ)��
��3������Ũ��Li2SO4��Һʱ����Ҫʹ�õĹ�������������������_________��_________��
��4��������������������Ũ��Li2SO4��Һ��Ŀ����____________________��
��5�����������﮵��ʱ������FeF3���������Ļ������ʣ�FeF3����FeCl3��40%HF��Һ��Ӧ�Ʊ������Ʊ���������Ҫѡ�����ƾ��ķ���ϩ���ϵ��������з�Ӧ������������ͨ�IJ����������մ���������ԭ����_________________________________(�û�ѧ��Ӧ����ʽ��ʾ)��
��6������﮿����ڴ�����������ԭ���ǣ���2Li��H2��2LiH����LiH��H2O��LiOH��H2��������֪LiH���ܶ�Ϊ0.82g��cm-3���ý��������224L H2����״����ǡ����ȫ��Ӧ�������ɵ�LiH������뱻���յ����������֮��Ϊ1: ______(��ȷ������)��
�ο��𰸣���1�� 2LiAlSi2O6��4H2SO4��Li2SO4��Al2(SO4) 3��4H2SiO3��(2��)��
(2) Al(OH)3��CaCO3 (2��)? (3)�ƾ���(1��)?������(1��)��
(4)̼�������ˮ������Ũ����Ŀ����������Һ�������Ũ�ȣ�ʹ�����Ũ����̼�������Ũ��֮������Ksp(Li2CO3)���Ա����̼��﮳�����(3��)
(5)SiO2��4HF��SiF4����2H2O(2��)��(6) 1148(2��)��
����������¡���﮿�����������������ﮡ���������������������˳�ȥ���ᣬ��Һ�м���Ca(OH)2��Na2CO3������CaCO3��Al(OH)3���dz���B�����ˣ��õ��������Һ������Ũ������Na2CO3�õ�Li2CO3������������õ�LiCl������ﮡ���6����������10Ħ��������LiH20Ħ����������160�ˣ������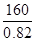 �������������22400�����������Ϊ1:1148
�������������22400�����������Ϊ1:1148
�����Ѷȣ�����
3������� ��14�֣�̼���ȹ㷺Ӧ���ڵ��ӹ�ҵ��������ʯ����Ҫ�ɷ�ΪSrSO4��Ϊ����ԭ���Ʊ�̼���ȡ�
��1��̼��ԭ���Ʊ���
����֪��SrSO4(s) + 4C(s)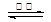 4CO(g) + SrS(s)? ��H=+a kJ��mol-1?
4CO(g) + SrS(s)? ��H=+a kJ��mol-1?
SrSO4(s) + 2C(s)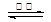 2CO2(g) + SrS(s)? ��H=+b kJ��mol-1?
2CO2(g) + SrS(s)? ��H=+b kJ��mol-1?
��ӦC(s) + CO2(g)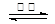 2CO(g)�ġ�H= ___________kJ��mol-1��
2CO(g)�ġ�H= ___________kJ��mol-1��
��SrS��ǿ�������Σ���ˮ�з���ˮ��Ļ�ѧ��Ӧ����ʽΪ_______________________��
��ˮ������Sr(OH) 2��NH4HCO3�������ʵ�����1:1Ͷ���Ʊ�SrCO3����ѧ��Ӧ����ʽΪ__________________________________________________��
��2��ʪ���Ʊ�������֪��Ksp��SrSO4��=3.2��10-7��Ksp��SrCO3��=1.1��10-10����
�ٽ�����ʯ�����Na2CO3��Һ������ȡ����ȣ����������ӷ�Ӧ����ʽΪ�� ____________��
�ڵ�ת�����ʱ�����Һ��c(CO32-)= 1.0��10-3mol/L��c(SO42-)=______________mol/L��?
�ο��𰸣���1����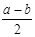 ?��2�֣�? ��2SrS+2H2O
?��2�֣�? ��2SrS+2H2O Sr(OH)2+Sr(HS)2��3�֣�
Sr(OH)2+Sr(HS)2��3�֣�
��Sr(OH)2+NH4HCO3= SrCO3+H2O+NH3��H2O��3�֣�
��2����SrSO4 + CO32- = SrCO3 + SO42-?��3�֣�?��2.91��3�֣�
�����������1���ٿ����˹���ɵ�Ӧ�á�����ӦSrSO4(s) + 4C(s)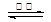 4CO(g) + SrS(s)��SrSO4(s) + 2C(s)
4CO(g) + SrS(s)��SrSO4(s) + 2C(s)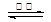 2CO2(g) + SrS(s)������õ�2C(s) + 2CO2(g)
2CO2(g) + SrS(s)������õ�2C(s) + 2CO2(g)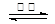 4CO(g)������C(s) + CO2(g)
4CO(g)������C(s) + CO2(g)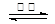 2CO(g)�ġ�H=
2CO(g)�ġ�H=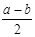 kJ��mol-1��
kJ��mol-1��
��ǿ�������Σ�ˮ���Լ��ԣ�����ʽΪ2SrS+2H2O Sr(OH)2+Sr(HS)2��
Sr(OH)2+Sr(HS)2��
�۸���ԭ���غ��֪����ӦʽΪSr(OH)2+NH4HCO3= SrCO3+H2O+NH3��H2O��
��2���ٸ��ݸ��ֽⷴӦ���ص��֪������ʽΪSrSO4 + CO32- = SrCO3 + SO42- ��
�ڸ����ܶȻ������ı���ʽ��֪��c(CO32-)�Uc(SO42-)��Ksp��SrCO3���UKsp��SrSO4���������й����ݼ��ɵõ�c(SO42-)��2.91mol/L��
�����Ѷȣ�һ��
4��ѡ���� ���¿�ѧ�ҡ���վ��������ѧ��ͨ�����Fe2O3��SiO2��CaO������Һ(1 600��)�Ƶ����������÷������ڹ�ҵ��ұ�����볣�淽����ȣ�����˵���������?
A���ܴ���Ƚ����ܺ�
B����������Ʒ����
C����������������ŷ�
D�����ǵ�ⷨұ��
�ο��𰸣�A
�����������һ����û�ԭ����ԭ������ⷨұ��ʱ��Ҫ���Ĵ����ĵ��ܣ�����ѡ��A�Ǵ���ģ��������ȷ�ģ���ѡA��
�����Ѷȣ���
5��ѡ���� �����й����ǽ������ϵ�˵���У�����ȷ����
[? ]
A���ߴ������������뵼�����
B��SiO2?�Ƴɲ�����ά�����ڵ�������ǿ���������������
C��������ˮ�ࡢ�մ���ɷ־����й�����
D��Si3N4��һ���������ǽ������ϣ����������췢����
�ο��𰸣�B
���������
�����Ѷȣ���