微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列电子式的书写中,正确的是( )
A.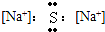
B.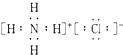
C.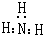
D.
参考答案:A、硫化钠是离子化合物,简单阳离子不用中括号,阴离子(S2-)采用中括号,硫化钠正确的电子式为: ,故A错误;
,故A错误;
B、氯化铵属于离子化合物,电子式中标出阴阳离子的电荷,氯化铵的电子式为: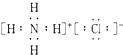 ,故B正确;
,故B正确;
C、氨气属于共价化合物,氮元素的一对孤对电子必须标出,氨气的电子式为: ,故C错误;
,故C错误;
D、H2O是共价化合物,分子里没有离子键,只有含有离子键时才能用中括号,并且标明离子符号,水的电子式为: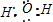 ,故C错误;
,故C错误;
故选B.
本题解析:
本题难度:简单
2、填空题 (12分) 已知 X、Y、Z、Q、R、E六种元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如下 表。
表。
元素
| 结构或性质信息
|
X
| 原子的L层上s电子数等于p电子数。
|
Y
| 原子核外的L层有3个未成对电子。
|
Z
| 在元素周期表的各元素中电负性仅小于氟。
|
Q
| 单质常温、常压下是气体,原子的M层上有1个未成对的p电子。
|
R
| 核电荷数是Y与Q的核电荷数之和
|
E
| 原子序数比R大3
|
请根据信息回答有关问题:
(1)元素Y?的原子核外 共有?种不同运动状态的电子,有?种不同能级的电子。
共有?种不同运动状态的电子,有?种不同能级的电子。
(2)X、Y、Z三种元素的电负性由高到低的排列次序依次为(写元素符号)?。
(3)X、Z、Q元素均表现最低化合价时的三种氢化 物中,沸点由高到低
物中,沸点由高到低 的排列次序依次为(写化学式)?。
的排列次序依次为(写化学式)?。
(4)R的最高化合价为?。R的一种配合物的化学式为RCl3・6H2O。已知0.01 molRCl3・6H2O在水溶液中用过量硝酸银溶液处理,产生0.02 mol AgCl沉淀。此配合物最可能是?。
A.[R(H2O)6]C l3? B.[R(H2O)5Cl]Cl2・H2O
l3? B.[R(H2O)5Cl]Cl2・H2O
C. [R(H2O)4Cl2]Cl・2H2O? D.[R(H2O)3Cl3]・3H2O
[R(H2O)4Cl2]Cl・2H2O? D.[R(H2O)3Cl3]・3H2O
(5)元素E能形成八面体构型的配合物离子[E (YH3) x Q 2]+,则中心离子为(写化学式)?,配位体为(写化学式)?,x 的值为?。
(6)Y的最低价氢化物与Z的一种氢化物反应,生成的两种产物均不 污染环境,其反应的化学方程式为??。
污染环境,其反应的化学方程式为??。
参考答案:

本题解析:略
本题难度:一般
3、选择题 下列物质中,含有共价键的化合物是
[? ]
A.碘化氢
B.烧碱
C.液溴
D.食盐
参考答案:AB
本题解析:
本题难度:简单
4、选择题 下列各组物质中,都是由极性键构成极性分子的一组是
[? ]
A.CH4和Br2
B.NH3和H2O
C.H2S和CCl4
D.CO2和HCl
参考答案:B
本题解析:
本题难度:简单
5、填空题 【化学 ――选修3:物质结构】(15分)
氮元素可形成卤化物、叠氮化物及络合物等。
(1)NF3构型为三角锥形,沸点为-129 ℃;可在铜 催化作用下由F2和过量NH3反应得到。NF3属于________晶体.
催化作用下由F2和过量NH3反应得到。NF3属于________晶体.
(2)氢叠氮酸(HN3)是一种弱酸,它的酸性类似于醋酸,微弱电离出H+和N。
①与N互为等电子体的分子、离子有______、________(各举1例),由此可推知N的空间构型是______形。
②叠氮化物、氰化物能与Fe3+、Cu2+及Co3+等形成络合物,如Co[(N3)(NH3)5]SO4、[Fe(CN)6]4-。写出钴原子在基态时的价电子排布式:__________。如Co[(N3)(NH3)5]SO4、中钴的配位数为________,CN-中C原子的杂化类型是________。
(3)由叠氮化钠(NaN3)热分解可得纯N2:2NaN3(s)===2Na(l)+3N2( g),有关说法正确的是________(选填序号)。
A.NaN3与KN3结构类似,前者晶格能较小
B.第一电离能(I1):N>P>S
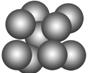
C.钠晶胞结构如图,该晶胞分摊2个钠原子
D.常温下,氮气很稳定,是因为氮的电负性小
参考答案:(1) 分子?( 1分 ) ?
(2)? ①N2O或CO2 ( 2分 ) OCN-或CNO- ( 2分 )?直线 ( 2分 )
②3d74s2 ( 2分 )?6 ( 2分 )sp杂化 ( 2分 )
(3)BC?( 2分)
本题解析:略
本题难度:一般