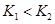��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��10�֣�ֱ���ŷź�SO2���������γ����꣬Σ�������������Ƽ�ѭ�������ѳ������е�SO2��
��1���û�ѧ����ʽ��ʾS�γ���������ķ�Ӧ����ʽ����������������������������
��2�����Ƽ�ѭ�����У�Na2SO3��Һ��Ϊ����Һ������NaOH��Һ����SO2�Ƶã��÷�Ӧ�����ӷ���ʽ��?��
��3������Һ����SO2�Ĺ����У�pH��n(SO3?��)��n(HSO3��)�仯��ϵ���±�:
n(SO3?��):��n(HSO3��)
| 91��9
| 1��1
| 1��91
|
PH
| ��.��
| 7.2
| 6.2
|
���ϱ��ж�NaHSO3��Һ���������������ԣ��û�ѧƽ��ԭ������:��������������������������
�ڵ�����Һ������ʱ����Һ������Ũ�ȹ�ϵ��ȷ����(ѡ����ĸ):������������������������
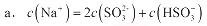

��4��������Һ��pH����ԼΪ6ʱ��������������������ʾ��ͼ����:

��HSO3-�������ŵ�ĵ缫��Ӧʽ����������������������������������
�ڵ�����������ҺPH����8����ʱ������Һ������ѭ�����á���������ԭ��:����������������
������������������������
2������� ���û�ѧ��Ӧԭ���о��������ȡ���ȵ��ʼ��仯����ķ�Ӧ����Ҫ���塣
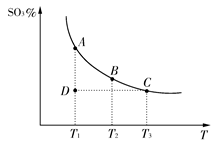
���������У�SO2����������SO3��2SO2(g)��O2(g)  2SO3(g)�������ϵ��SO3�İٷֺ������¶ȵĹ�ϵ����ͼ��ʾ(�������κ�һ�㶼��ʾƽ��״̬)������ͼʾ�ش��������⣺
2SO3(g)�������ϵ��SO3�İٷֺ������¶ȵĹ�ϵ����ͼ��ʾ(�������κ�һ�㶼��ʾƽ��״̬)������ͼʾ�ش��������⣺
(1)2SO2(g)��O2(g)  2SO3(g)�Ħ�H________0(�>����<��)�����ں��£���ѹ������������ƽ����ϵ��ͨ�뺤����ƽ��________�ƶ�(��������ҡ�����)��
2SO3(g)�Ħ�H________0(�>����<��)�����ں��£���ѹ������������ƽ����ϵ��ͨ�뺤����ƽ��________�ƶ�(��������ҡ�����)��
(2)���¶�ΪT1��T2����Ӧ��ƽ�ⳣ���ֱ�ΪK1��K2����K1________K2������Ӧ���е�״̬Dʱ��v��________v��(�>����<������)��
3��ѡ���� ��һ������ɱ���ܱ������У�ͨ��2molHI���壬��һ�������½�������ƽ�⣺2H1��g�� I2(g)+H2(g);��H>0�����ƽ��ʱ�������Ϊ1L��c(I2)=0.5mol/L���ı�������������н�����ȷ����
I2(g)+H2(g);��H>0�����ƽ��ʱ�������Ϊ1L��c(I2)=0.5mol/L���ı�������������н�����ȷ����
A����������������䣬�����¶ȣ�����������ɫ��dz
B����������������¶Ȳ��䣬����һ���������������뷴Ӧ����������Ӧ���ʺ��淴Ӧ���ʾ�����
C�������¶Ȳ��䣬����ѹ��������ʹ��������㶨Ϊ0.2L��һ��ʱ����c(I2)=25mol/L
D����������ѹǿ���¶Ȳ��䣬��ͨ��2molHI���壬����ƽ��״̬���HI��ת����Ϊ60%
4��ѡ���� ��2A��B 3C��4D�У���ʾ�÷�Ӧ����������
3C��4D�У���ʾ�÷�Ӧ����������
[? ]
A����(A) = 0��5mol��L-1��S-1
B����(B) = 0��3 mol��L-1��S-1
C����(C) = 0��8mol��L-1��S-1
D����(D)= 1 mol��L-1��S-1
5��ѡ���� �ں����ܱ������д�������ƽ�⣺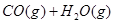

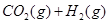 ��
��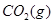 ?��ƽ�����ʵ���Ũ��
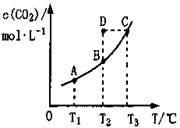
?��ƽ�����ʵ���Ũ��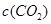 ���¶�T�Ĺ�ϵ����ͼ��ʾ������˵��������ǣ�?��?
���¶�T�Ĺ�ϵ����ͼ��ʾ������˵��������ǣ�?��?
A����Ӧ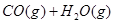

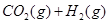 ��
��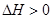
B����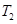 ʱ������Ӧ����״̬
ʱ������Ӧ����״̬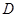 ����һ����
����һ����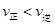
C��ƽ��״̬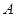 ��
�� ��ȣ�ƽ��״̬
��ȣ�ƽ��״̬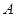 ��
�� С
С
D����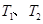 ʱ��ƽ�ⳣ���ֱ�Ϊ
ʱ��ƽ�ⳣ���ֱ�Ϊ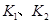 ����
����