微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 阿伏加德罗常数约为6.02×1023 mol-1,下列说法中错误的是
A.标准状况下,3.01×1023个CCl4所占的体积约为11.2 L
B.80 gNH4NO3晶体中约含有NH4+6.02×1023个
C.3.9 gNa2O2吸收足量的CO2时转移的电子数约是3.01×1022
D.46 gNO2和N2O4混合气体中含有原子数约为1.806×1024
参考答案:A
本题解析:
本题难度:一般
2、选择题 在标准状况下,1L的密闭容器中恰好可盛放n个N2分子和m个H2分子组成的混合气体,则阿伏加德罗常数可近似表示为
[? ]
A.22.4(m+n)
B.22.4×6.02×1023(m+n)
C.22.4(m+n)/(6.02×1023)
D.m+n
参考答案:A
本题解析:
本题难度:简单
3、选择题 若NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.含有NA个氖原子的氖气在标准状况下的体积约为11.2L
B.2.3gNa被O2完全氧化时,失去0.1?NA个电子
C.2L 1mol?L-1的醋酸溶液中含有2NA个醋酸分子
D.标准状况下,5.6L苯含有O.25NA个分子
参考答案:A、由于氖是单原子的气体,NA个氖原子的氖气物质的量是1mol,标准状况下的体积约为22.4L,故A错误;
B、2.3g钠物质的量是1mol,失去0.1mol电子,即失去0.1 NA个电子,故B正确;
C、醋酸的物质的量是2mol,由于醋酸是电解质,溶液中发生电离,故溶液中醋酸的物质的量小于2mol,即小于2NA个醋酸分子,故C错误;
D、苯在标准状况下是液体,无法计算其物质的量,故D错误;
故选B.
本题解析:
本题难度:一般
4、选择题 NA为阿伏加德罗常数,下列说法正确的是( )
A.1molNa2O2与H2O完全反应,转移2NA个电子
B.2L0.5mol/L的氯化镁溶液中所含的粒子数为3NA
C.NA个SO2分子所占的体积与NA个SO3分子所占的体积比1:1
D.标准状况下,5.6L氯气和16.8L氧气的混合气体中含有分子数为NA
参考答案:A、2Na2O2+2H2O=4NaOH+O2↑,每生成1molO2时2molNa2O2与水完反应中转移的电子为2NA,故A错误;
B、氯化镁溶液由氯化镁和水组成,所含的粒子不仅氯化镁中的阴阳离子还有水分子,该题只是计算了氯化镁中的阴阳离子,没有水分子,故B错误;
C、标况下三氧化硫是固体,该题未说明温度、压强,所以三氧化硫的状态未知,且气体摩尔体积未知,所以无法计算二氧化硫和三氧化硫的体积,故C错误;
D.标准状况下,5.6L氯气和16.8L氧气的混合气体的物质的量为1mol,所以分子总数为NA,故D正确;
故选D.
本题解析:
本题难度:简单
5、计算题 .在120℃,1.01×105Pa时,将4mLO2和3mLNxHy(y>x)混合气体充入一密闭与容积可变的容器中,点燃充分反应,恢复到原温度和压强,测得容器中N2、O2、H2O混合气体密度减小3/10。
(1)试写出该反应的化学方程式为 。
(2)通过计算推断NxHy的分子式:
参考答案:4NxHy+yO2 →2xN2+2yH2O 反应前后质量守恒,同温同压下气体密度与气体体积成反比 x=2,y=4 N2H4
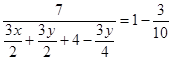
本题解析:
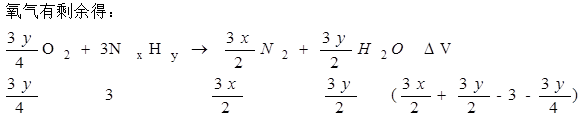
反应前后质量守恒,同温同压下气体密度与气体体积成反比,即等质量,同温同压,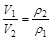 ,则反应后气体体积为:10ml。
,则反应后气体体积为:10ml。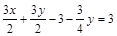 ,化简:
,化简: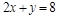 ,讨论得x=2,y=4。
,讨论得x=2,y=4。
(1)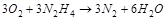
本题难度:一般