微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 根据判断,下列元素一定属于主族元素的是
A.X元素能形成+7价的含氧酸及其盐
B.Y元素的原子最外层上有7个电子
C.Z元素阳离子与惰性气体元素原子的电子层结构相同
D.R元素的氧化物是两性氧化物
参考答案:B
本题解析:
本题难度:一般
2、简答题 下表列出了①~⑤五种元素在周期表中的位置:

请按要求回答下列问题:
(1)元素④的原子结构示意图为______.
(2)元素①和③形成的化合物中的化学键是______共价键(填“极性”或“非极性”).
(3)元素①单质的电子式为______.
(4)元素②~⑤的原子半径由大到小的顺序为(填元素符号)______,它们的最高价氧化物对应的水化物中,酸性最强的是______(填化学式).
(5)元素②的单质在氧气中燃烧的产物与二氧化碳反应的化学方程式为______;元素③的最高价氧化物与烧碱溶液反应的离子方程式为______.
参考答案:根据元素在周期表中的位置知,①②③④⑤分别是N、Na、Si、S、Cl元素,
(1)元素④的原子核外有3个电子层,K、L、M电子层上电子数分别是2、8、6,其原子结构示意图为: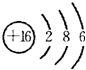 ,
,
故答案为: ;
;
(2)元素①和③形成的化合物是Si3N4,氮化硅中N和Si原子之间存在极性共价键,故答案为:极性;
(3)元素①单质是N2,氮原子之间存在氮氮三键,其电子式为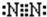 ,故答案为:
,故答案为: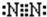 ;
;
(4)同一周期元素中,元素原子半径随着原子序数的增大而减小,所以原子半径大小顺序是Na>Si>S>Cl;同一周期元素中,元素的非金属性随着原子序数的增大而增强,元素的非金属性越强,其最高价氧化物的水化物酸性越强,这几种元素非金属性最强的元素是Cl元素,所以酸性最强的酸是HClO4,
故答案为:Na>Si>S>Cl;HClO4;
(5)Na在氧气中燃烧生成Na2O2,Na2O2与CO2反应生成Na2CO3和O2,反应方程式为:2Na2O2+2CO2=2Na2CO3+O2;元素③的最高价氧化物是SiO2,SiO2与NaOH溶液反应生成Na2SiO3和H2O,离子反应方程式为:SiO2+2OH-=SiO32-+H2O,故答案为:2Na2O2+2CO2=2Na2CO3+O2;SiO2+2OH-=SiO32-+H2O.
本题解析:
本题难度:一般
3、选择题 下列叙述正确的是( )
A.N、O、S元素的原子半径依次增大
B.由于Si原子半径较大,SiH4比CH4稳定
C.若aXm+和bYN-两种离子电子层结构相同,则a-b=n-m
D.元素周期表从IIIB族到IIB族10个纵列的元素都是金属元素
参考答案:A、同周期原子半径从左向右在减小,则原子半径N>O,同主族元素的原子半径从上到下在增大,则原子半径S>O,S的电子层最多,则硫原子半径最大,氧原子半径最小,故A错误;
B、因非金属性C>Si,则气态氢化物的稳定性为CH4>SiH4,故B错误;
C、因两种离子电子层结构相同,则a-m=b+n,即a-b=m+n,故C错误;
D、从IIIB族到IIB族10个纵列的元素为过渡元素,过渡元素都是金属元素,故D正确;
故选D.
本题解析:
本题难度:简单
4、选择题 下列关于同主族元素的说法中错误的是( )
A.同主族元素随原子序数递增,元素原子失电子能力逐渐增强
B.同主族元素随原子序数递增,单质氧化性逐渐增强
C.同主族元素原子最外层电子数都相同
D.同主族元素的原子半径,随原子序数增大而逐渐增大
参考答案:A.同主族元素随原子序数递增,元素金属性增强,失电子能力增强,故A正确;
B.同主族元素随原子序数递增,元素的非金属性减弱,单质氧化性逐渐减弱,故B错误;
C.主族元素的族序数等于其最外层电子数,所以主族元素原子最外层电子数都相同,故C正确;
D.随原子序数增大而逐渐增大,主族元素的原子核外电子层数最多,原子半径增大,故D正确;
故选B.
本题解析:
本题难度:简单
5、选择题 下列事实能判断金属元素甲的金属性一定比乙强的有
①甲单质能与乙盐的溶液反应并置换出乙
②甲、乙两元素原子的最外层电子数相同,且甲的原子半径小于乙
③甲、乙两短周期元素原子的电子层数相同,且甲的原子序数小于乙
④甲、乙两元素的最高价氧化物水化物的碱性甲大于乙
⑤两单质分别与氯气反应时生成的阳离子,甲失去的电子数比乙多
A.全部可以
B.仅②可以
C.仅②⑤不可以
D.①③④可以
参考答案:D
本题解析:
本题难度:简单