|
高中化学知识点总结《常见的化学电源》考点特训(2017年冲刺版)(二)
2017-07-18 02:06:14
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应
产生电流。电池总反应为:4A1+3O2+6H2O=4A1(OH)3,下列说法不正确的是( )
A.正极反应式为:O2+2H2O+4e--=4OH--
B.电池工作时,电流由铝电极沿导线流向铂电极
C.以网状的铂为正极,可增大与氧气的接触面积
D.该电池通常只需更换铝板就可继续使用
|
参考答案:B
本题解析:
试题解析:正极上通入空气,发生还原反应,正极反应式为O2+2H2O+4e-=4OH-,故A正确;电池工作时,电流由正极流向负极,即从铂电极沿导线流向铝电极,故B错误;铂做成网状的目的是增大与氧气的接触面积,故C正确;不断反应,不断溶解,所以一段时间后,更换铝板就可以继续使用,故D正确.
考点:化学电源新型电池
本题难度:一般
2、选择题 镁/H2O2酸性燃料电池采用海水作电解质(加入一定量的酸),下列说法正确的是
[? ]
A.电池总反应为:Mg+H2O2=Mg(OH)2
B.正极发生的电极反应为:H2O2+2H++2e-=2H2O
C.工作时,正极周围海水的pH增大
D.电池工作时,溶液中的H+向负极移动
参考答案:BC
本题解析:
本题难度:一般
3、选择题 关于铜锌原电池和电解CuCl2溶液的装置(如右图),下列说法正确的是 ?
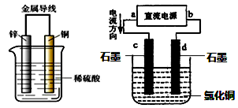
A.锌是负极,铜片上有气泡产生,电流从锌片经导线流向铜片
B.铜片质量逐渐减少,氢离子在铜片表面被还原
C.d为阳极,电极反应为:2Cl―-2e―=Cl2↑
D.电解过程中, d电极质量增加
参考答案:D
本题解析:A 错误,是电子从锌片经导线流向铜片
B 错误,铜片质量不变
C 错误,d为阴极,Cu2++2e―=Cu
D 正确,铜在d电极析出,质量增加。
本题难度:一般
4、选择题 锂钒氧化物电池的能量密度远远超过其他材料电池,电池总反应式为:V2O5+xLi→LixV2O5,下列说法不正确的是
A.向外供电时,锂离子向负极移动
B.负极上反应的物质是锂,正极上反应的物质是V2O5
C.正极的电极反应为:V2O5+xe-+xLi+→LixV2O5
D.负极的电极反应为:xLi-xe-→ xLi+
参考答案:A
本题解析:反应中V由+5价降为 价,Li由0价升为+1价,负极上反应的物质是Li,正极上反应的物质是V2O5,B正确;负极反应为Li-e-=Li+,D正确;正极反应为V2O5+xe-+xLi+=LixV2O5,C正确;原电池内部阳离子向正极迁移、阴离子向负极迁移,A错误。 价,Li由0价升为+1价,负极上反应的物质是Li,正极上反应的物质是V2O5,B正确;负极反应为Li-e-=Li+,D正确;正极反应为V2O5+xe-+xLi+=LixV2O5,C正确;原电池内部阳离子向正极迁移、阴离子向负极迁移,A错误。
点评:原电池中负极失电子、正极得电子;原电池内部阳离子向正极迁移、阴离子向负极迁移。
本题难度:简单
5、填空题 (每空2分,共8分)熔融盐燃料电池具有高的发电效率,因而受到重视。某燃料电池以熔融的K2CO3(其中不含O2-和HCO3-)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池负极电极反应式为:
2C4H10+26CO32--52e-=34CO2+10H2O
试回答下列问题:
(1)该燃料电池的化学反应方程式为?;
(2)正极电极反应式为?。
(3)为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此,必须在通入的空气中加入一种物质,加入的物质是?,它来自?。
参考答案:(每空2分,共8分)(1)? 2C4H10+13O2=8CO2+10H2O?;?
(2)? O2+2CO2+4e-=2CO32-?。(3)? CO2?,?负极反应产物
本题解析:(1)原电池中负极失去电子,正极得到电子,所以丁烷在负极通入,氧气在正极通入,所以总反应式为2C4H10+13O2=8CO2+10H2O。
(2)总反应式减去负极电极反应式即得到正极电极反应式,即正极反应式为O2+2CO2+4e-=2CO32-。
(3)根据正极反应式可知,正极消耗CO2,所以必需在正极加入CO2补充。由于负极产生CO2,所以加入的CO2可来自于负极产生的CO2。
本题难度:一般
|