微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (14分)现向含6 mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加人KBrO3的物质的量的关系如图所示。请回答下列问题:
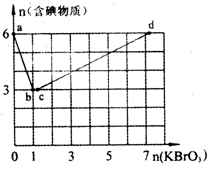
(1)b点时,KI反应完全,则氧化产物与还原产物的物?质的量之比为____,电子转移数目为?。
(2)已知b→c过程中,仅有溴元素发生化合价变化,写出并配平该反应的离子方程式?。
(3)已知在c→d段发生下列反应: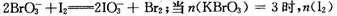 =?mol,再向溶液中通入足量乙烯,充分反应后溶液增加的质量为?g。
=?mol,再向溶液中通入足量乙烯,充分反应后溶液增加的质量为?g。
(4)含a mol KI的硫酸溶液所能消耗n(KBrO3)的最大值为____。整个过程中转移的电子数目为____。
参考答案:(14)(1)3:1;(2分)6NA(或6×6.02×1023);(2分).
(2)BrO3-+ 5Br- + 6H+ =3Br2 + 3H2O;(2分)
(3)2.1(2分);100.8(2分)
(4)1.2a(2分) 6aNA(2分)
本题解析:本题考察了氧化还原反应知识在图表中的综合分析能力。(1)在b点时,纵坐标的含碘物质从6mol到3mol,应该是有I2生成,即发生BrO3-+ 6I- + 6H+ =3I2 + 3H2O + Br-。(2)b→c过程中纵坐标的含碘物质不变,则I2未反应,应该为生成的Br-反应。(3)c点前,横坐标消耗KBrO31.2mol,当n(KBrO3)=3mol时,c→d段则消耗KBrO31.8mol。(4)综合三阶段反应,a mol KI最多消耗1.2 a mol KBrO3,最后产物为Br2、IO3-,所以转移电子数目为6a mol。
本题难度:一般
2、选择题 在2KMnO4+16HCl====2KCl+2MnCl2+5Cl2↑+8H2O反应中(? )
A.氧化产物与还原产物粒子个数比是2∶5
B.被氧化的盐酸占参加反应盐酸总数的5/8
C.KMnO4只有一部分发生还原反应
D.KMnO4与HCl恰好分别完全发生还原反应和氧化反应
参考答案:B
本题解析:这是一道部分氧化还原反应的题目,根据电子转移数相等,2个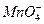 得到10e-,则可氧化10个HCl分子,所以被氧化的盐酸占参加反应盐酸总分子数的5/8。
得到10e-,则可氧化10个HCl分子,所以被氧化的盐酸占参加反应盐酸总分子数的5/8。
本题难度:简单
3、选择题 已知反应:①Cl2+2KBr=2KCl+Br2, ②KClO3 +6HCl=3Cl2+KCl +3H2O,
③2KBrO3 +Cl2=Br2 + 2KClO3,下列说法正确的是
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2
C.反应②中还原剂与氧化剂的物质的量之比为6:1
D.③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol
参考答案:B
本题解析:A.②中生成物有单质但反应物没有单质,所以不是置换反应,A错误;B.①Cl2+2KBr=2KCl+Br2中氧化剂是氯气,氧化产物是溴,氯气的氧化性大于溴,②KClO3+6HCl=3Cl2+KCl+3H2O中氧化剂是氯酸钾,氧化产物是氯气,氯酸钾的氧化性大于氯气,③2KBrO3+Cl2=Br2+2KClO3中氧化剂是溴酸钾,氧化产物是氯酸钾,溴酸钾的氧化性大于氯酸钾,所以,氧化性强弱顺序是 KBrO3>KClO3>Cl2>Br2,B正确;C.②KClO3+6HCl=3Cl2+KCl+3H2O中,氧化剂是氯酸钾,还原剂是参加反应氯化氢的 ,所以还原剂和氧化剂的物质的量之比是5:1,C错误;D.③还原剂是氯气,氧化剂是溴酸钾,该反应式中lmol还原剂反应则氧化剂得到电子的物质的量=2×(5-0)mol=10mol,D错误;
,所以还原剂和氧化剂的物质的量之比是5:1,C错误;D.③还原剂是氯气,氧化剂是溴酸钾,该反应式中lmol还原剂反应则氧化剂得到电子的物质的量=2×(5-0)mol=10mol,D错误;
本题难度:一般
4、选择题 已知下面六句话:①A氧化B,②B氧化A,③A被B氧化,④B被A氧化,⑤A被B还原, ⑥B被A还原。其中和第一句话的意思相同的是
[? ]
A.②③?
B.?②④?
C.⑤⑥?
D.?④⑤
参考答案:D
本题解析:
本题难度:简单
5、选择题 下列反应中,SO2被还原的是(?)
A.SO2+2NaOH====Na2SO3
B.SO2+Cl2+2H2O====H2SO4+2HCl
C.SO2+2H2S====3S+2H2O
D.SO2+NO2====SO3+NO
参考答案:C
本题解析:SO2被还原,则硫的化合价将降低,生成单质硫,故选C。
本题难度:简单