��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��8�֣���1����MnSO4������Ļ����Һ�����K2S2O8����������أ�����Һ�ᷢ
���·�Ӧ��Mn2++S2O82-+H2O��MnO4-+SO42-+H+
�÷�Ӧ�����ڼ���Mn2+�Ĵ��ڡ�������������_________________��
����Ӧ����0.1 mol��ԭ���μӷ�Ӧ�����������������ʵ���__________mol��
��2�����÷�Ӧ���õ������̸�Ϊ�Ȼ��̣������������Ĺ�����ط�Ӧʱ�����и�����ء�����ء����������⣬�����������ﻹ��_________________��
��3����NaBiO3���壨��ɫ�ܣ����뵽MnSO4��H2SO4�Ļ����Һ����ȣ������ܽ��Ϊ������Һ���������·�Ӧ��
?NaBiO3+?MnSO4+??H2SO4�� ?Na2SO4+?Bi2(SO4)3+?NaMnO4+?H2O
����ƽ������Ӧ�Ļ�ѧ����ʽ�����������ת�Ƶķ������Ŀ��
��������Ӧ�л�ԭ������?
�ο��𰸣�(1)��Һ����ɫ��Ϊ��ɫ? 0.25? (2)Cl2
��3��10? 4? 14?�� 3? 5? 4? 14?��2��Bi2(SO4)3
�����������1������MnO4������Һ�����Ϻ�ɫ��������������Һ����ɫ��Ϊ��ɫ����ԭ����Mn2�������ϼ۴ӣ�2�����ߵ���7�ۣ�����ʧȥ5�����ӣ���������S�Ļ��ϼ۴ӣ�7�۽��͵���6�ۣ��õ�1�����ӣ�����1mol�������õ�2mol���ӣ��������Ӧ����0.1 mol��ԭ���μӷ�Ӧ�����������������ʵ���0.25mol��
��2�������ڷ�Ӧ��������Ҳ�ܱ����������Ի�����������
��3�����ݷ���ʽ��֪��Bi�Ļ��ϼ۴ӣ�5�۽��͵���3�ۣ��õ�2�����ӡ�MnSO4��Mn�Ļ��ϼ۴ӣ�2�����ߵ���7�ۣ�ʧȥ5�����ӣ�������������NaBiO3����ԭ����MnSO4�����ߵ����ʵ���֮����5�U2�����л�ԭ������Bi2(SO4)3������������NaMnO4����˷���ʽΪ
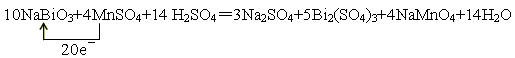
�����Ѷȣ�һ��
2��ѡ���� ������������������ȷ���ǣ�?��
A�������в�һ��������Ԫ��
B��������һ��������Ԫ��
C���ڷ�Ӧ����ʧ���ӵ�����
D���Ƿ�Ӧ���ɵ�����
�ο��𰸣�A
�����������
�����Ѷȣ���
3��ѡ���� ���з�Ӧ�У�������������ԭ��Ӧ����
A��2Na+2H2O��2NaOH+ H2��
B��2Na2O2+2 CO2��2 Na2CO3+ O2
C��NaH+ H2O �� NaOH+ H2��
D��ICl+H2O��HCl+HIO (ICl��ClΪ-1��)
�ο��𰸣�D
���������������Ԫ�ػ��ϼ������ķ�Ӧ����������ԭ��Ӧ��ѡ��D��Ԫ�صĻ��ϼ۶�û�б仯������������ԭ��Ӧ������ǣ���ѡD��
�����Ѷȣ���
4������� (10��) ͭ��Ũ���ᷢ����Ӧ�Ļ�ѧ����ʽΪ��
Cu +2H2SO4��Ũ��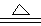 CuSO4+SO2��+2H2O
CuSO4+SO2��+2H2O
��1��ŨH2SO4��_________��������?�ԣ�����������?��д��ѧʽ����
��2���ڸ÷�Ӧ�У���������32 g Cu����ת����_______mol ���� ����ԭ��?mol H2SO4������??L SO2����״�������塣
��3��Cu��SO2�Ļ�ԭ����ǿ������˳��Ϊ��Cu?SO2���>������<����=������
�ο��𰸣���10�֣���1��������������CuSO4? (ÿ��1��)
��2��1? 0.5? 11.2?(ÿ��2��)?��3��>? (1��)
�����������1��������SԪ�صĻ��ϼ۴ӣ�6�۽��͵���4�ۣ��õ�2�����ӣ����������������������������ԡ�ͭ�Ļ��ϼ۴�0�����ߵ���2�ۣ�ʧȥ2�����ӣ�����ԭ�����������������������ͭ��
��2��32g�����ʵ�����32g��64g/mol��0.5mol����ʧȥ0.5mol��2=1.0mol���ӣ����ݵ��ӵĵ�ʧ�غ��֪������ԭ����������ʵ�����1.0mol��2��0.5mol���������ɵ�SO2����0.5mol�������ڱ�״���µ������0.5mol��22.4L/mol��11.2L��
��3��������������ԭ��Ӧ�У���ԭ���Ļ�ԭ��ǿ�ڻ�ԭ����ģ�����ͭ�Ļ�ԭ��ǿ��SO2�ġ�
�����������Ǹ߿��еij������ͣ������ѶȲ������������ǿ��ѧ�����ѵ÷֡�����Ĺؼ��������йصĸ�����Ҫȷ����й�Ԫ�صĻ��ϼ۱仯�����Ȼ�������йصĸ������������жϼ��ɡ�
�����Ѷȣ�һ��
5������� ��6�֣�ijһ��Ӧ��ϵ�з�Ӧ��������ﹲ�������ʣ�O2��H2CrO4��Cr(OH)3��H2O��H2O2����֪�÷�Ӧ�У�H2O2ֻ�������¹��̣�H2O2��O2��
��1��������H2O2�ڷ�Ӧ�б��ֳ�?����д��ţ���
a��������? b����ԭ��? c�������Ժͻ�ԭ��? d��������ȷ
��2������Ӧת����5.418��1023�����ӣ�������������ڱ�״���µ������________L��
��3���� �������ͻ�ԭ���Ļ�ѧʽ����ƽ���ϵ���������з����У����������ת�Ƶ���Ŀ��
�������ͻ�ԭ���Ļ�ѧʽ����ƽ���ϵ���������з����У����������ת�Ƶ���Ŀ��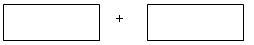
�ο��𰸣���1��b����2��10.08 ��3��2 H2CrO4? 3 H2O2?6e-
�����������
�����Ѷȣ�һ��