|
高中化学必备知识点《化学反应与能量》考点强化练习(2017年押题版)(四)
2017-07-18 02:28:10
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列过程中,需要吸收能量的是
A.H+H=H2
B.H+Cl=HCl
C.I2→I+I
D.S+O2=SO2
|
参考答案:C
本题解析:化学键的形成,释放能量;A,B错。化学键的断裂要吸收能量;C正确;燃烧反应是放热反应。所以D错。故选C。
考点:化学反应与能量
点评:熟记常见的的吸放热反应和放热反应,常见放热反应:1、金属和水或酸反应2、酸碱中和反应3、一切燃烧4、大多数化合反应和置换反应5、缓慢氧化反应如生锈常。见吸热反应:1、大多数分解反应2、铵盐和碱反应3、碳作还原剂的反应。只要学生学习过程中牢记并理解这些变化,便不难解答此题。
本题难度:一般
2、选择题 中心原子采取sp2杂化的是? ( )
A.NH3
B.BCl3
C.PCl3
D.H2O
参考答案:B
本题解析:根据杂化轨道数判断杂化类型,杂化轨道数=δ键数+孤对电子对数,则A、N原子杂化轨道数=δ键数+孤对电子对数=3+1=4,所以采取sp3杂化,故错误;B、B原子杂化轨道数=δ键数+孤对电子对数=3+0=3,所以采取sp2杂化,故正确;C、P原子杂化轨道数=δ键数+孤对电子对数=3+1=4,所以采取sp3杂化,故错误;D、O原子杂化轨道数=δ键数+孤对电子对数=2+2=4,所以采取sp3杂化,故错误,答案选C。
本题难度:一般
3、选择题 下列变化过程中,必需加入氧化剂才能实现的是
A.Na2O2→NaOH
B.CO2→CO
C.Fe2+→Fe3+
D.Ba(OH)2→BaSO4
参考答案:C
本题解析:分析:必需加入氧化剂才能实现,则选项中的物质为还原剂的变化,还原剂中元素的化合价升高,以此来解答.
解答:A.Na2O2→NaOH中O元素的化合价降低,发生氧化还原反应,但不需加还原剂,与水反应即可实现,故A不选;
B.CO2→CO中C元素的化合价降低,则需加还原剂才能实现,故B不选;
C.Fe2+→Fe3+中Fe元素的化合价升高,则需加氧化剂才能实现,故C选;
D.Ba(OH)2→BaSO4中元素的化合价没有变化,发生酸碱中和反应即可实现,故D不选;
故选C.
点评:本题考查氧化还原反应,明确元素的化合价变化是解答本题的关键,并注意氧化剂、还原剂中元素的变化来解答,难度不大.
本题难度:一般
4、实验题 (16分)二甲醚是重要的有机中间体,利用二氧化碳加氢合成二甲醚能变废为宝,且可替代汽油作为新型清洁燃料。
(1)常温常压下,二氧化碳加氢可选择性生成二甲醚或一氧化碳:
①CO2 (g)+3H2(g)=CH3OH(l)+H2O(l) △H1 =-55.7 kJ/mol
②2CH3OH(l) = CH3OCH3(g)+H2O (l) △H2 =-23.4 kJ/mol
③CO2 (g)+3H2(g) =CO(g) + H2O (l) △H 3>0
则CO2(g)加氢转化为CH3OCH3(g)和H2O (l)的热化学方程式是___________________________________________________。
(2)合成二甲醚往往选用硅铝混合物作催化剂,硅铝比例不同,生成二甲醚或一氧化碳的物质的量分数不同。下图是硅铝比与产物选择性图:
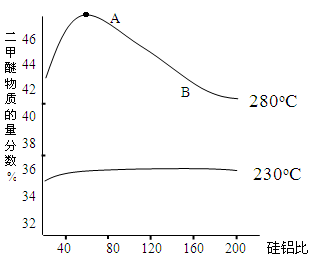
反应③的平衡常数表达式为 ,图中A点和B点的平衡常数比较:KA______KB(填“>、=、<”)。根据以上两条曲线,写出其中一条变化规律: ___________________。
(3)在280oC时,向一个2L的密闭容器中加入等量2mol二氧化碳和氢气, A点二甲醚的浓度为0.15 mol・L-1,计算在A点二氧化碳的转化率,要求写出计算过程。
(4)二甲醚逐渐发展为替代汽油的清洁燃料,在二甲醚燃料电池中,二甲醚通入______极,碱性条件下,该电极反应式是 。
参考答案:(1)2CO2(g)+6H2(g) = CH3OCH3(g)+3 H2O(l) △H =-134.8kJ/mol (3分)
(2)K=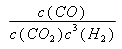 (2分) “="”" (2分) (2分) “="”" (2分)
a.温度越高,二甲醚的选择性越大;b.低温时硅铝比对二甲醚的选择性影响不大,高温时随着硅铝比增大,二甲醚的选择性先增大后减小。(其它正确答案均可得分,2分)
(3)起始状态c(H2)=c(CO2)=2mol/2L=1mol/L
2CO2+6H2=CH3OCH3+ 3H2O
c(起始) 1.00mol/L 1.00mol/L 0 0
c(转化) 0.30mol/L 0.90mol/L 0.15mol/L 0.45mol/L
c(平衡) 0.70mol/L 0.10mol/L 0.15mol/L 0.45mol/L
CO2的转化率=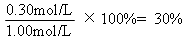 (2分,答案正确且有过程均给2分) (2分,答案正确且有过程均给2分)
(4)负 (2分) CH3OCH3+16OH--12e-
本题解析:
本题难度:一般
5、选择题 反应:CO(g) + H2O (g) = CO2(g) + H2(g) 的能量变化如图所示,有关该反应的说法正确的是
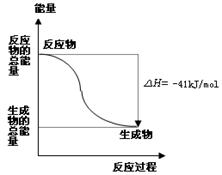
A.该反应为吸热反应
B.1mol CO2(g)和1mol H2(g)反应生成1molCO(g)和1molH2O(g)要放出41kJ热量
C.反应的热化学方程式是:CO(g) + H2O (g) = CO2(g) +H2(g)△H=+41kJ/mol
D.CO(g)与H2O(g)所具有的总能量大于CO2(g)与H2(g)所具有的总能量
参考答案:D
本题解析:从图像可看出该反应为放热反应,热化学方程式是:CO(g) + H2O (g) = CO2(g) +H2(g)?△H=―41kJ/mol 。
本题难度:简单
|