|
�߿���ѧ֪ʶ���ܽᡶ������������ǿ����ϰ��2017�����°棩(��)
2017-07-18 02:31:07
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
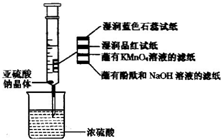
1��ѡ���� ����ͼ��ʾ����ע�����м�������Na2SO3�����壬������������Ũ���ᣨ�Բ��Ӵ�ֽ��Ϊ�����������й�˵����ȷ���ǣ�������
A��ʪ����ɫʯ����ֽ�ȱ�����ɫ
B��պ��KMnO4��Һ����ֽ��ɫ��֤����SO2��Ư����
C��ʪ��Ʒ����ֽ��ɫ��֤����SO2��Ư����
D��պ�з�̪��NaOH��Һ����ֽ��ɫ��֤����SO2��Ư����
| 
�ο��𰸣�A��SO2ֻ��ʹ���ָʾ����ɫ������ʪ�����ɫʯ����ֻֽ��죬��A����
B��SO2���л�ԭ�ԣ������ǿ�����Ե�KMnO4����������ԭ��Ӧ��KMnO4��Һ����ֽ��ɫ����B����
C��ʪ��Ʒ����ֽ��ɫ�����ֳ�SO2��Ư���ԣ���C��ȷ��
D��SO2Ϊ�������壬����NaOH��Һ��Ӧ�����κ�ˮ����Һ���Լ�������ɫ��ȥ��û������SO2��Ư���ԣ���D����
��ѡC��
���������
�����Ѷȣ�һ��
2������� �ⶨת����SO3��ת���ʿ�������ͼװ�ã�װ������ƿ�ڷ����Ļ�ѧ��Ӧ����ʽΪ��
Na2SO3��s��+H2SO4��85%��=Na2SO4+H2O+SO2������֪S03���۵���16.8�棬�е���44.8�棩
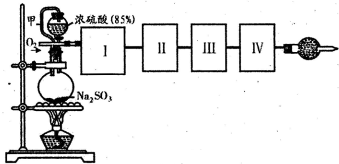
��1��װ���мܵ�������______��
��2������ʵ����Ҫ��Ӧ����I��II��III��IV�����Ӻ��ʵ�װ�ã������ͼA?Eװ����ѡ�����ʺ�װ�ò���������������Ŀո��У�I��II��III��IV�����ӵ�װ�÷ֱ���______
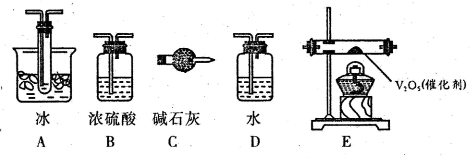
��3��ΪʹSO2�нϸߵ�ת���ʣ�ʵ���м��ȴ�����μ�Ũ�����˳���У�Ӧ��ȡ�IJ�����______�����ô�������ƿʱ��SO2��ת���ʻ�______?������ߡ��������䡱���͡�����
��4����һС����ʵ���з��֣�SO2����������������º���ʵ���������ԣ����ֲ��������������⣬�����Ʋ���ܵ�ԭ���Բ���������ԭ��______��ԭ��______?��ԭ��______
��5����SO2ͨ�뺬1mol�������Һ�У�������һ��ǿ���һ�����������6.02��1023������ת�ƣ���÷�Ӧ�Ļ�ѧ����ʽΪ______
��6����nmolNa2SO3��ĩ������Ũ������д�ʵ�飬����Ӧ����ʱ������ͨ��O2-��ʱ����װ��IV������?mg����ʵ����SO2��ת����Ϊ______�����ú�m��n�Ĵ���ʽ��д��
�ο��𰸣���1����ͼ��֪��Һ������ʱʹ��Һ©����ѹǿ��С��������Һ�����£�����װ���ܱ�֤��Һ©������ƿ������ѹǿ��ȣ������ʹҺ��˳�����£��ʴ�Ϊ��������˳�����£�
��2�������Һ�з�Ӧ���������л���ˮ��������I��Ӧѡ��Bװ��������ˮ��������ĸ��II��ѡE���ж�����������Ĵ�������S03���۵���16.8�棬�е���44.8�棬III��ѡA������ȴ��ʹ�������������������룬��IV��ѡ��Cװ��������δ��Ӧ��SO2���ʴ�Ϊ��BEAC��
��3���������һ�����¶��´�Ч���ã���Ӧ�ȼ��ȴ�����������ʱ��Ӧ���ʹ��죬���ɵIJ��ֶ�������δ��Ӧ��ͨ����Eװ�ã�����SO2��ת���ʽ��ͣ�
�ʴ�Ϊ���ȼ��ȴ����ٵ���Ũ������ͣ�
��4��SO2�����������������ΪNa2SO3�������������ƣ�Ҳ����ΪŨ�����Ũ�Ȳ�������Ӧ���ʱ������ʴ�Ϊ��Na2SO3���ʣ�Ũ�����Ũ�Ȳ�����
��5��SO2ͨ�뺬1mol�������Һ�У�������һ��ǿ���һ���������6.02��1023������ת�ƣ���ClԪ�صĻ��ϼ���+5�۽���Ϊ+4�ۣ��������غ㶨�ɿ�֪��Ӧ�Ļ�ѧ����ʽΪ
SO2+2HClO3�TH2SO4+2ClO2���ʴ�Ϊ��SO2+2HClO3�TH2SO4+2ClO2��
��6��IV������mg��Ϊδ��Ӧ��SO2�������������ʵ���Ϊm64mol��nmolNa2SO3��ĩ������Ũ���ᷴӦ����nmolSO2����ת����Ϊn-m64n��100%=64n-m64n��100%��
�ʴ�Ϊ��64n-m64n��100%��
���������
�����Ѷȣ�һ��
3��ѡ���� ����SO2���Ƿ����CO2���壬�ɲ��õķ����ǣ� ? ��
A��ͨ��Ʒ����Һ
B����ͨ��NaOH��Һ����ͨ������ʯ��ˮ
C��ͨ������ʯ��ˮ
D����ͨ��KMnO4������Һ����ͨ������ʯ��ˮ
�ο��𰸣�D
���������
�����Ѷȣ���
4��ѡ���� Ʈ��������ȼ��ʱ��������״Ʈ���������С�����׳��������������SO2��O2�Ӵ�ʱ��SO2�Ჿ��ת ��ΪSO3��ʹ������������ӣ�Ʈ����������ÿ�����
[? ]
A��������
B����ԭ��
C������
D��������
�ο��𰸣�CD
���������
�����Ѷȣ�һ��
5������� ��ͼ��ʵ������ͭƬ��Ũ������ȡSO2����֤�����ʵ�װ��ͼ�����Թܢ��м���һС��ͭƬ���ټ���3��5mL?Ũ���ᣬ�ô����ܵĵ������������Թܣ����ȣ������ɵ�����ͨ���Թܢ����Һ�У�
��1�����Թܢ��е���Һ����ɫʯ����Һ����Ӧһ��ʱ����Թܢ��п�����������______��
��2�����Թܢ��е���Һ��Ʒ����Һ����Ӧһ��ʱ�������������______����Ӧ��ֺ�ȡ���Թܢ��ھƾ����ϼ��ȣ�������������______��
��3��ʵ������У��Թܢ�ܿ���һ�Ž���NaOH��Һ������������______���йط�Ӧ�����ӷ���ʽΪ______��
�ο��𰸣�ͭ��Ũ�����ڼ����������ܷ�����������ͭ�Ͷ�������ˮ��
��1�����������ˮ��Ӧ���������ᣬ�������ܵ���������ƶ��������ӣ�������Һ�����ԣ���ɫʯ����Һ������ɫ��������Һ�ʺ�ɫ��
�ʴ�Ϊ����Һ�ʺ�ɫ��
��2�����������ܺ���ɫ����������ɫ���ʣ�����������ʹƷ����Һ��ɫ�����Զ����������Ư���ԣ������ɵ���ɫ���ʲ��ȶ�������ʱ��ָ�ԭ������ɫ��
�ʴ�Ϊ��Ʒ����Һ��ɫ����Һ�ָ���ɫ��
��3�����������ж������Բ���ֱ���ſգ���������������������ܺͼӦ�����κ�ˮ�������Թܢ�ܿ���һ�Ž���NaOH��Һ����������������δ��Ӧ��SO2���壬���ӷ���ʽΪSO2+2OH-=SO32-+H2O��
�ʴ�Ϊ������δ��Ӧ��SO2���壻?SO2+2OH-=SO32-+H2O��
���������
�����Ѷȣ�һ��
| 