| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《影响化学反应速率的因素》试题巩固(2017年最新版)(八)
参考答案:B 本题解析:由图象可知:同压下T2条件下NO2的体积分数大,故T1<T2,故D项错误;c点压强大于a点,故.a、c两点的反应速率:a<c,故A项错误;同压下,a点到b点,温度降低平衡正向移动,NO2的转化率增大故a<b ,B项正确;a、c两点c点压强大于a点,则c点NO2浓度大,故c点颜色深,故C项错误。 本题难度:困难 2、实验题 (16分)某学校研究性学习小组开展课题探究:
(2)对比实验①和④,可以研究 对化 学反应速率的影响,实验④中加入1 mL蒸馏水的目的是 。 探究课题Ⅱ.该小组查阅资料得知:C2O42-+MnO4-+H+→ CO2↑+Mn2++H2O(未配平),欲利用该反应测定某草酸钠(Na2C2O4)样品中草酸钠的质量分数。该小组称量1.34 g草酸钠样品溶于稀硫酸中,然后用0.200 mol・L-1的酸性高锰酸钾溶液进行滴定(其中的杂质不跟高锰酸钾和稀硫酸反应)。 (1)滴定前是否要滴加指示剂? (填“是”或“否”),请说明理由 。 (2)滴定时用 (填a或b)滴定管盛装KMnO4标准溶液。 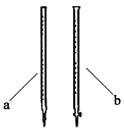 (3)达到终点时消耗了15.00 mL的高锰酸钾溶液,样品中草酸钠的质量分数为 。 参考答案:Ⅰ.(1)①和② (2分);① 和 ③ 本题解析:Ⅰ.(1)如果研究催化剂对化学反应速率的影响需有对照实验,因此选①和②;如果研究温度对化学反应速率的影响需要其他因素相同做对照实验,因此选① 和 ③;(2)①和④中浓度不同, 确保①和④组对比实验中c(KMnO4)不变,或确保溶液总体积不变。Ⅱ.(1)由于KMnO4本身是紫红色,无需再加指示剂;(2)KMnO4盛装在酸式滴定管中;(3) 本题难度:一般 3、选择题 对处于平衡状态的反应2A(g)+B(g) 参考答案:A 本题解析:增大反应物A的浓度,瞬间增大正反应的速率,但生成物的浓度瞬间不变,所以你反应速率不变,A正确;△H<0说明该反应的正反应是放热反应,所以升高温度影响的只是使平衡逆向移动,但是正逆反应都会瞬间同时增大,故B错误;反应中反应物和生成物均是气体,所以增大压强是反应物和生成物的浓度都瞬间增大,所以正逆反应速率都增大,C错误;加入催化剂不改变平衡,只是使正逆反应速率同等程度增大;故选A。 本题难度:一般 4、填空题 决定化学反应速率的主要因素是:______,其次外界条件如:______,______,______,______,等对化学反应速率也有一定的影响. 参考答案:影响反应速率的因素有内因和外因,内因是反应物本身的性质,为主要因素,外界因素有浓度、温度、压强、催化剂、固体的表面积以及溶剂等, 本题解析: 本题难度:一般 5、实验题 已知氯水中有如下平衡:Cl2+H2O 参考答案:(1)气体体积缩小,溶液呈浅黄绿色; 本题解析:正确分析出该装置中所发生的物理化学变化,然后运用外界条件对化学平衡移动的影响来解释。其中主要化学变化为:Cl2+H2O 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《二氧化硫》.. | |