微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列能达到实验目的是( )
A.用NaOH溶液除去CO2中混有的HCl气体
B.用分液漏斗分离四氯化碳和水的混合物
C.加入盐酸以除去硫酸钠中的少许碳酸钠杂质
D.配制一定浓度的氯化钾溶液1000mL,准确称取氯化钾固体,放入到1000ml的容量瓶中,加水溶解,振荡摇匀,定容
参考答案:B
本题解析:
本题难度:简单
2、选择题 下列实验设计、操作或实验现象正确的是( )
A.检验甲酸中是否混有甲酸甲酯,可向样品中加入足量NaOH溶液以中和HCOOH,再做银镜反应实验
B.向含有溴单质的溴苯中加入NaOH溶液,振荡静置后分液,以除去杂质溴
C.液态溴乙烷中加入AgNO3溶液观察有无淡黄色沉淀生成,以检验溴元素的存在
D.分离苯和苯酚的混合液,加入少量浓溴水,过滤,即可分离
参考答案:B
本题解析:
本题难度:一般
3、选择题 下图中,能顺利安全地达到实验目的的是
[? ]
A.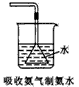
B.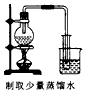
C.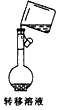
D.
参考答案:B
本题解析:
本题难度:一般
4、简答题 为了用实验的方法验证镁和铁的金属性强弱,学生甲和学生乙分别设计了两种不同的方法:
方案一:学生甲用水作试剂,比较镁和铁与水反应的情况
方案二:学生乙用稀盐酸作试剂,比较镁和铁与稀盐酸反应的情况
回答下列问题:
(1)以上两实验方案实验现象较为明显的是方案______
(2)学生乙在实验中取了一段镁条,投入稀盐酸中,现象不是十分明显,请分析原因______.
(3)学生丙另辟蹊径,仅用镁条、铁片与盐酸只进行一次实验也得出正确的结论(其它用品自选),学生丙用的是什么方法?______简述现象______.
参考答案:(1)常温下金属镁和水的反应不是很剧烈,金属铁和水不反应,但是二者均可以和盐酸反应,并且金属镁和酸反应产生氢气的速率快,剧烈,而金属铝不如镁剧烈,故答案为:方案二;
(2)在金属镁条的表面会生成一层致密的氧化物薄膜,阻止一些反应的进行,这样导致镁条投入稀盐酸中,现象不是十分明显,故答案为:镁的表面存在氧化膜;
(3)原电池中负极金属的活泼性一般是强于正极金属的活泼性的,这样让金属镁和铁做电极,让盐酸作电解质,会在金属铁电极表面产生气泡,所以金属铝是正极,镁条溶解,镁是负极,活泼性:金属镁强于金属铝,
故答案为:构成原电池的方法;镁条溶解,铁的表面有气泡.
本题解析:
本题难度:一般
5、选择题 下列实验能达到目的的是?
[? ]
A.在容量瓶中加一定体积的水,再加入浓硫酸配制准确浓度的稀硫酸
B.用稀硫酸和锌粒反应制氢气
C.用玻璃棒搅拌漏斗中的液体以加快过滤的速度
D.加入盐酸以除去硫酸钠中的少量碳酸钠杂质
参考答案:B
本题解析:
本题难度:简单