微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 实验室用如图所示装置分离CO2和CO气体并干燥。请完成(1)―(2)两个小题。
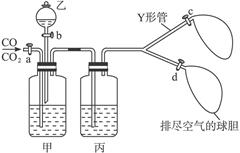
图3-9
(1)图中a为止水夹,b为分液漏斗的活塞,通过Y形管和止水夹c、d分别接两球胆。现装置内的空气已排尽。为使实验成功,甲、乙、丙分别盛放的溶液是(?)
A.NaHCO3饱和溶液、12 mol・L-1盐酸、18.4 mol・L-1 H2SO4
B.NaOH饱和溶液、2 mol・L-1 H2SO4、18.4 mol・L-1 H2SO4
C.Na2CO3饱和溶液、2 mol・L-1 H2SO4、NaOH饱和溶液
D.18.4 mol・L-1 H2SO4、NaOH饱和溶液、18.4 mol・L-1 H2SO4
(2)①打开a? ②打开b? ③打开c? ④打开d,为了使气体分离,下列打开止水夹(或活塞)的顺序正确的是(关闭的步骤省略,只要打开的步骤)(?)
A.①④②③? B.①②③④
C.②①③④? D.③④①②
参考答案:(1)B?(2)A
本题解析:根据本题中装置及提供的备选试剂,可初步分析其可以实现实验的目的的操作方法是:先用氢氧化钠吸收二氧化碳,浓硫酸干燥后收集CO;待CO收集完后,再将分液漏斗中的硫酸放下来,与吸收二氧化碳后转变成碳酸钠的溶液反应,重新产生二氧化碳,再用浓硫酸干燥、用球胆来收集二氧化碳,这样利用反应顺序差别,将二氧化碳与一氧化碳给分离开。
本题难度:一般
2、选择题 2003年诺贝尔化学奖授予美国科学家Peter Agre和Roderick Mackinnon以表彰他们在“水通道”和“离子通道”的研究成果。Mackinnon教授的研究内容主要是Na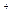 、K
、K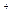 虽然体积很接近,但在生物体内呈现的差别却高达1万倍,他让科学家们观测到Na
虽然体积很接近,但在生物体内呈现的差别却高达1万倍,他让科学家们观测到Na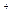 、K
、K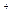 在进入离子通道前、通道中以及穿过通道后的状态,在医学应用上可为病人在“离子通道”中寻找具体的病因,并研制相应药物。下列关于钠、钾的说法正确的是(?)
在进入离子通道前、通道中以及穿过通道后的状态,在医学应用上可为病人在“离子通道”中寻找具体的病因,并研制相应药物。下列关于钠、钾的说法正确的是(?)
A.质钠的密度比钾的密度小
B.和钾在空气中燃烧的产物都是过氧化物
C.一小块钠投入盛5 mL澄清石灰水的试管里,可能观察到溶液变浑浊
D.和钾的合金〔w(K)=50%~80%〕熔点比钠和钾都高
参考答案:C
本题解析:本题以诺贝尔化学奖获得者的研究成果为背景命题,考查了金属钠、钾的性质和用途(新考纲增加知识点)及溶解度变化等知识点。详细的解答过程为:碱金属的密度总体上随原子序数增大而增大,但钠的密度反常(比钾大);钠在空气中燃烧的产物是过氧化钠,但钾在空气中燃烧的产物中还有超氧化钾;将钠投入澄清石灰水中会和水发生反应且放出热量,若石灰水是饱和的(氢氧化钙的溶解度随温度升高而减小),则会有少量Ca(OH)2析出来。
本题难度:简单
3、实验题 (10分)实验室有甲、乙两瓶无色溶液,其中一瓶是稀盐酸,另一瓶是碳酸钠溶液。为测定甲、乙两瓶溶液的成分及物质的量浓度,进行以下实验:
①量取25.00mL甲溶液,缓慢滴入乙溶液15.00mL,共收集到224mL(标准状况)气体
②量取15.00mL乙溶液,缓慢滴入甲溶液25.00mL,共收集到112mL(标准状况)气体。
(1)判断:甲是?溶液,乙是? ?溶液。
?溶液。
(2)写出中所发①生反应的离子方程式?。
(3)乙溶液的物质的量浓度是多少?
参考答案:(10分)
(1)甲:稀盐酸(2分);乙:碳酸钠(2分)
(2)CO32―+2H+→CO2↑+H2O(2分)
(3)1.0mol/L(4分)
本题解析:略
本题难度:一般
4、选择题 关于锂的结构和性质判断错误的是
①与水反应比钠剧烈?②原子半径小于钠?③有Li2O、Li2O2两种氧化物
④它的阳离子最外层电子数与钠的阳离子相同?⑤它是还原剂
A.③⑤
B.①②③
C.①③④
D.①③
参考答案:C
本题解析:①错,锂的金属性比钠弱,与水反应钠更剧烈;②正确,同主族元素从上到下,原子半径逐渐增大;③错,无Li2O2氧化物;④错,锂离子最外层只有2个电子,而钠的阳离子最外层有10个电子;它的阳离子最外层电子数与钠的阳离子不相同;⑤正确,锂的最外层只有一个电子,易失去电子,是还原剂;
本题难度:一般
5、选择题 通过观察和 合理推测,实验室中保存少量金属钠的正确方法是(?)
合理推测,实验室中保存少量金属钠的正确方法是(?)
A.保存在水中
B.保存在广口瓶中
C.用铝箔包裹,密封在广口瓶中
D.保存在煤油中
参考答案:D
本题解析:略
本题难度:简单