微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组离子能大量共存且溶液呈无色的是
[? ]
A.K+ Na+ OH- Cl-
B.Cu2+ Ba2+ NO3- Cl-
C.Na+ OH- Mg2+ Cl-
D.Ba2+ H+ NO3- OH-
参考答案:A
本题解析:
本题难度:一般
2、选择题 下列叙述或表示正确的是(?)
A.常温下pH均为3的醋酸和硫酸的水溶液,分别加水稀释100倍后,两种溶液的pH仍相同
B.氢氧化钙溶液中加入过量的碳酸氢钙溶液的离子方程式:Ca2+ + HCO3―+OH― = CaCO3 ↓+ H2O
C.Ksp反映了难熔电解质在水中的溶解能力,它的大小与浓度无关,与温度无关。
D.c(H+)=1×10-2 mol・L的溶液:Fe2+、Ba2+、N03-、Cl-不能大量共存。
参考答案:D
本题解析:A. 醋酸是弱酸,部分电离,C(CH3COOH)>C(H+)。当加谁呢稀释时,会使电离平衡向电离的方向移动,导致C(H+)又有所增加;硫酸是强酸,完全电离。加水稀释,C(H+)只是减小,所以常温下将pH均为3的醋酸和硫酸的水溶液,分别加水稀释100倍后,两种溶液的pH硫酸的大于醋酸的。错误。B.酸式盐与碱发生反应时要以不足量的物质为标准。氢氧化钙溶液中加入过量的碳酸氢钙溶液的离子方程式:Ca2+ +2OH―+2 HCO3―= CaCO3 ↓+ 2H2O+ CO32-。错误。C. Ksp反映了难熔电解质在水中的溶解能力,它的大小与浓度无关,与温度有关。错误。D.c(H+)=1×10-2 mol・L的溶液是酸性溶液这时:H+、Fe2+、N03-会发生离子反应而不能大量共存。正确。
本题难度:一般
3、选择题 常温下,下列各组离子在指定溶液中一定能大量共存的是
[? ]
A.pH=1的溶液中:Na+、Fe2+、NO3-、SO42-
B.c(OH-)= 10-12 mol/L的溶液中:NH4+、Al3+、NO3-、Cl-
C.由水电离的c(H+)=1×10-13 mol/L的溶液中:Ba2+、K+、Cl-、[Al(OH)4]-
D.能使淀粉碘化钾试纸显蓝色的溶液:K+、SO42-、S2-、SO32-
参考答案:B
本题解析:
本题难度:一般
4、选择题 下列在指定溶液中的各组离子,能够大量共存是(?)
A.无色溶液中: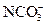 、Na+、Cl-、OH-
、Na+、Cl-、OH-
B.pH=11的溶液中:S2-、K+、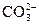 、Cl-
、Cl-
C.pH=1的溶液中:Fe2+、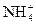 、Mg2+、
、Mg2+、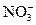
D.水电离的c(H+)=10-12 mol・L-1的溶液中:Fe3+、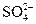 、K+、SCN-
、K+、SCN-
参考答案:B
本题解析:此题考查离子共存知识。
A项中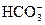 +OH-====
+OH-====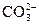 +H2O;B项中pH=11溶液中含有大量OH-,但S2-、K+、
+H2O;B项中pH=11溶液中含有大量OH-,但S2-、K+、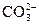 、Cl-均可存在;C项中pH=1溶液中含有大量H+,而
、Cl-均可存在;C项中pH=1溶液中含有大量H+,而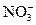 在H+存在时,可将Fe2+氧化成Fe3+,此项要求学生熟悉“
在H+存在时,可将Fe2+氧化成Fe3+,此项要求学生熟悉“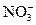 ”的氧化特点;D项“水电离的c(H+)=10-12 mol・L-1”说明溶液可显强酸性,也可显强碱性,所给离子组必须在两种可能环境中均大量存在。此项中Fe3++3OH-====Fe(OH)3↓;H++SCN-====HSCN,但最主要是:Fe3++3SCN-====Fe(SCN)3不能大量共存。
”的氧化特点;D项“水电离的c(H+)=10-12 mol・L-1”说明溶液可显强酸性,也可显强碱性,所给离子组必须在两种可能环境中均大量存在。此项中Fe3++3OH-====Fe(OH)3↓;H++SCN-====HSCN,但最主要是:Fe3++3SCN-====Fe(SCN)3不能大量共存。
本题难度:简单
5、选择题 现将等物质的量的CuSO4、FeCl3、Zn放入盛有水的烧杯中充分反应,所得溶液中除SO42-、Cl-外,还含有的金属阳离子是?
A.Zn2+、Cu2+、Fe3+
B.Zn2+、Cu2+、Fe2+
C.Zn2+、Fe2+、Cu2+、Fe3+
D.Zn2+、Fe3+
参考答案:B
本题解析:等物质的量的CuSO4、FeCl3、Zn放入盛有水的烧杯中充分反应,由于氧化性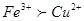 其反应离子方程式为:第一步反应为:
其反应离子方程式为:第一步反应为: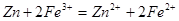 ?;第二步反应为:
?;第二步反应为: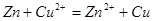 ;所以,所得溶液中除SO42-、Cl-外,还含有的金属阳离子Zn2+、Cu2+、Fe2+
;所以,所得溶液中除SO42-、Cl-外,还含有的金属阳离子Zn2+、Cu2+、Fe2+
本题难度:一般