|
|
|
�߿���ѧ֪ʶ���������������ת��������ǿ����ϰ��2017��Ѻ��棩(��)
2017-07-18 02:47:00
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� (15��)̼�͵��Ļ���������������������������ء�
��1����һ���¡������ܱ������з�����Ӧ�� Ni(s)+4CO(g)  ?Ni(CO)4(g)�� ?Ni(CO)4(g)��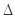 H<0�����ø÷�Ӧ���Խ�����ת��Ϊ���ȴ�99��9���ĸߴ������Ը÷�Ӧ��˵����ȷ����?? H<0�����ø÷�Ӧ���Խ�����ת��Ϊ���ȴ�99��9���ĸߴ������Ը÷�Ӧ��˵����ȷ����??
(����ĸ���)��
A������Ni���������CO��ת���ʣ�Ni��ת���ʽ���
B����С�����ݻ���ƽ�����ƣ�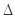 H��С H��С
C����Ӧ�ﵽƽ�����CO�ٴδﵽƽ��ʱ��CO�������������
D����4vNi(CO)4=v(CO)ʱ�������л�������ܶȲ���ʱ������˵����Ӧ�Ѵﻯѧƽ��״̬
| ��2��CO������Ӧ������������ж���Ϊ��ֹ�������ж�����ҵ�ϳ���SO2��CO��������������ת��Ϊ������
��֪��C(s)+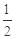 O2(g)==CO(g)? O2(g)==CO(g)?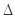 H= -Q1 kJ��mol-1 H= -Q1 kJ��mol-1
C(s)+ O2(g)==CO2(g)?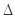 H= -Q2 kJ��mol-1 H= -Q2 kJ��mol-1
S(s)+O2(g)==SO2(g)?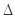 H= -Q3 KJ��mol-1 H= -Q3 KJ��mol-1
��SO2(g)+2CO(g)==S(s)+2CO2(g)?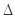 H=?kJ��mol-1�� H=?kJ��mol-1��
��3������������ɱ�һ����̼��ԭ���ɽ������ʺͶ�����̼��ͼ��1�������ֽ��������Cr2O3��SnO2��PbO2��Cu2O)��һ����̼��ԭʱ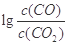 ���¶ȣ�t���Ĺ�ϵ����ͼ�� ���¶ȣ�t���Ĺ�ϵ����ͼ��
700oCʱ���������ѱ���ԭ�Ľ�����������??(�ѧʽ)����һ����̼��ԭ�ý���������ʱ������Ӧ����ʽϵ��Ϊ��������ȣ��÷�Ӧ��ƽ�ⳣ��(K)��ֵ���� ??��
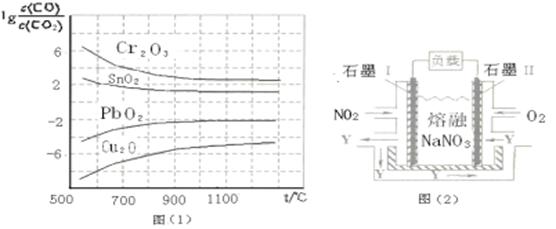
��4��NO2��O2������NaNO3������ȼ�ϵ�أ���ԭ������ͼ��2����ʾ���õ����ʹ�ù�����ʯīI�缫������������Y����缫��ӦʽΪ?��
����ȼ�ϵ��ʹ��һ��ʱ����ռ���20mol Y������������Ҫ���ı�״�������������Ϊ?L��
�ο��𰸣���15�֣�
��1��C?��3�֣�
��2����(2Q2��2Q1��Q3) kJ��mol��1��2Q1��2Q2��Q3��kJ��mol��1?��3�֣�
��3��Cr2O3?��3�֣�?10��12?��2�֣�
��4��NO2��NO3����e����N2O5?��2�֣�? 224��2�֣�
�����������1��A��Ni�ǹ��壬Ũ��Ϊ�������ı�������ƽ����Ӱ�죬��Ӧ���ת���ʲ��䣬����B��һ���¶��¸����Ļ�ѧ����ʽ�ġ�H��������ƽ���ƶ����ı䣬ֻ�뷽��ʽ����д��ʽ�йأ�����C�����������Ϊ���º��ݡ�Ni�ǹ���������ӦΪ���������С�ķ�Ӧ�����Է�Ӧ�ﵽƽ������CO���൱���ں��º�ѹ�����´�ƽ����ּ�ѹ��ƽ�����ƣ�CO��ת������ߣ�ƽ���������������ͣ���ȷ��D�����ʹ�ϵδ˵�������棬�����ж��Ƿ��Ѵ�ƽ�⣬����
��2����֪��������Ӧ�ֱ��â٢ڢ۱�ʾ�����ø�˹���ɿɵã�SO2��g��+2CO��g���TS��s��+2CO2��g�����ɡ��١�2+�ڡ�2-�۵õ������H=-��2Q2-2Q1-Q3�� kJ?mol-1��2Q1-2Q2+Q3��kJ?mol-1
��3��700��ʱ��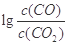 Խ����KԽС��˵����Ӧ���еij̶�С������������Խ�ѱ���ԭ������ͼ��Cr2O3��Ӧ�� Խ����KԽС��˵����Ӧ���еij̶�С������������Խ�ѱ���ԭ������ͼ��Cr2O3��Ӧ��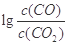 �������Cr2O3���ѱ���ԭ����ʱCr2O3��Ӧ�� �������Cr2O3���ѱ���ԭ����ʱCr2O3��Ӧ��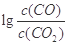 =4����c(CO2)/c(CO)=10-4�����Cr2O3��CO��Ӧ�Ļ�ѧ����ʽCr2O3+3CO =4����c(CO2)/c(CO)=10-4�����Cr2O3��CO��Ӧ�Ļ�ѧ����ʽCr2O3+3CO 2Cr+3CO2���ɵ�K="[" c(CO2)/c(CO)]3=10-12�� 2Cr+3CO2���ɵ�K="[" c(CO2)/c(CO)]3=10-12��
��4��ʯīI�缫��ͨ��NO2��Ϊ�����������ĵ缫��ӦΪ��NO2+NO3--e-=N2O5�����ݵ���ܷ�Ӧ4NO2+O2=2N2O5���ռ���20molN2O5������O2Ϊ10mol����״�������Ϊ224L��
�����Ѷȣ�һ��
2��ѡ���� ���б仯�������ȷ�Ӧ���ǣ�
��Һ̬ˮ����?�ڽ��������ȱ�Ϊ��ɫ��ĩ?��Ũ����ϡ��?������طֽ�������
����ʯ����ˮ��Ӧ������ʯ��?��I2��I��I?��H��Cl��HCl?��������ԭ����ͭ
A���٢ڢܢ�
B���ڢܢݢ�
C���٢ܢݢ�
D���ڢܢ�
�ο��𰸣�D
���������
��ȷ�𰸣�D
��Һ̬ˮ�������������仯?�ڽ��������ȱ�Ϊ��ɫ��ĩ���ֽⷴӦ������?��Ũ����ϡ�ͣ������仯Ϊ��������?������طֽ�����������ѧ�仯������
����ʯ����ˮ��Ӧ������ʯ�ң���ѧ�仯������?��I2��I��I ���Ȣ�H��Cl��HCl ���Ȣ�������ԭ����ͭ�����ȡ�
�����Ѷȣ�һ��
3��ѡ���� ��ӦA(g)+B(g) C(g) +D(g)�����е������仯��ͼ��ʾ��������˵����ȷ���� C(g) +D(g)�����е������仯��ͼ��ʾ��������˵����ȷ����
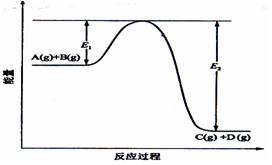
A���÷�Ӧ�Ƿ��ȷ�Ӧ
B����Ӧ��ϵ�м�������Է�Ӧ����Ӱ��
C������Ӧ�ﵽƽ��ʱ�������¶ȣ�A��ת���ʼ�С
D���ı�ѹǿ��Ӵ����Է�Ӧ��Ӱ��ԭ����ͬ��������ʹƽ�ⷢ���ƶ�
�ο��𰸣�AC
�����������
�����Ѷȣ���
4��ѡ���� ����˵���У���ȷ����
[?]
A���ڻ�ѧ��Ӧ�����У��������ʱ仯��ͬʱ��һ�����������仯
B��ȼ������ָ1mol����ȼ�����ų�������
C����Ӧ��������������ڷ�Ӧ���������ʱ����Ӧ���ȣ���H��0
D����H�Ĵ�С���Ȼ�ѧ����ʽ�ļ���ϵ����
�ο��𰸣�C
���������
�����Ѷȣ���
5������� ��10�֣�����ƽ�����ʢ��ǿ��ԭ��Һ̬�£�N2H4����ǿ������Һ̬˫��ˮ�������ǻ�Ϸ�Ӧʱ������������������ˮ���������ų��������ȡ���֪0.4molҺ̬����������Һ̬˫��ˮ��Ӧ�����ɵ�����ˮ�������ų�QKJ��������
��1����Ӧ���Ȼ�ѧ����ʽΪ?
��2���˷�Ӧ���ڻ���ƽ������ͷŴ����ȺͿ��ٲ������������⣬����һ���ܴ���ŵ���?
��3������������ʮ����, ���������䡱������֮һ.
���������䡱�еġ�������ָ(? )
A��ˮú��
B���ѽ���
C����Ȼ��
D����ʯ��
|
(4)2001��2��24��,�������̨����:�����������Ŀ����������,��ʯ��ׯ��.����Ҫ�����ڰ�Ǩһ���������ŷŵĹ����ʹ���ʹ��ȼ��ȼ��,������SO2�ͷ۳����ŷ�,�ر���ʹ��������Ļ���������,�ŷ���Ⱦֵ���.��֪1g������ȫȼ��������̬ˮʱ�ų�����50.125KJ.��д������ȼ�յ��Ȼ�ѧ����ʽ
?
�ο��𰸣�
�����������
�����Ѷȣ���
 O2(g)==CO(g)?
O2(g)==CO(g)?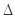 H= -Q1 kJ��mol-1
H= -Q1 kJ��mol-1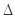 H= -Q2 kJ��mol-1
H= -Q2 kJ��mol-1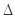 H= -Q3 KJ��mol-1
H= -Q3 KJ��mol-1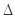 H=?kJ��mol-1��
H=?kJ��mol-1��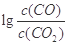 ���¶ȣ�t���Ĺ�ϵ����ͼ��
���¶ȣ�t���Ĺ�ϵ����ͼ��