��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���ڡ�������ѧ��־���������й���ѧ���Զ�����̼Ϊ̼Դ��������Ϊ��ԭ������470�棬80MPa�ºϳɳ����ʯ��������Զ���壮����˵������ȷ���ǣ�������
A���ɶ�����̼�ϳɽ��ʯ�ǻ�ѧ�仯
B���˷�Ӧ�н��ʯ����������
C�����ʯ��̼��һ��ͬ��������
D���˷�Ӧ����Ԫ�ط���������Ӧ
�ο��𰸣�A��������̼Ϊ̼Դ��������Ϊ��ԭ������470�棬80MPa�ºϳɳ����ʯ�Ĺ����������������ɵı仯���̣����ڻ�ѧ�仯����A��ȷ��
B��������̼Ϊ̼Դ��������Ϊ��ԭ������470�棬80MPa�ºϳɳ����ʯ�Ĺ��̣���Ԫ�ػ��ϼ����ߣ�̼Ԫ�ػ��ϼ������ͣ����ʯ�ǻ�ԭ�����B����
C�����ʯ��ʯī������ϩ��ͬ��Ԫ����ɵ��������ʲ�ͬ����ѧ�������Ƶ�CԪ�صIJ�ͬ���ʣ���Ϊͬ�������壬��C��ȷ��
D��������̼Ϊ̼Դ��������Ϊ��ԭ������470�棬80MPa�ºϳɳ����ʯ�Ĺ��̣���Ԫ�ػ��ϼ����ߣ����ϼ�����Ԫ���ڷ�Ӧ�б�����������������Ӧ����D��ȷ��
��ѡB��
���������
�����Ѷȣ�һ��
2������� ͭ������ϡ���ᷴӦ��Ҳ����Ũ���ᷴӦ����ͭ��һ��Ũ�����ᷴӦʱ���ɽ�����ʽ��ʾΪ��Cu+HNO3��Cu��NO3��2+NO��+NO2��+H2O?������ʽδ��ƽ��
��1�������ڸ÷�Ӧ�е�������______���÷�Ӧ�Ļ�ԭ������______��
��2��0.3mol?Cu��������ȫ�ܽ��Cuʧȥ�ĵ�������______?��������õ���NO��NO2���ʵ�����ͬ����μӷ�Ӧ����������ʵ�����______��������ˮ���ռ���Щ���壬�ɵñ�״���µ��������______��
��3������μӷ�Ӧ��Cu��HNO3�����ʵ���֮����3��10��д������ƽ�÷�Ӧ�����ӷ���ʽ______��
��4�����û�жԸ÷�Ӧ�е�ijЩ���ʵı�����������ʽ���ܵ���ƽϵ���������飮ԭ����______��
�ο��𰸣���1���ڸ÷�Ӧ�����ᷴӦ���������Σ���������NԪ�صĻ��ϼ۽��ͣ������������������ڷ�Ӧ�б���ԭ�����Ӧ�IJ���NO��NO2Ϊ��ԭ���
�ʴ�Ϊ�����������NO��NO2��
��2���÷�Ӧ��CuԪ����0�����ߵ�+2�ۣ���ʧȥ�ĵ���Ϊ0.3mol����2-0����NAmol-1=0.6NA����
��NO�����ʵ���Ϊn���õ���NO��NO2���ʵ�����ͬ��
�ɵ����غ��֪��0.3mol��2=n����5-2��+n����5-4����
���n=0.15mol��
��Nԭ���غ��֪��������������Ϊ0.15mol+0.15mol=0.3mol��
��Cu��NO3��2��֪�������Ե�����Ϊ0.3mol��2=0.6mol��
��μӷ�Ӧ����������ʵ�����0.3mol+0.6mol=0.9mol��
��3NO2+H2O�T2HNO3+NO��֪��0.15molNO2��ˮ��Ӧ����0.05molNO��
������ˮ���ռ���Щ���壬�������ΪNO�������ʵ���Ϊ0.15mol+0.05mol=0.2mol��
�ڱ�״���£���������Ϊ0.2mol��22.4L/mol=4.48L���ʴ�Ϊ��0.6NA��0.9mol��4.48L��?
��3��Cu+HNO3��Cu��NO3��2+NO��+NO2��+H2O�У��μӷ�Ӧ��Cu��HNO3�����ʵ���֮����3��10��
��3Cu+10HNO3��3Cu��NO3��2+xNO��+yNO2��+5H2O��
�ɵ����غ㼰Nԭ���غ�ɵã�
���������
�����Ѷȣ�һ��
3������� �����������Ԫ�أ��纬�������Ӱ�������֬��Ĵ�л����������������ж����йغ�����������ת����ϵ���£�
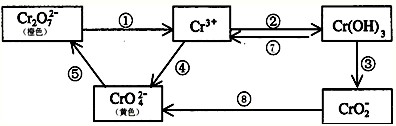
�ش��������⣺
��1������ת����ϵ������������ԭ��Ӧ����______�����ţ���������Ҫʹ������������______�����ţ���
��2����Ӧ���ǿ��淴Ӧ����Na2CrO4��Һ�м���ϡ���ᣬ��Һ�ɻ�ɫ��ɳ�ɫ��д���÷�Ӧ�����ӷ���ʽ��______��
��3����ͼʾ��Ϣ��֪����һ�ֺ��������������ԣ�д���û�������NaOH��Һ��Ӧ�����ӷ���ʽ��______��
��4����ҵ�ϴ�����Cr2O72-�ķ�ˮʱ��һ�㽫�綾��Cr2O72-ת��ΪCr3+����̼Ϊ����������������������NaCl��Cr2O72-�����Է�ˮ��д���缫��Ӧ����Һ�н��еķ�Ӧ�����ӷ���ʽ������______������______��Һ��______��
��5����֪Ag2CrO4��AgCl��Ksp�ֱ�Ϊ9.0��10-12��1.56��10-10��������ͬŨ�ȵ�Na2CrO4��NaCl�Ļ����Һ����μ�����������Һ���������ɵij�����______��
�ο��𰸣���1����������ת���У�����CrԪ�صĻ��ϼ۽��ͣ��ܢ���CrԪ�صĻ��ϼ����ߣ���٢ܢ�����������ԭ��Ӧ���Ңܢ�����Ҫ������������
�ʴ�Ϊ���٢ܢࣻ�ܢࣻ
��2����Na2CrO4��Һ�м���ϡ���ᣬ��Һ�ɻ�ɫ��ɳ�ɫ��ת���ݿ�֪�����������ӷ�ӦΪ2CrO42-+2H+

?Cr2O72-+H2O��
�ʴ�Ϊ��2CrO42-+2H+

?Cr2O72-+H2O��?
��3��ת��ͼ��ֻ�����������������������ƣ������������������ԣ�����Ӧ�����ӷ�ӦΪCr��OH��3+OH-=CrO2-+2H2O��
�ʴ�Ϊ��Cr��OH��3+OH-=CrO2-+2H2O��?
��4��������������������ӦΪFe-2e=Fe2+����Һ�е�������H+�������ŵ磬��������ӦΪH++2e=H2�������������������Ӿ��л�ԭ�ԣ���
Cr2O72-����������ԭ��Ӧ��Cr2O72-ת��ΪCr3+������Һ�з��������ӷ�ӦΪ6Fe2++Cr2O72-+14H+�T6Fe3++2Cr3++7H2O��
�ʴ�Ϊ��Fe-2e=Fe2+��H++2e=H2����6Fe2++Cr2O72-+14H+�T6Fe3++2Cr3++7H2O������?
��5��Ag2CrO4��AgCl��Ksp�ֱ�Ϊ9.0��10-12��1.56��10-10��������ͬŨ�ȵ�Na2CrO4��NaCl�Ļ����Һ����μ�����������Һ��
��Na2CrO4��NaCl��Ũ�ȶ�Ϊ1mol/L��
Ag2CrO4����ʱ��Ҫ��c��Ag+��=
���������
�����Ѷȣ�һ��
4��ѡ���� ���б仯�У�������뻹ԭ������ʵ�ֵ��ǣ�������
A��MnO2��Mn2+
B��Zn��Zn2+
C��H2��H2O
D��CuO��CuCl2
�ο��𰸣�A��MnO2��Mn2+����Ԫ�صõ��ӻ��ϼ۽��ͣ����Զ�����������������������뻹ԭ������ʵ�֣���A��ȷ��
B��Zn��Zn2+��пʧ���ӻ��ϼ����ߣ�����п����ԭ���������������������ʵ�֣���B����
C��H2��H2O����Ԫ��ʧ���ӻ��ϼ����ߣ�������������ԭ���������������������ʵ�֣���C����
D��CuO��CuCl2��ͭԪ�ػ��ϼ۲��䣬���Բ���������ԭ��Ӧ����D����
��ѡA��
���������
�����Ѷȣ�һ��
5��ѡ���� �Է�ӦCaH2+2H2O=Ca��OH��2+2H2������CaH2��H��-1�ۣ������ж���ȷ���ǣ�������
A��H2ֻ����������
B���õ���ԭ�Ӻ�ʧ����ԭ�ӵĸ�����Ϊ2��1
C��CaH2�õ���
D��H2O��������
�ο��𰸣�D
���������������A���ɷ�Ӧ��֪�����������뻹ԭ��Ӧ��Ϊ��������A����
B���õ��Ӻ�ʧ���ӵ�ԭ�Ӷ���Hԭ�ӣ��ҵõ��Ӻ�ʧ���ӵ�Hԭ�Ӹ�����ȣ�Ϊ1��1����B����
C��CaH2��HԪ��Ϊ-1�ۣ��ڷ�Ӧ��ʧ���ӣ���C����
D��H2O��HԪ��Ϊ+1�ۣ��ڷ�Ӧ�еõ��ӻ��ϼ۽��ͣ�����ˮ������������D��ȷ��
���Դ�ѡD
�����Ѷȣ���