微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在原子的第n电子层中,当它属于最外电子层时,最多容纳的电子数目与(n-1)层相同,当它属于次外层时,最多容纳的电子数比(n+1)层多容纳10个电子,则此电子层是( )
A.K层
B.L层
C.M层
D.N层
参考答案:C
本题解析:
本题难度:简单
2、选择题 下列有关物质结构的表述正确的是
[? ]
A.次氯酸的电子式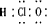
B.二氧化硅的分子式SiO2
C.硫原子的最外层电子排布式3s23p4
D.钠离子的结构示意图
参考答案:C
本题解析:
本题难度:简单
3、选择题 同种元素的原子和离子,一定具有相同的( )
A.质子数
B.电子数
C.电子层数
D.最外层电子数
参考答案:A
本题解析:
本题难度:简单
4、选择题 下列有关说法正确的是( )
A.原子的最外层有两个电子的元素都在第ⅡA族
B.第ⅠA族元素都是典型的金属元素
C.氟、氯、氧、氮四种元素都是第ⅦA族的元素
D.第三周期的元素的原子核外都有三个电子层
参考答案:D
本题解析:
本题难度:一般
5、填空题 下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素
试回答下列问题:
(1)表中第一电离能最小的是______(填字母,下同),第一电离能最大的是______.c、d、e三种元素的第一电离能由大到小的顺序是______,它们与a元素形成的最简单化合物的热稳定性由强到弱的是______(填化学式).
(2)第三周期中由电负性最大的元素与电负性最小的元素组成的化合物化学式是______.
(3)表中基态原子的未成对电子数最多的元素是______,其二价阳离子的外围电子排布式是______.
(4)写出由a、d、e三种元素组成的一种离子化合物的化学式______,并用离子方程式来说明其水溶液显酸性的原因______.
参考答案:(1)同一周期自左而右,第一电离能呈增大的趋势,同主族自上而下,第一电离能逐渐降低,故第一电离能最小的应在周期表的左下方,为n元素(即K元素),第一电离能最大的元素应在周期表的右上方,但稀有气体的第一电离能最大为m元素(即Ar元素);由元素在周期表中的位置可知,c、d、e三种元素分别为C、N、O元素,N元素原子的2p能级处于半满稳定状态,能量较低,第一电离能高于同周期相邻的元素,故三种元素的第一电离能由大到小的顺序是d>e>c;a为H元素,三者与a形成的化合物为氢化物,同周期自左而右,非金属性增强,非金属性O>N>C,非金属性越强,氢化物越稳定,故氢化物稳定性H2O>NH3>CH4.
故答案为:n,m,d>e>c,H2O>NH3>CH4.
(2)同周期自左而右,电负性增大,故第三周期中电负性最大的元素是Cl,电负性最小的元素是Na,二者形成的物质化学式为NaCl.
故答案为:NaCl.
(3)表中基态原子可以形成+2离子,属于金属,未成对电子数最多,故为过渡元素中的o(Fe元素),Fe元素核外电子排布为1s22s22p63s23p63d64s2,故Fe2+的外围电子排布式为3d6.
故答案为:o(Fe元素);3d6.
(4)由元素在周期表中的位置可知,a为H元素、d为N元素、e为O元素,三种元素组成的一种离子化合物为NH4NO3,铵根离子水解NH4++H2O

NH3?H2O+H+,使溶液呈酸性.
故答案为:NH4NO3;NH4++H2O

NH3?H2O+H+.
本题解析:
本题难度:一般