微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用相应化学用语回答下列问题:
族周期
| IA
| ?
| 0
|
1
| ①
| ⅡA
| ⅢA
| ⅣA
| ⅤA
| ⅥA
| ⅦA
| ?
|
2
| ?
| ?
| ?
| ②
| ③
| ④
| ?
| ?
|
3
| ⑤
| ?
| ⑥
| ⑦
| ?
| ⑧
| ⑨
| ?
|
(1)画出表中形成化合物种类最多元素的原子结构示意图?;写出它与原子半径最小的原子形成10电子且为正四面体结构的化合物的电子式_________,用电子式表示⑤和⑧形成化合物的过程________________________________________。
(2)④⑤⑧形成的简单离子半径由大到小的顺序为_______________(填离子符号);③⑦⑨的最高价氧化物对应水化物的酸性由强到弱的顺序为____(填化学式)。
(3)⑤和⑨形成化合物的晶体类型为__________。
(4)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是___________(填化学式),写出它与⑤的最高价氧化物对应水化物发生反应的离子方程式__________。
(5)X、Y由①②④中的两种或三种元素组成。X的溶液能与小苏打反应产生Y,若X是其所属系列中最简单的分子,且相对分子质量为46,则X的名称为?,写出X溶液与小苏打反应的化学方程式为_______________。
参考答案:(1) (1分);
(1分);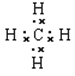 (1分);
(1分);
 (1分);
(1分);
(2)S2->O2->Na+(1分);HClO4>HNO3>H2SiO3(1分)?(3)离子晶体(1分)
(4)Al2O3(1分) ;Al2O3+2OH-=2AlO- 2+H2O(2分)
(5)甲酸(1分);HCOOH+NaHCO3= HCOONa +CO2↑+H2O(2分)
本题解析:根据元素①~⑨在表中的位置可知,它们分别是H、C、N、O、Na、Al、Si、S、Cl。
(1)形成化合物种类最多元素是碳元素,碳元素的原子序数是6,其原子结构示意图为 ;原子半径最小的是氢元素,因此它与原子半径最小的原子形成10电子且为正四面体结构的化合物是甲烷,其电子式为
;原子半径最小的是氢元素,因此它与原子半径最小的原子形成10电子且为正四面体结构的化合物是甲烷,其电子式为 ;⑤和⑧形成化合物是硫化钠,含有离子键的离子化合物,其形成过程可表示为
;⑤和⑧形成化合物是硫化钠,含有离子键的离子化合物,其形成过程可表示为 。
。
(2)④⑤⑧形成的简单离子分别是O2-、Na+、S2-,离子的核外电子层数越多离子半径越大。核外电子排布相同的微粒其离子半径随原子序数的增大而减小,所以④⑤⑧形成的简单离子半径由大到小的顺序是S2->O2->Na+。非金属性越强,最高价氧化物对应水化物的酸性越强,③⑦⑨三种元素的非金属性强弱顺序是Cl>N>Si,其最高价氧化物对应水化物的酸性由强到弱的顺序为HClO4>HNO3>H2SiO3。
(3)⑤和⑨形成化合物是NaCl,其晶体类型为离子晶体。
(4)不溶于水,但既能与强酸又能与强碱反应的是Al2O3。钠的最高价氧化物对应水化物是氢氧化钠,和氧化铝反应的离子方程式为Al2O3+2OH-=2AlO- 2+H2O。
(5)X的溶液能与小苏打反应产生Y,这说明X的酸性强于碳酸的。又因为X是由H、C、O元组成,如果X是其所属系列中最简单的分子,且相对分子质量为46,则X一定是甲酸,与碳酸氢纳反应的化学方程式为HCOOH+NaHCO3= HCOONa +CO2↑+H2O。
本题难度:一般
2、填空题 (16分)X、Y、Z三种短周期元素,其单质在常温下均为无色气体,它们的原子序数之和为16。在适当条件下三种单质两两化合,可发生如右图所示变化。己知l个B分子中含有Z元素的原子个数比C分子中含有Z元素的原子个数少1个。请回答下列问题:
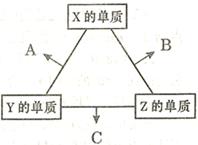 ?
?
(1)由 X、Y、Z三种元素共同组成的三种不同种类的常见化合物的化学式为?,相同浓度上述水溶液中由水电离出的c(H+)最小的是?(填写化学式)。
(2)Allis-Chalmers制造公司发现可以用C作为燃料电池的燃料,以氢氧化钾溶液为介质,反应生成对环境无污染的常见物质,试写出该电池负极的电极反应式?,溶液中OH-向?极移动(填“正”或“负”)。
(3)Z分别与X、Y两元素可以构成18个电子分子甲和乙,其分子中只存在共价单键,常温下甲、乙均为无色液体,甲随着温度升高分解速率加快。
①乙能够将CuO还原为Cu2O,已知每lmol乙参加反应有4mole- 转移,该反应的化学方程式为?。
②将铜粉末用10%甲和3.0mol?L-1H2SO4混合溶液处埋,测得不同温度下铜的平均溶解速率如下表:
温度(℃)
| 20
| 30
| 40
| 50
| 60
| 70
| 80
|
铜的平均溶解速率
(×10-3mol?L-1・min-1)
| 7.34
| 8.01
| 9.25
| 7.98
| 7.24
| 6.73
| 5.76
|
由表中数据可知,当温度高于40℃时,铜的平均溶解速率随着温度的升高而下降,其主要原因是?
_____________________________________________________。
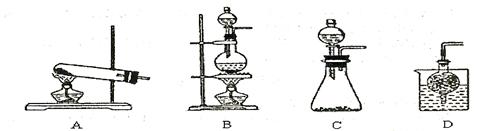
③实验室可用甲作试剂取X的单质,发生装置可选用下图中的?(填装置代号)。
参考答案:(1)HNO3、NH4NO3、NH3・H2O (3分)? HNO3?(1分)
(2)4NH3 + 12OH - 12e- =2N2 + 12H2O?(3分)?负(2分)
(3)①N2H4 + 4CuO = N2↑ + 2Cu2O + 2H2O(3分)
②高于40℃后,H2O2的分解速率加快,c(H2O2)降低,使铜的溶解速率减慢 (2分) ③C (2分)
本题解析:X、Y、Z三种短周期元素,其单质在常温下均为无色气体,短周期中形成无色气体单质的只有H2、N2、O2(稀有气体除外),H、N、O原子序数之和为16,故三种元素为H、N、O,三种气体单质相互反应生成H2O、NH3、NO,一个B分子中含有的Z元素的原子个数比一个C分子中少一个,则B为H2O,C为NH3,Z为氢元素.由关系图可知:Z单质与X单质反应生成B(H2O),故X为氧元素;Z单质与Y单质反应生成C(NH3),故Y为氮元素;所以A为NO,则:
(1)由 X、Y、Z三种元素共同组成的三种不同种类的常见化合物一般是酸碱盐,因此化学式分别为HNO3、NH4NO3、NH3・H2O。硝酸和氨水抑制水的电离,硝酸铵水解促进水的电离。硝酸是一元强酸,氨水是一元弱碱,因此相同浓度上述水溶液中由水电离出的c(H+)最小的是HNO3。
(2)原电池中负极失去电子,正极得到电子,因此在该燃料电池中氨气在负极通入,若以氢氧化钾溶液为介质,反应生成对环境无污染的常见物质,该物质应该是氮气和水,因此该电池负极的电极反应式4NH3 + 12OH - 12e- =2N2 + 12H2O。原电池中阳离子向正极移动,阴离子向负极移动,所以溶液中OH-向负极移动。
(3)Z分别与X、Y两元素可以构成18个电子分子甲和乙,其分子中只存在共价单键,常温下甲、乙均为无色液体,甲随着温度升高分解速率加快,所以甲是双氧水,乙是N2H4。
①乙能够将CuO还原为Cu2O,已知每lmol乙参加反应有4mole- 转移,由于N2H4中氮元素的化合价是-2价,这说明在反应中氮元素化合价升高2个单位,因此其氧化产物是氮气,所以该反应的化学方程式为N2H4 + 4CuO = N2↑ + 2Cu2O + 2H2O。
②由于双氧水不稳定,受热易分解,因此高于40℃后,H2O2的分解速率加快,c(H2O2)降低,使铜的溶解速率减慢。
③在催化剂的作用下双氧水分解生成氧气和水,反应不需要加热,因此选择装置是C。
本题难度:一般
3、选择题 下列物质中所有原子都满足最外层为8电子结构的是
A.H2O
B.AlCl3
C.SF6
D.CO2
参考答案:D
本题解析:只要元素的化合价的代数和与最外层电子数之和满足8,则就满足8电子稳定结构。所以选项D是正确的。答案选D。
本题难度:一般
4、填空题 (8分)下表列出了①~⑥六种元素在元素周期表中的位置。
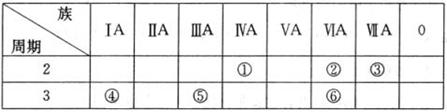
请回答下列问题:
(1)①、②、③三种元素相比较,非金属性最强的是__ __(填写元素符号);
(2) ②、⑥两种元素的原子半径大小为:② ⑥(填“<”或“>”);;
(3) 元素①的原子结构示意图??;?
(4)④、⑤两种元素的最高价氧化物对应的水化物在溶液中相互反应的离子方程式是
______________?____________。
参考答案:(1)F (2)<(3)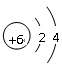 (4)Al(OH)3+OH-=AlO2-+2H2O
(4)Al(OH)3+OH-=AlO2-+2H2O
本题解析:考查元素周期表的结构和元素周期律的应用。根据元素在周期表中的位置可判断①~⑥分别为C、O、F、Na、Al、S。
(1)同周期元素自左向右非金属性逐渐减弱,所以非金属性最强的是F。
(2)同主族元素自上而下原子半径逐渐增大,所以S的原子半径大于O的原子半径。
(3)C的原子序数是6,所以原子结构示意图为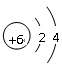 。
。
(4)④、⑤两种元素的最高价氧化物对应的水化物分别是氢氧化钠和氢氧化铝,氢氧化铝是两性氢氧化物能溶于强碱,方程式为Al(OH)3+OH-=AlO2-+2H2O。
本题难度:一般
5、选择题 短周期金属元素A和非金属元素B,它们的简单离子为aAm+和bBn-,已知bBn-比aAm+多两个电子层,则a的取值可以是:①1 ?②2 ?③3 ?④4 ?⑤5
A.①②
B.③④
C.①④
D.③⑤
参考答案:B
本题解析:bBn-比aAm+多两个电子层,且二者都是短周期元素,则两种微粒的核外电子数相差是10个18-2=16个。又因为A是金属,所以A只能是第二周期的Li或Be元素,即a=3或4,答案选B。
点评:该题设计新颖,基础性强,注重单体的灵活性,有利于激发学生的学习兴趣和学习积极性。该题的关键是熟练掌握核外电子排布规律,然后结合题意灵活运用即可,有利于培养学生的逻辑思维能力和发散思维能力。
本题难度:一般