��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���б仯�У����������������ʵ�ֵ���
[? ]
A.CaCO3��CaO
B.CuO��Cu
C.Zn��ZnSO4
D.H2O(g)��H2O(l)
�ο��𰸣�C
���������
�����Ѷȣ���
2��ѡ���� ���������ڵ�O2��2��ת��Ϊ�����Լ�ǿ�Ļ������������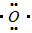 �ȣ���Щ�������ܼ�������˥�ϣ�����Ϊ������ɱ�֡����ҹ���ѧ�ҳ����ú���������Na2SeO3���������ڵĻ�������������������ʱ��
�ȣ���Щ�������ܼ�������˥�ϣ�����Ϊ������ɱ�֡����ҹ���ѧ�ҳ����ú���������Na2SeO3���������ڵĻ�������������������ʱ��
Na2SeO3��������
[? ]
A����ԭ��
B��������
C�����������������ǻ�ԭ��
D�����Ͼ�����
�ο��𰸣�A
��������������ڻ��������������ԣ��������ƾ��л�ԭ�ԣ����������ڻ�������Ӧ������ֹ����˥�ϡ���ѡA.
�����Ѷȣ���
3��ѡ���� �����裨Si3N4����һ�������մɲ��ϣ�������ʯӢ�뽹̿�ڸ��µĵ������У�ͨ�����·�Ӧ�Ƶã�3SiO2+6C+2N2====Si3N4+6CO�����жԸ÷�Ӧ��˵����ȷ����
[? ]
A���÷�Ӧ����������SiO2��N2
B������1mol?Si3N4ʱ��ת��6mol����
C���÷�Ӧ���������ͻ�ԭ��������Ϊ9�s7
D���÷�Ӧ�Ļ�ԭ����ΪSi3N4
�ο��𰸣�D
���������
�����Ѷȣ���
4��ѡ���� ���ж��������ʵ���������ģ�������
A��SO2��NH3��HC1��CO���л�ԭ��
B��SO3��NO2��ClO2��CO2����������
C��HC1��H2S��PH3��SiH4�����ȶ�������
D��H2SiO3��H3PO4��H2SO4��HClO����������ǿ
�ο��𰸣�A��SO2��NH3��HC1��CO���л�ԭ�ԣ������������ʹ���������ɫ�����Ĵ�������Ӧ���������̺�Ũ������������һ����̼��ԭ����ͭ�ķ�Ӧ��֤������һ�㣬��A��ȷ��
B�����ڸۻ��м�۵�Ԫ�ؾ��������ԣ�SO3��NO2��ClO2��CO2���������ԣ���B��ȷ��
C��ͬ����Ԫ�ص�ԭ�ӣ������ң�Ԫ���⻯����ȶ�������ǿ������HC1��H2S��PH3��SiH4�����ȶ�����������C��ȷ��
D��ͬ����Ԫ�ص�ԭ�ӣ�����������������ˮ������������ǿ������H2SiO3��H3PO4��H2SO4��HClO4����������ǿ����Ԫ������������ˮ����Ӧ��HClO4����D����
��ѡD��
���������
�����Ѷȣ�һ��
5��ѡ���� �������У�ֻ�л�ԭ�Ե����ǣ�������
A��H+
B��H2O
C��Cl2
D��S2-
�ο��𰸣�A��H+��HԪ�صĻ��ϼ۴�����ۣ���ֻ�������ԣ���A����
B��H2O��HԪ��Ϊ+1�ۣ�������ۣ�OԪ��Ϊ-2�ۣ�������ͼۣ���H2O�������������л�ԭ�ԣ���B����
C��Cl2��ClԪ�صĻ��ϼ�Ϊ0�������м��̬����Cl2�������������л�ԭ�ԣ���C����
D��S2-��SԪ�صĻ��ϼ�Ϊ-2�ۣ�������ͼۣ���ֻ�л�ԭ�ԣ���D��ȷ��
��ѡD��
���������
�����Ѷȣ���