��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ӷ���ʽ�У��������
A������ˮ��Ӧ��Na+H2O=Na++OH��+H2��
B������������������Һ��Ӧ��H++OH��=H2O
C������ϡ���ᷴӦ��Fe+2H+=Fe2++H2��
D���Ȼ�����Һ����������Һ��Ӧ��Ag++Cl��=AgCl��
�ο��𰸣�A
�������������ˮ��Ӧ��Na+H2O=Na++OH��+H2����ԭ�Ӳ��غ㡣��ѡA��
���������ӷ���ʽ�����ж�Ҫע�⣺���Ƿ���Ͽ���ʵ�����Ƿ���������غ㡢���Ƿ���ϵ���غ㡢���Ƿ���ϵ�ʧ������ȡ����ܵ���������ʲ�����ӡ�ע������������������ȡ�
�����Ѷȣ�һ��
2��ѡ���� �������ӷ���ʽ��ȷ���ǣ�������
A���Ȼ�������Һ��ͨ����������Fe2++Cl2=Fe3++2Cl-
B�����廯������Һ��ͨ�����������Fe2++2Br-+2Cl2�TFe3++Br2+4Cl-
C����̼�������Һ�м���������NaOH��Һ��NH4++OH-=NH3?H2O
D������������ʵ���Ũ�ȵ�NaHCO3��Һ��Ba��OH��2��Һ���ʱ������Ӧ��HCO3-+Ba2++OH-�TBaCO3��+H2O
�ο��𰸣�A���Ȼ�������Һ��ͨ���������������ӷ�ӦΪ2Fe2++Cl2=2Fe3++2Cl-����A����
B�����廯������Һ��ͨ��������������ӷ�ӦΪ2Fe2++4Br-+3Cl2�T2Fe3++2Br2+6Cl-����B����
C����̼�������Һ�м���������NaOH��Һ�����ӷ�ӦΪHCO3-+NH4++2OH-=NH3?H2O+CO32-����C����
D������������ʵ���Ũ�ȵ�NaHCO3��Һ��Ba��OH��2��Һ���ʱ������Ӧ�����ӷ�ӦΪ
HCO3-+Ba2++OH-�TBaCO3��+H2O����D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
3��ѡ���� �������ӷ���ʽ����ȷ����
[? ]
A����ˮ��������Һ�ķ�Ӧ��H++OH-=H2O
B��ͭ���Ȼ�����Һ��Ӧ��Fe3++Cu=Fe2++Cu2+
C������������Ũ����ķ�Ӧ��MnO2+4H++4Cl-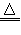 Mn2++Cl2��+2H2O
Mn2++Cl2��+2H2O
D��̼������������������Һ�ķ�Ӧ��HCO3-+OH-=CO32-+H2O
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4��ѡ���� ��a L����״����CO2ͨ��100mL 3mol��L-1 NaOH��Һ�У����и���Ϊͨ��CO2��������Һ�ڷ�����Ӧ�����ӷ���ʽ�����в���ȷ����?
A��a =3.36ʱ��CO2 + 2OH- = CO32- + H2O
B��a =4.48ʱ��2CO2 + 3OH- = CO32- + HCO3- + H2O
C��a =6.72ʱ��CO2 + OH- = HCO3-
D��a =8.96ʱ��3CO2 + 4OH- = CO32- + 2HCO3- + H2O
�ο��𰸣�D
���������A��a=3.36ʱ���ʵ���Ϊ��n��CO2��=0.15mol��n��NaOH��=0.3mol��n��CO2����n��NaOH��=0.15mol��0.3mol=1��2����Ӧ���ӷ���ʽΪ��CO2+2OH-=CO32-+H2O����A��ȷ��
B��a=4.48ʱ�����ʵ���Ϊ��n��CO2��=0.2mol��n��NaOH��=0.3mol��n��CO2����n��NaOH��=0.2mol��0.3mol=2��3���������ƺͶ�����̼ǡ�÷�Ӧ����̼���ƺ�̼�����ƣ���Ӧ���ӷ���ʽ����ֱƽ��д��Ϊ��2CO2+3OH-=CO32-+HCO3-+H2O����B��ȷ��
C��a=6.72ʱ���ʵ���Ϊ��n��CO2��=0.3mol��n��NaOH��=0.3mol��n��CO2����n��NaOH��=0.3mol��0.3mol=1��1����Ӧ���ӷ���ʽΪ��CO2+OH-=HCO3-����C��ȷ��
D��a=8.96ʱ���ʵ���Ϊ����n��CO2��=0.4mol��n��NaOH��=0.3mol��n��CO2����n��NaOH��=0.4mol��0.3mol=4��3��n��CO2����n��NaOH����1��1����Ӧ���ӷ���ʽΪ����CO2+OH-=HCO3-����D����
��ѡD��
���������⿼���˶�����������ӷ���ʽ����д�����Ͳ����жϣ���Ҫ������ͬ���ﲻͬ�IJ����ж��ǽ���ؼ���
�����Ѷȣ�һ��
5��ѡ���� �±������ۺ������ǣ�?��
ѡ��
| ��ѧ��Ӧ�������ӷ���ʽ
| ����
|
A
| FeO��������ϡ���ᷴӦ��
FeO+2H+=Fe2++H2O
| ��ȷ
|
B
| ���������Һ�м�������������Һ��
Ba2++ SO42-=BaSO4��
| ��ȷ
|
C
| ̼��������Һ�еμ�������ʯ��ˮ��
2HCO3-+Ca2++ 2OH-=
CO32- +CaCO3��+2H2O
| ����HCO3-��OH-��H2O��ϵ��Ӧ��Ϊ1����������û��CO32-?
|
D
| ��ʳ�׳�ȥˮƿ�е�ˮ����
CaCO3+2H+=" " Ca2++H2O+CO2��
| �����������ᣬ��Ӧд��H+��ʽ
�ο��𰸣�D
���������A������Ϊǿ�������ᣬFe2+�ᱻ������������ȷ��Ϊ��FeO+10H++NO3��=Fe2++NO��+5H2O��B����Ba2++ SO42-=BaSO4���⣬��ͬʱ����NH4����OH��=NH3��H2O��C������ʯ��ˮΪ���������Բμӷ�Ӧ��Ca2+�� 2OH-�����ʵ���֮�Ⱦ�Ӧ��Ϊ1��2��ԭ���ӷ���ʽ��ȫ��ȷ��D��������ȫ��ȷ����ȷ�����ӷ���ʽΪ��CaCO3+2CH3COOH= Ca2++2CH3COO��+H2O+CO2��
�����Ѷȣ�һ��
|