��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��8�֣�ij�о���ѧϰС�飬������������ҩƷ��֤�����Ͻ�(��Cu��Fe��Zn�����������)������Ũ���ᷴӦ�����������к�NO(N2��O2�����������ɿ��ƣ�����Һ���¶ȣ�
NO2��21�棬NO��-152��)
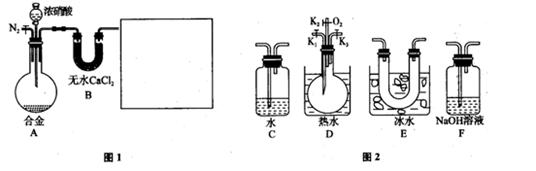
(1)��ͼ2��ѡ��ǡ����������ͼ1������������ѡ������������˳��(����������ӣ�����������)Ϊ_________(2��).
(2)��Ӧǰ��ͨ��N2Ŀ����_______________________________________(2��).
(3)ȷ�������к�NO��������______________________ _________________(2��).
_________________(2��).
(4)�����У�Ũ����(������a mol)��ȫ��Ӧ����ԭ����ֻ��NO��NO2������ԭ��������ʵ���n��ȡֵ��ΧΪ_________________________________________(3��).
2��ѡ���� ���й����У�û������ʵ��������ǣ�?��
A����Fe��NO3��2��Һ�еμ�ϡ����
B����HC1ͨ��NaAlO2��Һ��
C����������SO2��Ʒ����Һ
D����̼��������Һ�еμ�����������Һ
3��ʵ���� ����þ�������̼�ķ�Ӧ�Ʋ⣬��Ҳ���ڶ�����̼��ȼ�գ��ҹ���������Ϊ̼���ơ������ơ�̼�е����ֻ����֡�ij��ȤС������ڶ�����̼��ȼ�պ�IJ�����ж��ԺͶ���̽����
��1���������ΪNa2CO3��Na2O��C�Ļ������ʵ�鷽������֤���е�Na2CO3��Na2O���ڴ����д��ʵ�鲽�衢Ԥ������ͽ��ۡ�����֪����ʱBaCO3������Һ��pH=9.6��
��ѡ�Լ���������ϡ���ᡢBaCl2��Һ��Ba(OH)2��Һ������pH��ֽ����ȷ��0.1�����ձ����Թܡ��ιܡ���������������ɫ��
ʵ�����
| Ԥ������ͽ���
|
����1��ȡ����������Ʒ�ڽྻ�ձ��У�������������ˮ����ֽ��裬���ã�ȡ�ϲ���Һ���á�
| �в��ܵĺ�ɫ���塣
|
����2��ȡ��������1��Һ���Թ��У�?
?
| ?
?
|
����3��?
?
| ?
?
|
?
��2���������ΪNa2CO3��Na2O��C�Ļ���Ϊ��һ���ⶨ������Na2CO3�ĺ���������������ʵ�飺
����1��ȷ��ȡw���������ܽ⡢���˺�ȷ���Ƴ�250mL��Һ��
����2��ȷ��ȡ25.00mL������Һ����ƿ�У��μӼ���ָʾ��A���μ�c mol/L�ı���������Һ��pHԼΪ8.2��̼����Ҫ������ʽΪHCO3�D����������������ΪV1mL���ٵμӼ��μ��ȣ��������������������Һ�ɻ�ɫ���ɫ��������������ΪV2mL��
����3���ظ�ʵ��3�Ρ��ζ��������
�ζ�
����
| ������Һ
�����/mL
| ���ı���������
|
V1/mL
| V2/mL
|
1
| 25.00
| 15.02
| 4.97
|
2
| 25.00
| 14.98
| 5.03
|
3
| 25.00
| 13.21
| 6.75
|
?
�ٲ���2�У���һ���ζ���ʹ�õ�Aָʾ��Ϊ?���ζ��յ������Ϊ?��
�ڼ���Na2CO3����������=?���ú�w��c�Ĵ���ʽ��ʾ��
4��ʵ���� ��ѧ��ȤС���ijƷ�������е�Ħ�����ɷּ��京����������̽����������ϣ�������Ħ������̼��ơ�����������ɣ������������ɷ���������ʱ�����������
��.Ħ���������������Ķ��Լ���
ȡ����������Ʒ����ˮ������衢���ˡ�
��1���������м������ NaOH��Һ�����ˡ�����������NaOH��Һ��Ӧ�����ӷ���ʽ��?��
��2������1��������Һ����ͨ�����������̼���ټ������ϡ���ᡣ�۲��������?��
��.������Ʒ��̼��ƵĶ����ⶨ
������ͼ��ʾװ�ã�ͼ�мг�������ȥ������ʵ�飬��ַ�Ӧ�ⶨC�����ɵ�BaCO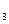 ������������ȷ��̼��Ƶ�����������
������������ȷ��̼��Ƶ�����������

����ʵ����̻ش��������⣺
��3��ʵ����������������ͨ������������ó��˿ɽ���B��C�еķ�Ӧ���⣬���У�________
��4��C�з�Ӧ����BcCO2�Ļ�ѧ����ʽ��__________________��
��5�����и����ʩ�У�������߲ⶨȷ�ȵ���_________�����ţ���
a.�ڼ�������֮ǰ��Ӧ�ž�װ���ڵ�CO2����
b.�μ�����˹���
c.��A-B֮������ʢ��Ũ�����ϴ��װ��
d.��B-C֮������ʢ�б���̼��������Һ��ϴ��װ��
(6)ʵ����ȷ��ȡ8.00 g��Ʒ���ݣ��������βⶨ�����BaCO2ƽ������Ϊ3.94 g������Ʒ��̼��Ƶ���������Ϊ__________��
��7��������Ϊ���زⶨC�����ɵ�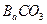 ������ֻҪ�ⶨװ��C������
������ֻҪ�ⶨװ��C������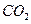 ǰ��������һ������ȷ��̼��Ƶ�����������ʵ��֤�����˷����ⶨ�Ľ������ƫ�ߣ�ԭ����______.
ǰ��������һ������ȷ��̼��Ƶ�����������ʵ��֤�����˷����ⶨ�Ľ������ƫ�ߣ�ԭ����______.
5��ʵ���� ��5�֣�Ϊ��̽����������ˮ�����������������ʵ��
����һ��ȡ��֧��ͬ���Թܱ��Ϊ1��2��3�����Թ������μ�������ҩƷ
�Թܱ��
| 1
| 2
| 3
|
�����ҩƷ������
| 4 mL����ˮ
| 4 mL ����ˮ
+3��ŨH2SO4
| 4 mL ����ˮ
+3��NaOHŨ��Һ
|
3�μ����Լ�
2 mL��������
| 3�μ����Լ�
2 mL��������
| 3��ʯ����Һ
2 mL��������
|
�����������֧�Թ����ã�������ˮԡ��Լ75�棩�У�����Լ5 min�����ȹ����в�����
�ش��������⣺
��1�����������еĶ�����������Ӧ��������ʶ����ʵ��Ԥ�ڿɹ۲쵽����������ͼ�е�?��
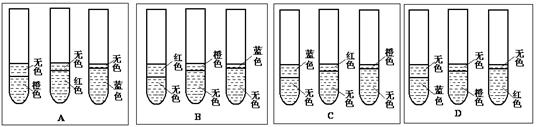
��2����ʵ��Է�Ӧ�¶ȵĿ��ƽ�Ϊ�ϸ����¶ȹ���ʱ����������Ҫ������?��
��3���ڲ�����У����Թܺ�ɹ۲쵽Һ�����Ի��ǣ���ԭ����?��
��4�������貽��ʵ�鷴Ӧ���ʽ���������Ҫԭ����?��
��5����ʵ�ʲ����У���ԣ�4���е�ԭ����иĽ���Ԥ�ڵ������Բ����ԣ������ֽ���ʵ�������¸Ľ�
�Թܱ��
| 1
| 2
| 3
|
�����ҩƷ������
| 4 mL����ʳ��ˮ
| 4 mL����ʳ��ˮ
+3��ŨH2SO4
| 4 mL����ʳ��ˮ
+3��NaOHŨ��Һ
|
3�μ����Լ�
2 mL��������
| 3�μ����Լ�
2 mL��������
| 3��ʯ����Һ
2 mL��������
|
ʵ�������Ԥ�ڵ���ȫһ�¡��������һ�Ľ�����Ҫ������?��